
|
Читайте также: |
Присутствие в одном из колец нафталина дезактивирующего электроноакцепторного заместителя предохраняет это кольцо от окисления:
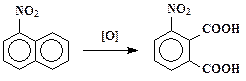
α -нитронафталин 3-нитрофталевая кислота
В общем случае при окислении многоядерных соединений окислению подвергается в первую очередь ядро, наиболее активное к электрофильной атаке, т.е. с наибольшей электронной плотностью.


Большое значение в промышленности красителей имеет окисление антрацена до антрахинона. В качестве окислителя в этой реакции чаще всего используют раствор бихромата натрия в 25 %-ной серной кислоте и кислород воздуха при температуре 170 – 175 °С (жидкофазное окисление) или 380 – 425 °С (парофазное окисление).
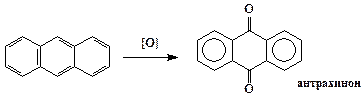
Окисление ароматических углеводородов до бензойной кислоты проходит через промежуточные стадии образования спирта и альдегида или кетона:

Для реакций окисления углеводородов действует правило: чем более окислен промежуточный продукт, тем легче он окисляется. Поэтому если надо остановить окисление, например, на стадии образования альдегида, приходится применять специальные приемы.
Так, при окислении толуола или его замещенных в кольце производных оксидом хрома(IV) в растворе уксусного ангидрида процесс удается остановить на стадии образования двухатомного спирта ArСН(ОН)2 путем связывания последнего уксусным ангидгидом и образования диацетата:

Диацетат устойчив к окислению в условиях синтеза и легко выделяется. Его гидролиз ведет к нестабильному двухатомному спирту, который, отщепляя воду превращается в альдегид:
:

В некоторых синтезах используется различие в температурах кипения исходного спирта и образующегося альдегида: более летучий альдегид успевает отогнаться из реакционного сосуда прежде, чем произойдет его дальнейшее окисление. На этом принципе, в частности, основан синтез бутаналя из бутанола-1:

Если в ароматической молекуле имеется две алкильные группы, одинаковые или разные, то иногда удается осуществить частичное селективное окисление. Так, каждый из трех изомерных ксилолов может быть окислен в соответствующую толуиловую кислоту с помощью азотной кислоты:

Хромовая кислота легче атакует пара -алкильные группы, чем мета -заместители той же природы. Можно также сказать, что длинная боковая цепь будет окисляться раньше, чем СН3-группа, т.к. реакции легче идут по вторичным a-СН-связям:

При окислении боковых цепей в фенолах или аминах для предупреждения более глубокого окисления необходимо защищать гидрокси- или амино-группы предварительным ацилированием:

Группа -NНСОСН3 менее активна, чем -NН2, и поэтому молекула пара -ацетотолуидина более устойчива, чем молекула пара -толуидина.
Дата добавления: 2015-10-21; просмотров: 157 | Нарушение авторских прав
| <== предыдущая страница | | | следующая страница ==> |
| Основные теоретические положения | | | Бензойная кислота (из бензилового спирта) |