
Читайте также:
|
Соли диазония неустойчивы и способны распадаться гетеролитически в растворителях с высокой диэлектрической проницаемостью:
Ar - N+ºN X-  Ar+ + N2 + X-
Ar+ + N2 + X-
или гомолитически (как правило, под действием катализаторов):
Ar - N+ºN X-  Ar. + N2 + X.
Ar. + N2 + X.
Направление распада зависит от аниона соли диазония и растворителя. Гомолизу способствуют в основном анионы слабых кислот, но в неводных растворах таким образом распадаются даже хлориды. Растворители с высокой диэлектрической проницаемостью способствуют гетеролитическому распаду (общая закономерность).
Диазосоединения широко используются для замены диазогруппы в аренах на различные функциональные группы. Иногда это единственный метод получения нужного продукта.
Ниже приведены наиболее часто применяемые в лаборатории синтезы с применением диазосоединений. Около каждой реакции указывается, если это достоверно известно, по какому механизму она протекает: ГТЛ (гетеролитически) или ГМЛ (гомолитически).
Замещение диазониевой группы гидроксилом:
Ar-N+ºN + H2O 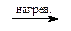 Ar-OH + N2 + H+ Ar-OH + N2 + H+
| (ГТЛ) |
2. Замещение диазогруппы на Cl, Br, CN и CNS (реакция Зандмейера). Осуществляется путем разложения соли диазония в присутствии соответствующих координационных соединений меди(I) ([CuCl4]3-, [CuBr4]3-, [Cu(CN)4]-, [Cu(CNS)4]3-):
Ar-N+ºN + X- 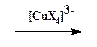 Ar-X + N2 Ar-X + N2
| (ГМЛ) |
Доказано, что этот процесс идет через промежуточное образование арильного радикала. Поставщиком электрона, необходимого для гомолитического разрыва связи С-N, является ион меди в степени окисления +1 (схематично):
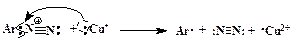
Далее ион Cu2+ вновь превращается в Сu+, забирая электрон у галогена, и радикал Х· образует ковалентную химическую связь с Ar ·:

Таким образом, медь в реакции Зандмейера служит переносчиком электрона.
Образованием в промежуточной стадии арильных радикалов объясняется прохождение ряда побочных процессов при реакциях Зандмейера:
а) Образование диарилов:
Ar. + Ar.  Ar-Ar
Ar-Ar
б) Образование производных азобензола:

3. Замещение диазогруппы на иод непосредственно действием йодистого калия на водный раствор соли диазония без катализатора:
Ar-N+ºN + I-  Ar-I + N2
Ar-I + N2
В случае реакции с йодид-анионом катализатор не нужен, т.к. роль переносчика электрона способен выполнить сам иодид-ион.
4. Разложение сухого тетрафторбората диазония с образованием фторзамещенных:
[Ar-N+ºN] [BF4]-  Ar-F + BF3 + N2 Ar-F + BF3 + N2
| (ГТЛ) |
5. В ряде случаев диазогруппа может быть замещена на сульфохлоридную группу и нитрогруппу:
Ar-N+ºN Cl- + SO2  Ar-SO2Cl + N2
Ar-SO2Cl + N2
Ar-N+ºN SO4H- + NaNO2  Ar-NO2 + N2 + NaHSO4
Ar-NO2 + N2 + NaHSO4
6. Взаимодействие диазониев с полисульфидами щелочных металлов:

Запрещается применять эту реакцию к диазониям, не содержащим групп, сообщающих растворимость в щелочной среде (-ОН, -СООН, -SО3Н), так как в этом случае наблюдаются сильные взрывы.
Если при диазотировании ароматических аминов образуется нерастворимая в воде соль диазония (например, при диазотировании сульфаниловой кислоты), ее необходимо перерабатывать только во влажном виде из-за чрезвычайной взрывчатости высушенных диазосоединений. Воронку и фильтр, на которых производилось отсасывание диазония, следует немедленно обмыть водой.
Дата добавления: 2015-10-21; просмотров: 150 | Нарушение авторских прав
| <== предыдущая страница | | | следующая страница ==> |
| Азосочетание | | | Йодбензол |