
|
Читайте также: |
Кривая комплексонометрического титрования обычно представляют собой зависимость рM = -lg[M] от степени оттитрованности. В
-3 2+
качестве примера рассмотрим кривую титрования 1,0-10" М Zn
-3
1,0-10" М раствором ЭДТА. Титрование проводится в аммиачном бу-
-2
ферном растворе, рН которого равен 9,50, а концентрация NH3 - 5-10"
2+
моль/л. Поскольку C(NH3) значительно больше C(Zn), будем счи-
2-
тать, [NH3] «C(NH3). Константа образования комплекса ZnY - равна 3,2-1016, а её десятичный логарифм - 16,50.
Катион цинка образует аммиачные комплексы, содержащие от 1 до 6 молекул лиганда. Общие константы образования этих комплексов: Р1 = 1,5-102; Р2 = 2,7-104; Р3 = 8,5-106; Р4 = 1,2-109; Р5 = 2,9-109; Р5 = 5,6-1012.
a^ 2+
Zn 1 + P1[NH3] + р 2[NH3]2 +... + р 6[NH3]6
--------------------------------------------------------------------------- 1,0 -10 -5
1 + 7,5 + 6,8 -101 + 1,1 -103 + 7,5 -103 + 9,1 -102 + 8,8 -104
lg a Zn2+ --5,00 a(Y4-) - 1 + 101^,26-9,50 = 1,5-10-1, lg a y4- --0,83.
lg e'ZnY2- - lg вZnY2- + lg aZn2+ + lg a Y4- = 16,50 - 5,00 - 0,83 -10,67 До начала титрования
pZn - - lg(C 0,Zn - a Zn2+ ) - - lgC 0,Zn - lg a Zn2+ До точки эквивалентности
1 - f
pZn -- lg C0,Zn - lg a Zn2+ - igj+f
Чтобы получить формулу для расчёта величины pZn в точке эквивалентности, воспользуемся выражением PZnY^.
в - [ZnY2- ]
ZnY C7n - C
Zn ■ ^Y
2+
где CZn и CY - общие концентрации, соответственно ионов Zn и ЭДТА, образовавшихся при диссоциации комплекса ZnY2-.
С учётом того, что в точке эквивалентности CZn = СЭдтА
179
| eZnY2- |
[ZnY2- ]
c2 C Zn
Если принять, что степень диссоциации комплекса ZnY - пренебрежимо мала, то
[ZnY2- ] C°,Zn
1 + f
С учётом того, что [Zn2+ ] - CZna Zn2+:
| C |
| pZn - - lg |
| aZn2+ - |
0,Zn
P'ZnY2-' (1 + f)
= 2lgP'ZnY2- - ^«C0,Zn - lgaz„2+ + 2lg(l + f)
Для того чтобы получить формулу для расчёта pZn после точки эквивалентности, также воспользуемся формулой, описывающей условную константу образования комплекса.
| f - 1 1 + f |
| 0,Y - |
CY - С
Так как С 0 Zn - С 0 y, то
| pZn - - lg |
| a Zn2+ |
C0(1 + f)
вZnY2- - (1 + f) - C0(f - 1)
= lg e'ZnY2- - lg aZn2+ + lg(f -1) - lg вZnY2- + lg a y4- + lg(f -1)
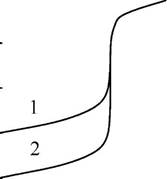
Формулы для расчёта рZn в различных точках кривой титрования и рассчитанные по ним значения рZn приведены в табл. 15.1. Кривая титрования показана на рис. 15.3.
На величину скачка титрования в комплексонометрии влияют (рис. 15.4):
• исходные концентрации титруемого иона и титранта,
• устойчивость комплекса катиона металла с ЭДТА,
• величины a(Y4-) и a m в условиях титрования.
Молярная доля Y4- зависит от рН, а величина a м - от концентрации комплексообразующего реагента и устойчивости образующихся комплексов
Табл. 15.1
3 2+
Расчёты для построения кривой титрования 1,0 -wj Мzn^
3 2
1,0-10' М раствором ЭДТА при рН 9,50 в присутствии 5-10' М NH3
| f | Расчётная формула | pZn |
| pZn --lgC0,Zn - lgaZn2+ | 8,00 | |
| 0,10 | 1-f pZn - lgC0,Zn lgaZn2 +!g_. Zn 1 + f | 8,09 |
| 0,50 | аналогично | 8,48 |
| 0,90 | аналогично | 9,28 |
| 0,99 | аналогично | 10,3 |
| 0,999 | аналогично | 11,3 |
| 1,00 | pZn - hg P'ZnY2- - "~lgC0JZn - lg aZn2 + + ^ + f) | 12,0 |
| 1,001 | pZn - lg PZnY2- + lg ay4- + lg(f - 1) | 12,7 |
| 1,01 | аналогично | 13,7 |
| 1,10 | аналогично | 14,7 |
| 1,50 | аналогично | 15,4 |
 Рис. 15.3. Кривая титрования 1,0 -10 3 М Zn2+ 1,0-10-3 М раствором ЭДТА при рН 9,50 в присутствии 5-101 М NH3
Рис. 15.3. Кривая титрования 1,0 -10 3 М Zn2+ 1,0-10-3 М раствором ЭДТА при рН 9,50 в присутствии 5-101 М NH3
|
| pM |
| pM |
| A |
| Б |
| 10 8 6 4 2 0 |
| 10 8 6 4 2 |
|
0,0 0,5 1,0 1,5
| 0,0 0,5 1,0 1,5 f |
f
| pM |
| B |
| Г |
pM

|
| 0,5 |
| 1,0 |
| 1,5 |
| 0,0 |
| 0,5 |
| 1,0 |
| 1,5 |
0,0
f
Рис. 15.4. Влияние различных факторов на величину скачка комплексоно- метрического титрования
А - концентрация титруемого иона (pH 10, Ca2) - 1) 1,0 -10-4 М; 2) 1,0 -10-2 М;
Б -устойчивость комплекса (рН 10, 1,0 -10-2 М) - 1) Ca2+, 2) Ba2+;
B - pH (Ca2+, 1,0 -10-2 М) - 1) pH 10; 2) pH 7;
Г - концентрация NH3 (рН 9,5, 1,0 -10-3 М Zn2+) - 1) [NH3] = 1-10-1 М; 2) [NH3] = 5-10-2 М
Изменение исходной концентрации титруемого вещества и концентрации вспомогательного реагента (а также и рН, если происходит образование гидроксокомплексов металла)влияют на ход кривых титрования до точки эквивалентности, в то время какpH и устойчивость комплекса -после точки эквивалентности.
| f |
Для каждого металла существует определённое значение рН, ниже которого комплексонометрическое титрование с удовлетворительной погрешностью оказывается невозможным.
При начальной концентрации титруемого катиона 1-10 моль/л и допустимой погрешности < 0,1% минимальная величина условной константы образования комплекса металла с ЭДТА составит
- [MY] - 110 -2 -1 108
PMY -------------------------------- ТТ - 1-10
CM - CY (1 -10-5)2
Таким образом, комплексонометрическое титрование
Дата добавления: 2015-09-07; просмотров: 188 | Нарушение авторских прав
| <== предыдущая страница | | | следующая страница ==> |
| Свойства этилендиаминтетрауксусной кислоты и её взаимодействие с катионами металлов | | | Способы обнаружения конечной точки титрования. Металлоиндикаторы |