
Читайте также:
|
Подведенная к телу теплота Q расходуется на увеличение его внутренней энергии U и на совершение работы А. В дифференциальной форме уравнение первого закона (начала) термодинамики (в отсутствие обмена веществом) имеет вид
dQ = dU + dA.
Правило знаков. Теплота, подведенная к телу, считается положительной, а отведенная – отрицательной. Работа, произведенная телом, считается положительной, а работа, совершенная над телом,– отрицательной.
В СИ единицей измерения энергии является джоуль (Дж=Н·м). Теплота и работа как формы передачи энергии имеют ту же единицу измерения.
Внутренняя энергия является функцией состояния. Ее изменение в ходе любого термодинамического процесса, переводящего тело (термодинамическую систему) из одного равновесного состояния в другое равновесное состояние, определяется лишь ее значениями в начальном и конечном состояниях, т.е. D U = U 2– U 1. Это означает, что dU является полным дифференциалом (dQ и dА таким свойством не обладают). Энергия – величина экстенсивная (аддитивная), т.е. энергия системы равна сумме энергий составляющих частей системы.
В случае, когда тело совершает работу только против сил внешнего давления, dА=PdV (работа расширения). Соответственно, уравнение первого закона термодинамики для удельных (массовых) величин с учетом правила знаков имеет вид
du = dq – Pdv. (4.1)
Здесь u=U/M (Дж/кг), q=Q/M (Дж/кг), v=V/M (м3/кг).
Энтальпия H=U+PV (Дж) так же, как и внутренняя энергия, является функцией состояния, т.к. P, V – параметры состояния. Поскольку du=dh–Pdv–vdP, уравнение первого закона в удельных величинах может быть записано в форме
dh = dq + vdP (Дж/кг).(4.2)
Произведение vdP называется располагаемой работой.
Идеальный газ. Согласно закону Джоуля внутренняя энергия идеального газа зависит только от температуры. Так как для идеального газа Pv = RT, то этим свойством обладает и энтальпия идеального газа. Прямым следствием закона Джоуля являются равенства
 (Дж/кг).
(Дж/кг).
сv, cp (Дж/кг K) – удельные теплоемкости в процессах подвода тепла при постоянном объеме и постоянном давлении соответственно.
Таким образом, для идеального газа уравнения (4.1) и (4.2) имеют вид
 (4.3)
(4.3)
Вычитая из первого уравнения второе, получим для удельных массовых теплоемкостей

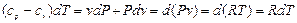 (Дж/(кг K))
(Дж/(кг K))
и, т.к. R=R 0/m,
 (формула Р.Майера).
(формула Р.Майера).
Отсюда для удельных молярных (мольных) теплоемкостей
 (Дж/кмоль K).
(Дж/кмоль K).
Удельная объемная теплоемкость для газов (с *) приводится к объему при нормальных физических условиях (V н):
с *=μ с /22,41 (Дж/м3 с)
и
сp *– сv *= R 0/22,41 (Дж/м3 K).
Для каждого вещества значения теплоемкостей определяются экспериментально и представлены в справочной литературе. Для оценочных расчетов можно принимать значения молярных теплоемкостей для разреженных газов (кДж/кмоль K), приведенные в табл. 4.1.
Таблица 4.1
| Газ | 
| 
|  – теория – теория
|
| Одноатомный | 12,56 | 20,93 | 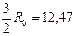
|
| Двухатомный | 20,93 | 29,31 | 
|
| Трехатомный | 29,31 | 37,68 | 
|
Следует различать истинную и среднюю теплоемкости.
По определению истинная теплоемкость c=dq/dT. Это функция температуры и процесса. Средняя теплоемкость связана с температурным интервалом:  ,
,  . Очевидно,
. Очевидно,
что  . Подведенное тепло (энергия в форме тепла) рассчитывается обычно с использованием средних значений теплоемкостей:
. Подведенное тепло (энергия в форме тепла) рассчитывается обычно с использованием средних значений теплоемкостей:
 .
.
Обычно знак усреднения (черта) опускается при использовании этих формул.
Замечание 1. С целью унификации таблиц и диаграмм принято считать, что внутренняя энергия равна нулю в «тройной» точке воды:
P = 610,8 Па; T = 273,16К=0,01ºC; v = 0,0010002 м3/кг.
В этой точке h = 0,611 Дж/кг.
Замечание 2. В силу исторических причин в энергетике также используется (вне системы единиц СИ) как единица энергии калория:
международная – 1 кал =4,1868 Дж;
15-градусная – 1 кал=4,1858 Дж;
термохимическая – 1 кал = 4,1840 Дж.
Иногда энергию измеряют в «лошадиных силах в час»:
1 л.с.ч = 75 кгс·м/с·3600 с = 75·9,8065 Н·м/c·3600 с ≈ 2648 кДж.
1 л.с. ≈ 736 Дж/с = 736 Вт.
Дата добавления: 2015-10-29; просмотров: 175 | Нарушение авторских прав
| <== предыдущая страница | | | следующая страница ==> |
| Теплоемкость смеси идеальных газов | | | Пример решения задач |