
Читайте также:
|
Общий подход.
Спирты, как и галогеналканы, способны вступать в реакции нуклефильногозамещения по механизмам SN или SN2. Однако их реакционная способность в реакциях нуклеофильного замещения выражена в меньшей степени, чем у галогеналканов.
Причин сравнительной инертности спиртов в реакциях нуклеофильного замещения две.
Во-первых, атом кислорода в спиртах, будучи двухковалентным, одновременно связан не только с углеродом алкильной группы, но и с атомом водорода, еще менее электроотрицательным, чем углерод. Поэтому дефицит электронной плотности в молекуле спирта имеется не в одном, а в двух местах, причем в большей степени на a–атоме углерода:

Следовательно, положительный заряд на a–атоме углерода в спиртах значительно меньше, чем в галогеналканах.
Во-вторых, в результате реакций нуклеофильного замещения непосредственно спиртового гидроксила должен вытесняться чрезвычайно богатый энергией гидроксид-анион, что энергетически невыгодно:

Облегчить замещение спиртового гидроксила на нуклеофильные частицы можно, если проводить реакцию в среде минеральных кислот. При этом реакции замещения будет предшествовать протонирование атома кислорода гидроксильной группы, в результате чего увеличивается электроноакцепторные свойства атома кислорода, повышается электрофильность реакционного центра, а также формируется хорошая уходящая группа – бедная энергией молекула воды:

Для первичных спиртов характерны реакции SN2. Однако, если первичный спирт содержит объемистый радикал, не позволяющий нуклеофилу атаковать реакционный центр «с тыла», реакция либо не пойдет, либо пойдет по механизму SN1, включающему образование первичного карбокатиона, который перегруппировывается в более стабильный карбокатион вследствие 1,2 – миграции алкильной группы (перегруппировка Вагнера-Мейервейна).
К таким спиртам относится неопентиловый спирт.
Этап 1. Химизм реакции.
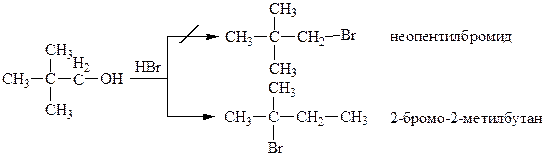
Механизм реакции (SN1).

Этап 2. Получение неопентилхлорида.

Заключение.
1. Неопентиловый спирт взаимодействует с HBr по реакции SN1, сопровождающейся перегруппировкой Вагнера-Мейервейна.
2. Неопентилхлорид можно получить реакцией монобромирования неопентана под действием УФ-облучения (SR) или неопентилового спирта и РBr3.
Обучающая задача № 5. Предложите схему синтеза простого эфира, исходя из бензола и метанола. Напишите химизм и механизм реакций, используемых в синтезе целевого продукта, а также химизм (и механизм) и внешние признаки реакций, с помощью которых его можно идентифицировать.
Дата добавления: 2015-07-20; просмотров: 523 | Нарушение авторских прав
| <== предыдущая страница | | | следующая страница ==> |
| Решение. | | | Решение |