
Читайте также:
|
Общий подход .
Реакция гидролиза – это реакция нуклеофильного замещения нуклеофильного фрагмента молекулы (например, галогена) на гидроксильную группу.
Реакционную способность в реакции гидролиза определяют следующие факторы:
1) электронодефицитность электрофильного реакционного центра субстрата, которая зависит от электроноакцепторного действия связанного с ним нуклеофильного атома;
2) полярность связи углерод-галоген;
3) поляризуемость связи углерод-галоген;
4) электронные эффекты заместителей;
5) пространственная доступность реакционного центра;
6) нуклеофильность реагента;
7) стабильность уходящей группы – нуклеофуга.
Рассмотрим эти факторы применительно к молекуле фторотана.
Фторотан является галогенопроизводным этана, у которого атомы водорода замещены на атомы галогенов - фтора, хлора, йода. Ковалентная связь углерод–галоген из-за различия электроотрицателности элементов сильно поляризована, что приводит к появлению электродефицитного реакционного центра – атома углерода, несущего частичный положительный заряд. Такой атом является электрофильным и может подвергаться атаке нуклеофильным реагентом. Вследствие сильной поляризации связи в процессе реакции происходит ее гетеролитический разрыв и замещение галогена на нуклеофил, т.е. происходит реакция нуклеофильного замещения (SN).
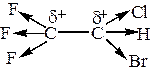
В молекуле фторотана имеются связи C–F, C–Cl, C–Br, полярность которых в этом ряду уменьшается в соответствии с уменьшением электроотрицательности галогена.
Однако для галогенов доминирующим фактором является не электроотрицательность, а поляризуемость, которая возрастает с увеличением атомного радиуса. Следовательно, поляризуемость связей C–F< C–Cl< C–Br увеличивается, поэтому и способность к гетеролитическому разрыву этих связей под действием нуклеофильного реагента увеличивается в этом ряду.
Дата добавления: 2015-07-20; просмотров: 68 | Нарушение авторских прав
| <== предыдущая страница | | | следующая страница ==> |
| Взаимодействие ароматического кольца с электрофильными реагентами включает два этапа. | | | Стабильность уходящей группы (нуклеофуга). |