
Читайте также:
|
Общий подход.
Озонолиз – многостадийный процесс, включающий реакцию окисления алкенов озоном с образованием озонидов и последующую реакцию гидролиза полученого озонида, в результате которой образуются карбонильные соединения: альдегиды и кетоны (при восстановительном озонолизе), кетоны и карбоновые кислоты (при окислительном озонолизе). Озонолиз используется в анализе алкенов для установления строения, определения местоположения двойной связи.
Окисление алкенов сопровождается разрывом либо только p-связи или расщеплением p- и s-связей. В первом случае углеродный скелет исходного алкена сохраняется (реакция гидроксилирования по Вагнеру, эпоксидирование), в другом случае происходит его фрагментация (озонолиз, окисление сильными окислителями в кислой среде). В зависимости от условий проведения реакции образуются соединения с кислородсодержащими функциональными группами – спирты, альдегиды, кетоны, карбоновые кислоты.
Этап 1. Установление структуры исследуемого алкена по продуктам его озонолиза.
Двойная связь в исходном алкене находится между атомами углерода, которые перешли в карбонильные группы конечных продуктов реакции озонолиза.
Поэтому чтобы установить структуру исследуемого алкена, следует записать структурные формулы 2–метилпропаналя (1) и метилэтилкетона (2), обратив карбонильные группы друг к другу; мысленно убрать атомы кислорода, соединить атомы углерода карбонильных групп двойной связью.
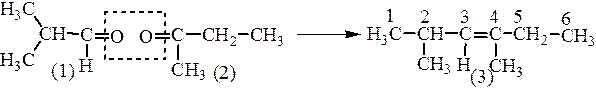
Таким образом, исследуемый алкен имеет структуру (3) – 2,4-диметилгексен-3.
Этап 2. Химизм процесса озонолиза 2,4-диметилгексена-3

Этап 3. Окисление алкенов сильными окислителями, например оксидом хрома (VI), хромовой смесью, перманганатом калия в кислой среде, также сопровождается разрывом двойной связи. Атомы углерода «осколков» углеродного скелета окисляются до максимально возможных степеней окисления: третичные атомы окисляются до кетонной группы, вторичные – до карбонильной группы, первичные – до оксида углерода.
В молекуле 2,4–диметилгексена–3 С-3 –– вторичный атом углерода (связан с двумя соседними атомами углерода), С-4 –– третичный атом углерода (связан с тремя соседними атомами углерода, поэтому при окислении перманганатом образуются карбоновая кислота и кетон.
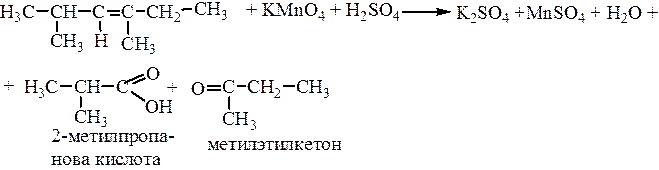
Реакция используется в анализе алкенов для установления местоположения двойной связи, а также для идентификации.
Этап 4.
Эпоксидирование – это реакция окисления алкенов пероксикислотами (реакция Прилежаева) или кислородом воздуха в присутствии катализатора Ag, в результате которой образуются эпоксиды (оксираны).
Реакция протекает по синхронному механизму, т.е. образование новых s-связей и разрыв p-связей происходит одновременно. Реакция эпоксидирования стереоселективна. Она проходит через переходное состояние, что предопределяет син-присоединение с образованием цис-оксирана.

Трехчленный a-оксидный цикл в эпоксидах – напряженный и легко раскрывается при действии нуклеофильных реагентов. При этом получаются гетерофункциональные соединения, содержащие спиртовой гидроксил и еще какую-нибудь функциональную группу в b-положении по отношению к спиртовой (OH, OR, NH2, C=N).
Взаимодействие замещенных эпоксидов с нуклеофильными реагентами проходит в соответствии с правилом Красуского: нуклеофильная атака атома происходит на наименее замещенный более электронодефицитный атом углерода оксидного цикла.

При гидролизе эпоксидов, как и в реакции Вагнера, образуются вицинальные диолы, но, в отличие от цис-диолов, получаемых в реакции Вагнера, образуются транс -диолы.
Механизм кислотного гидролиза эпоксидов.
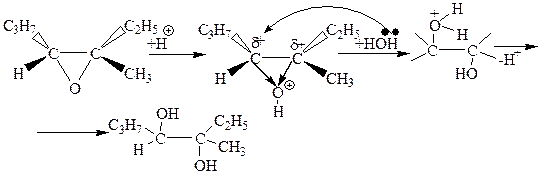 Этап 5. Реакция Вагнера, гидроксилирование
Этап 5. Реакция Вагнера, гидроксилирование
Одним из способов окисления алкенов, сопровождающееся разрывом только π– связи, является окисление перманганатом калия в нейтральной или слабощелочной среде. В результате реакции образуются двухатомные вицинальные спирты (гликоли). Эта реакция используется для идентификации алкенов по обесцвечиванию раствора перманганата калия и выпадению бурого осадка оксида марганца (IV).
Реакция протекает через стадию образования циклического эфира, за счет чего получающиеся гликоли имеют цис-конфигурацию.
Химизм реакции.

Механизм реакции.

Заключение. 1. Исследуемый углеводород ― 2,4–диметилгексен–4, что подтверждается продуктами озонолиза и окисления перманганатом калия в кислой среде.
2. Исследуемый углеводород в реакции эпоксидирования образует 3– изопропил–2–метил–2–этилоксиран; при окислении в условиях реакции Вагнера образуется 2,4–диметилгександиол–3,4.
Дата добавления: 2015-07-20; просмотров: 581 | Нарушение авторских прав
| <== предыдущая страница | | | следующая страница ==> |
| Механизм | | | Решение. |