
Читайте также:
|
Обучающая задача №1. Природный (-)-ментол (2-изопропил-5-метилциклогексанол-1) имеет следующую конфигурацию:

Приведите пространственную формулу (+)-ментола в клиновидной записи и проекционной формуле. Как различить (+) и (-)-ментолы? Сколько и каких стереоизомеров может быть у (-)-ментола? Оцените термодинамическую устойчивость природного ментола, используя метод конформационного анализа.
Решение.
Этап 1. Запишем строение (-)-ментола в виде проекционной формулы

Связь, изображенная сплошным клином, находится над воображаемой плоскостью циклогексанового кольца; связь, изображенная заштрихованным клином, находится под плоскостью кольца.
(+)-Ментол является энантиомером природного (-)-ментола, следовательно, у него конфигурация у всех асимметрических атомов противоположная.

(-)-ментол (1) (+)-ментол (2)
Ментол (2-изопропил-5-метилциклогексанол-1) имеет 3 асимметрических атома и, согласно формуле Фишера N=2n=23=8, может быть представлен 8 конфигурационными формулами. Одним из восьми стереоизомеров является природный (-)-ментол, второй изомер – его энантиомер (+)-ментол; остальные, то есть шесть стереоизомеров являются их диастереомерами.
Природный (-)-ментол и его энантиомер (+)-ментол можно различить, используя метод поляриметрии: оба изомера, являясь хиральными молекулами, вращают плоскость поляризации на одну и ту же величину угла, но в противоположные стороны.
Этап 2. Для того чтобы оценить термодинамическую устойчивость
(-)-ментола, необходимо использовать метод конформационного анализа, согласно которому соединение принимает ту конформацию, в которой максимально отсутствуют все виды напряжений. Такой конформацией для замещенных циклогексана является конформация кресла с экваториальным расположением объемных заместителей. Наибольшей термодинамической устойчивостью обладает тот конфигурационный изомер, у которого есть возможность принять конформацию с экваториальным расположением большинства объемных заместителей. Изобразим произвольную, например, 4С1 - конформацию кресла; перенесем заместители на соответствующие связи с учетом конфигурации, взяв за основу проекционную формулу (-)-ментола (1), в которой гидроксильная и метильная группы расположены над воображаемой плоскостью кольца. В 4С1 -конформации эти группы будут расположены также вверху над плоскостью кольца на аксиальных связях. Изопропильный радикал расположен под плоскостью кольца и занимает также аксиальное положение. Конформация, в которой все объемные заместители занимают аксиальное положение, энергетически невыгодная из-за 1,3-диаксиального взаимодействия. Но вследствие возможности инверсии эта конформация может перейти в 4С1. кресло (2), в котором все заместители окажутся экваториальными.
Таким образом, наибольшей термодинамической устойчивостью обладает (-)-ментол в 4С1- конформации и его энантиомер в конформации 4С1. Их диастереомеры менее термодинамически устойчивы, так как экваториальное положение могут занять не все, а только часть заместителей.

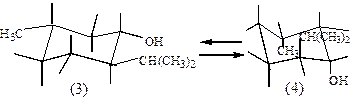


Обучающая задача 2. Треонин (2-амино-3-гидроксибутановая кислота) имеет трео -конфигурацию асимметрических атомов. Укажите конфигурацию этих центров по R,S-системе.
Решение.
Общий подход. Трео-эритро – номенклатура применяется для обозначения конфигурации в паре диастереоизомеров с двумя асимметрическими атомами.
Трео-изомер - диастереомер, у которого одинаковые лиганды в проекционной формуле Фишера расположены противоположно; эритро - изомер – диастереомер, у которого одинаковые лиганды расположены по одну сторону.
Этап 1. Напишем структурную формулу треонина (2-амино-3-гидроксибутановой кислоты), отметим асимметрические атомы углерода, изобразим пространственное строение в виде стандартных проекционных формул Фишера. Треонин имеет два асимметричных атома углерода, следовательно, может существовать в виде четырех стереомеров.


1 и 2; 3 и 4- пары энантиомеров, 1 и 3; 1 и 4; 2 и 3; 2 и 4 – пары диастереомеров.
Выделим стереохимический ключ. У a-аминокислот – это атом углерода, связанный с атомом водорода и аминогруппой и находящийся в a-положении по отношению к карбоксильной группе.
Так как треонин является природной a-аминокислотой и, следовательно, относится к L-стереохимическому ряду, выделим пару диастеромеров, относящихся к L-стереохимическому ряду. Такими диастереомерами являются (2) и (4). Конфигурация в стереохимическом ключе этих изомеров сходна с конфигурацией L-глицеринового альдегида (5). Изомер (2) является эритро-изомером: одинаковые лиганды – атомы водорода находятся в формуле Фишера по одну сторону; изомер (4) является трео-изомером: одинаковые лиганды расположены в формуле Фишера по разные стороны относительно вертикальной линии.
Таким образом, природная a-аминокислота треонин имеет трео-конфигурацию, представленную проекционной формулой (4).
Этап 2. Обозначение конфигурации по R,S- системе.
R,S-номенклатура является незаменимой, если:
1) соединение значительно отличается по структуре от стандарта – глицеринового альдегида;
2) соединение имеет несколько асимметрических атомов углерода и необходимо знать конфигурацию хирального центра не только в стереохимическом ключе, но и остальных хиральных центров.
Чтобы определить конфигурацию по R,S-системе необходимо:
1) определить старшинство заместителей (лигандов);
2) преобразовать проекцию Фишера в проекцию, в которой младший заместитель расположен внизу (или вверху) на вертикальной линии;
3) определить направление расположения лигандов в порядке уменьшения старшинства.
Если направление убывания старшинства лигандов совпадает с направлением движения часовой стрелки, т.е. вправо, то конфигурация хирального центра обозначается символом R (от лат. rectus – правый), если против часовой стрелки, т.е. влево – символом S (от лат.sinister - левый). Старшинство лигандов устанавливается по атомному номеру элемента, непосредственно связанного с центром хиральности. Если в «первом» слое наблюдается равенство, то процедуру распространяют на «второй» слой и т.д. Порядковые номера атомов с двойной или тройной связью соответственно удваивают, утраивают.
Определим лиганды для хирального центра С-2 и их старшинство в молекуле треонина:  отметим атомные
отметим атомные
6 7 6 1
номера: СООН, NH2, СН(ОН)СН3, Н.
Старшим заместителем является NH2 –группа, младшим – атом водорода. Остальные заместители в первом слое имеют одинаковый атомный номер. Определяем старшинство этих лигандов по второму слою. Во втором слое младшим лигандом является метил. Оба остальных лиганда имеют атом кислорода. Определяем старшинство этих лигандов, суммируя атомные номера, причем удваиваем атомный номер атома кислорода карбонильной группы.

Во втором слое суммарный атомный номер (24) больше для карбоксильной группы. Расположим заместители в ряд в порядке уменьшения старшинства: NH2>COOH>CH(OH)CH3>H
Преобразуем проекцию так, чтобы младший заместитель был на вертикальной линии (внизу или вверху), используя один из приемов, например, перемещая три заместителя в плоскости чертежа по часовой стрелке, не затрагивая четвертый (покажем это перемещение стрелкой). Напишем преобразованную проекцию и проведем стрелку в направлении от старшего заместителя через средний к младшему; уменьшение старшинства заместителей идет влево, что соответствует S-конфигурации С-2 хирального центра.

S-конфигурация С-2.
Определим лиганды и их старшинство для хирального центра С-3: 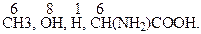 По первому слою старшим заместителем является ОН-группа, младшим - атом водорода. Определяем старшинство остальных заместителей по второму слою.
По первому слою старшим заместителем является ОН-группа, младшим - атом водорода. Определяем старшинство остальных заместителей по второму слою.

Во втором слое суммарный атомный номер больше для СН(NH2)COOH – группы. Расположим заместители в ряд в порядке уменьшения старшинства:
OH>СН(NH2)COOH>CH3>H.
Преобразуем проекцию, направив младший заместитель – атом водорода против часовой стрелки. В преобразованной проекции проведем стрелку от старшего заместителя через средний к младшему заместителю.

Направление уменьшения старшинства совпадает с направлением часовой стрелки, что соответствует R- конфигурации С-3 хирального центра.
В проекционной формуле Фишера около каждого хирального центра запишем соответствующий символ, обозначающий конфигурацию.

Обучающая задача № 3. Изобразите 4С1 - и 4C1 – конформации транс -1,2 - дибромциклогексана. Какая из этих конформаций должна преобладать с учетом только 1,3 - диаксиального взаимодействия? Какой еще тип внутримолекулярного взаимодействия проявляется в данной молекуле, если известно, что конформации с диэкваториальным и диаксиальным положением атомов брома энергетически равноценны?
Дата добавления: 2015-07-20; просмотров: 2171 | Нарушение авторских прав
| <== предыдущая страница | | | следующая страница ==> |
| Электронное строение цианогруппы (1) и изонитрильной группы (2) | | | Решение. |