
Читайте также:
|
Если рассматривать молекулу как осциллирующий диполь, то ориентация вектора её дипольного момента значима не только для реализации миграции энергии электронного возбуждения, но и при поглощении кванта электромагнитного излучения. Поглощаться будут только те кванты, вектор электрического поля у которых в момент взаимодействия с молекулой будет параллелен вектору ее дипольного момента. В обычных растворах, освещаемых неполяризованным излучением, этот факт большого значения не имеет, поскольку у растворенных молекул вектора дипольных молекул ориентированы случайным образом, а вектора электрических полей квантов излучения расположены хаотически. Но ситуация меняется, если освещать объект плоскополяризованным излучением. При таком освещении в образце поглощать кванты будут лишь те молекулы, дипольный момент которых оказался удачно ориентирован относительно вектора электрического поля фотона. Поскольку за время жизни возбуженного состояния у синглетно-возбужденных молекул значимого изменения положения вектора дипольного момента обычно не происходит, то и фотолюминесценция при ее возбуждении плоскополяризованным излучением оказывается частично поляризованной.
Количественно выраженность поляризации фотолюминесценции описывается двумя величинами – степенью поляризации фотолюминесценции и анизотропией фотолюминесценции. Обозначим эти величины соответственно Р и А.
Для регистрации выраженности поляризации фотолюминесценции в кюветное отделение флуориметра помещаются 2 поляризационных светофильтра, один из которых (поляризатор) располагается между источником возбуждающего света и образцом, а второй (анализатор) – между образцом и фотодетектором (рис. 22).

Рисунок 22. Схема регистрации поляризации фотолюминесценции. 1 – источник возбуждающего излучения; 2 – поляризатор; 3 – кювета с образцом; 4 – анализатор; 5 – фотодетектор. Начало координат помещено в центр кюветы с образцом. Направление возбуждения принимается за ось х. Поляризатор установлен таким образом, чтобы плоскость поляризации возбуждающего света была вертикальной (электрический вектор излучения параллелен оси z). Положение анализатора переменно. Если плоскость поляризации пропускаемого им излучения параллельна оси z, регистрируется величина J // . Если плоскость поляризации пропускаемого анализатором излучения параллельна оси х, регистрируется J^. Публикуется с модификациями по: Владимиров Ю.А., Потапенко А.Я. Физико-химические основы фотобиологических процессов. М.: «Дрофа», 2006, с. 70.
Регистрация Jфл в таких случаях осуществляется дважды, при совпадении (J //) плоскостей поляризации света у поляризатора и анализатора, и при их взаимно перпендикулярном расположении (J^). Степень поляризации фотолюминесценции затем рассчитывается по формуле:
|

Анизотропия фотолюминесценции рассчитывается несколько иначе:
|

Из выражений (98) и (99) очевидно, что величины Р и А связаны друг с другом, и, измерив одну из них, нетрудно затем рассчитать другую.
Очевидно, что степень поляризации фотолюминесценции будет зависеть от ряда обстоятельств:
(1) От угла между векторами электрического поля возбуждающего излучения и дипольного момента молекулы-люминофора (обозначим его b).
(2) От времени жизни возбужденного состояния данной молекулы.
(3) От скорости вращательного движения данной молекулы (которая, в свою очередь, зависит от температуры и вязкости среды в месте локализации люминофора).
Сначала рассмотрим зависимость поляризации от угла b. Пусть время реальное жизни возбужденного состояния у молекулы-люминофора будет достаточно мало для того, чтобы её вектор дипольного момента не успевал сильно измениться, а среда в месте локализации этой молекулы отличается высокой вязкостью. Ясно, что в такой ситуации поляризация фотолюминесценции должна быть максимально возможной. Обозначим ее степень Р0. Зависимость Р0 от угла b описывается уравнением Перрена-Яблонского:
|

Из этого уравнения, определив Р0, можно рассчитать величину b.
Фотолюминесценция, определяемая сиглет-синглетными излучательными переходами (флуоресценция), при её регистрации в схеме «под прямым углом», будет частично поляризована даже при ее возбуждении неполяризованным светом. Связано это с тем, что (1) колебания электрического поля излучения поперечны относительно направления распространения света и (2) поглощают свет и возбуждаются молекулы, вектор дипольного момента у которых удачно ориентирован в момент взаимодействия с фотоном (лежит в плоскости z0y на рис. 22). При возбуждении флуоресценции неполяризованным излучением зависимость Р0=f(b) описывается отличным от уравнения (100) выражением:
|
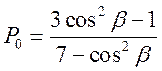
Из уравнений (100) и (101) вытекает, что при возбуждении фотолюминесценции плоскополяризованным светом предельная степень поляризации вторичного свечения Р0 будет меняться в пределах от +1/2 до -1/3 при изменении b от 0 до 90о, а при возбуждении неполяризованным светом при таком же изменении b - от +1/3 до -1/7.
Ранее рассматривалось возбуждение и регистрация фотолюминесценции при фиксированных длинах волн возбуждения и регистрации (соответственно lв и lфл). Но с помощью современных спектрофлуориметров возможно получить зависимости Р0=f(lв) и Р0=f(lфл). Эти спектры носят название соответственно «спектр поляризации фотолюминесценции по возбуждению» и «спектр поляризации фотолюминесценции по излучению».
Нужно заметить, что, поскольку излучательный электронный переход происходит всегда с одной и той же электронной орбитали (электронного уровня), поляризация фотолюминесценции в гомогенных растворах люминофоров не зависит от длины волны регистрируемых квантов вторичного свечения. Поэтому спектры поляризации фотолюминесценции по излучению представляют собой параллельные оси длин волн прямые. Гораздо информативнее поэтому спектр поляризации фотолюминесценции по возбуждению (рис. 23, б).
Для интерпретации спектра поляризации флуоресценции триптофана по возбуждению следует вспомнить, что у этой ароматической аминокислоты имеется 3 основных максимума поглощения – при 220, 280 и 296 нм. Самый длинноволновый максимум наблюдается в виде плеча на длинноволновом «склоне» преды-

Рисунок 23. Спектры поляризации флуоресценции триптофана по излучению (а) и по возбуждению (б).
Публикуется с модификациями по: Владимиров Ю.А., Потапенко А.Я. Физико-химические основы фотобиологических процессов. М.: «Дрофа», 2006, с. 73.
дущей полосы поглощения. Однако в положительную поляризацию флуоресценции триптофана основной вклад вносит именно полоса при 296 нм. Это указывает на то, что направления векторов дипольного момента у молекулы триптофана в момент поглощения кванта с длиной волны 296 нм и в момент последующего испускания кванта фотолюминесценции различаются незначительно. После же поглощения квантов с длинами волн 220 и 280 нм вектор дипольного момента триптофана успевает повернуться на 90о, в результате чего у возбужденной при таких длинах волн флуоресценции степень поляризации оказывается отрицательной. В целом же спектр поляризации флуоресценции триптофана при длинных волн возбуждения 220-320 нм будет суперпозицией эффектов всех полос поглощения. Поэтому он имеет довольно сложный вид.
Как уже указывалось выше, ранее рассмотренные уравнения справедливы только в случае, если молекулы люминофора практически не вращаются (т.е. направления векторов их дипольных моментов меняются со временем мало). В реальных же растворах эти молекулы, кроме всего прочего, участвуют во вращательной диффузии, из-за чего степень поляризации флуоресценции оказывается снижена. Выраженность вращательной диффузии молекул характеризуется двумя величинами, коэффициентом вращательной релаксации DВ и временем вращательной релаксации r.
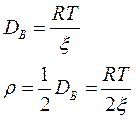
где R – универсальная газовая постоянная, Т – абсолютная температура, x - коэффициент трения в среде.
Иногда временем вращательной релаксации называют также величину s, которая равна:

Из-за вращения люминесцирующих молекул степень поляризации фотолюминесценции снижается, и измеренные значения Р оказываются (по модулю) меньше Р0. Степень деполяризации фотолюминесценции (1/Р) зависит от реального времени жизни возбужденных состояний (t) у молекул-люминофоров и времени релаксации r (которое, в свою очередь, зависит от вязкости среды h):
|

где V – объем 1 моля молекул.
Если для возбуждения фотолюминесценции используется поляризованное излучение, в уравнении (102) следует применять «-», а если неполяризованное – «+».
Из выражения (102) вытекает, что измерив величины Р, Р0 и t, можно определить значение вязкости среды в месте локализации люминофорной молекулы. К сожалению, это выражение справедливо только для молекул, форма которых примерно соответствует сфере. Для молекул несферической формы выражение (102) неприменимо.
При замене степень поляризации фотолюминесценции Р в уравнении (102) на соответствующую величину анизотропии фотолюминесценции А вид этого выражения значительно упрощается:
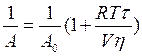 ,
,
откуда вытекает, что:
|
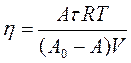
Величина А0 в данном случае – предельная анизотропия фотолюминесценции в вязких средах.
Как уже говорилось выше, в большинстве случаев в обычных водных растворах фотолюминесценция большинства веществ практически полностью деполяризована. Однако, если люминофорная молекула встраивается в липидный бислой биологической мембраны или связывается с белком, поляризация её фотолюминесценции заметно увеличивается. Это обстоятельство позволяет применять анализ поляризации фотолюминесценции флуоресцентных зондов для изучения величины вязкости в местах их локализации в биологических объектах. Именно таким образом установлено, например, что вязкость липидного бислоя в большинстве биологических мембран составляет 10-2-10-3 Па´с (что примерно соответствует вязкости растительного масла).
Дата добавления: 2015-07-25; просмотров: 194 | Нарушение авторских прав
| <== предыдущая страница | | | следующая страница ==> |
| Миграция энергии электронного возбуждения | | | Замедленная флуоресценция и фосфоресценция. |