
Читайте также:
|
а) К раствору соли сульфата меди (II) добавьте по каплям раствор гидроксида натрия. Отметьте цвет образовавшегося осадка. Полученный осадок растворите в избытке раствора аммиака, учитывая, что при этом образуется комплексное соединение с координационным числом комплексообразователя, равным 4. Как изменилась окраска раствора? Составьте молекулярные и ионно-молекулярные уравнения химических реакций.
б) К 1 мл раствора нитрата серебра добавьте по каплям насыщенный раствор хлорида натрия. Отметьте цвет образовавшегося осадка. Полученный осадок растворите в небольшом количестве раствора аммиака. При этом образуется комплексный ион 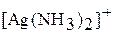 . Убедитесь, что в полученном растворе серебро не осаждается раствором хлорида натрия. Составьте молекулярные и ионно-молекулярные уравнения химических реакций.
. Убедитесь, что в полученном растворе серебро не осаждается раствором хлорида натрия. Составьте молекулярные и ионно-молекулярные уравнения химических реакций.
в) К 0,5 – 1 мл раствора нитрата ртути (II) добавьте по каплям концентрированный раствор иодида калия. Какой цвет имеет образовавшийся осадок? Осадок растворите в избытке иодида калия, при этом образуется комплексное соединение, в котором координационное число ртути равно 4. Составьте молекулярные и ионно-молекулярные уравнения химических реакций.
Напишите уравнения электролитической диссоциации полученного комплексного соединения. Запишите выражение для константы нестойкости комплекса.
Дата добавления: 2015-07-25; просмотров: 42 | Нарушение авторских прав
| <== предыдущая страница | | | следующая страница ==> |
| Опыт №5. Влияние среды на окислительные свойства перманганата калия | | | Гексацианоферрата (III) калия |