
Читайте также:
|
А) В пробирку налейте 1 – 2 мл раствора хлорида олова (II) и добавьте 2 – 3 капли раствора хлорида железа (III). К продуктам реакции добавьте еще одну каплю роданида аммония. Зачем добавляют роданид аммония? Почему при появлении красного окрашивания раствора необходимо прибавить дополнительное количество раствора хлорида олова (II)?
Напишите уравнения соответствующих химических реакций. Определите тип окислительно-восстановительной реакции. Коэффициенты в окислительно-восстановительной реакции подберите методом электронного баланса. Сделайте вывод об окислительно-восстановительных свойствах ионов 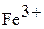 и
и 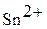 .
.
Б) Поместите в пробирку 2 – 3 капли раствора хлорида олова (II) и добавьте по каплям раствор гидроксида натрия. Что наблюдаете? Отметьте цвет образовавшегося осадка. Затем прибавьте избыток гидроксида натрия до полного растворения осадка. Почему растворился осадок? К образовавшемуся в пробирке веществу добавьте 3 – 4 капли раствора нитрата висмута (III). Что наблюдаете?
Напишите уравнения всех проведенных химических реакций. Определите тип окислительно-восстановительной реакции. Коэффициенты в окислительно-восстановительной реакции подберите методом ионно-электронного баланса. Сделайте вывод об окислительно-восстановительных свойствах иона 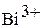 .
.
Дата добавления: 2015-07-25; просмотров: 87 | Нарушение авторских прав
| <== предыдущая страница | | | следующая страница ==> |
| Опыт №6. Полный гидролиз | | | Опыт №4. Окислительно-восстановительная двойственность пероксида водорода |