
Читайте также:
|
1. В цилиндре на 100 мл с помощью ареометра измерьте плотность раствора исходной концентрированной серной кислоты.
2. Найдите массовую долю серной кислоты в растворе по табл. 12. Если значение полученной плотности раствора лежит в интервале двух табличных значений, то массовую долю растворённой серной кислоты найдите методом интерполяции (графический способ).
Таблица 12
Плотность водных растворов серной кислоты
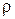 , г/мл , г/мл
| Содержание  , г , г
| 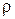 , г/мл , г/мл
| Содержание  , г , г
| ||
| в 100 г | в 1 л | в 100 г | в 1 л | ||
| 1,005 | 10,05 | 1,132 | 215,1 | ||
| 1,018 | 30,55 | 1,147 | 240,9 | ||
| 1,032 | 51,58 | 1,163 | 267,4 | ||
| 1,047 | 73,17 | 1,178 | 294,6 | ||
| 1,059 | 95,32 | 1,194 | 322,4 | ||
| 1,073 | 118,00 | 1,210 | 351,0 | ||
| 1,087 | 141,4 | 1,227 | 380,3 | ||
| 1,102 | 165,3 | 1,243 | 410,3 | ||
| 1,117 | 189,9 | 1,260 | 441,0 |
3. Для приготовления раствора заданной концентрациисерной кислоты найдите плотность её раствора, используя данные табл. 12.
4. Рассчитайте объём концентрированной серной кислоты и воды (мл), необходимый для приготовления раствора заданной концентрации.
5. Отмерьте мерным цилиндромрассчитанный объём концентрированной серной кислоты.
6. Отмерьте мерным цилиндромрассчитанный объём воды. В химический стакан вылейте небольшое количество воды (» 20 мл), отмеренной для приготовления раствора.
7. Осторожно вылейте в химический стакан концентрированную серную кислоту, постоянно перемешивая раствор стеклянной палочкой. Лейте концентрированную кислоту в воду, но не воду в кислоту!
8. Ополосните водой цилиндр, где находилась концентрированная серная кислота. Вылейте остатки водыиз цилиндра в химический стакан.
9. Раствор перемешайте. Если раствор нагрелся, то охладите его до комнатной температуры.
10. Приготовленный раствор серной кислоты вылейте в мерный цилиндр на 100 мл до 80 – 90 мл и измерьте плотность раствора ареометром.
11. Найдите в табл. 12 по плотности массовую долю (в %) приготовленного раствора серной кислоты. Если измеренная величина плотности окажется между двумя табличными значениями, то массовую долю серной кислоты приготовленного раствора найдите методом интерполяции (графический способ).
12. Сравните полученную величину массовой доли раствора серной кислоты с заданной и вычислите относительную ошибку опыта по формуле:
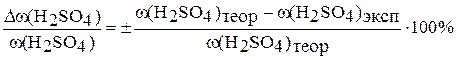 .
.
Дата добавления: 2015-07-25; просмотров: 55 | Нарушение авторских прав
| <== предыдущая страница | | | следующая страница ==> |
| Опыт №1. Приготовление раствора нитрата натрия с заданной массовой долей вещества в растворе | | | Опыт № 4. Приготовление раствора гидроксида натрия заданной молярной концентрации из кристаллического вещества. Проверка концентрации приготовленного раствора методом титрования |