
Читайте также:
|
Английские физики Д. Джоуль и У. Томсон (1853 – 1854) экспериментально обнаружили, что при адиабатном расширении газа без совершения полезной работы температура газа изменяется. Процесс такого необратимого расширения называется адиабатным дросселированием, а явление изменения температуры в этом процессе – эффектом Джоуля-Томсона.
Пропуская газ по теплоизолированной трубке с пористой перегородкой, Джоуль и Томсон обнаружили, что при расширении, которым сопровождается прохождение газа через перегородку, температура его несколько изменяется. В зависимости от начальных давления и температуры  имеет тот или иной знак и может быть
имеет тот или иной знак и может быть  =0. Это явление было названо явлением Джоуля-Томсона.
=0. Это явление было названо явлением Джоуля-Томсона.
· Если  , температура понижается, эффект считается положительным;
, температура понижается, эффект считается положительным;
· если  , газ нагревается, эффект считается отрицательным.
, газ нагревается, эффект считается отрицательным.
· 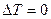 - нулевой эффект
- нулевой эффект
Схема опыта представлена на рис. 6.7..

· По трубе с крайне плохо проводящими тепло стенками устанавливается стационарное течение газа.
· В трубке имеется перегородка с мелкими порами (пробка из ваты), на которой происходит перепад давления от большого значения  до малого значения
до малого значения  , в результате чего газ сильно расширяется. Разность температур
, в результате чего газ сильно расширяется. Разность температур  фиксируется.
фиксируется.
Выделим мысленно часть газа, ограниченную сечениями 1 и 2.
По мере движения газа по трубе эти сечения перемещаются и спустя некоторое время оказываются в положениях  и
и  соответственно. Так как за перегородкой та же порция газа занимает больший объем, чем перед перегородкой, сечение 2 переместится на больший отрезок, чем сечение 1. Расширение газа происходит без теплообмена с внешней средой (процесс адиабатный), приращение внутренней энергии газа равно совершенной над ним работе:
соответственно. Так как за перегородкой та же порция газа занимает больший объем, чем перед перегородкой, сечение 2 переместится на больший отрезок, чем сечение 1. Расширение газа происходит без теплообмена с внешней средой (процесс адиабатный), приращение внутренней энергии газа равно совершенной над ним работе:
 (6)
(6)
Работу над данной порцией газа совершает граничащий с ней газ.
Слева на выделенную часть газа действует сила  (S - сечение трубки), направленная в сторону движения.
(S - сечение трубки), направленная в сторону движения.
Справа действует сила 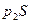 , противодействующая движению.
, противодействующая движению.
В итоге над рассматриваемой массой газа совершается работа: 
Здесь  - объем, занимаемый газом до расширения,
- объем, занимаемый газом до расширения,
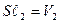 - объем газа после расширения.
- объем газа после расширения.
Тогда
 (7)
(7)
С учетом (7) выражение (6) принимает вид
 (8)
(8)
Таким образом, в опыте Джоуля-Томсона сохраняется величина  , называемая теплосодержанием или энтальпией.
, называемая теплосодержанием или энтальпией.
Проведем расчет для моля газа.
После расширения газ имеет большой объем, и его можно считать идеальным,
до расширения – газ Ван-дер-ваальсов, поэтому

Для внутренней энергии 
Подставив в (8), получаем 
Преобразуем 
Тогда 
и 
Знак  определяется знаком выражения, стоящего в скобках.
определяется знаком выражения, стоящего в скобках.
Нулевой эффект  =0 достигается при условии
=0 достигается при условии 
 Этому уравнению соответствует на плоскости (
Этому уравнению соответствует на плоскости ( ) кривая (рис.6.8).
) кривая (рис.6.8).
· Точки этой кривой определяют значения параметров  , при которых
, при которых 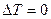 .
.
· Точки, лежащие выше кривой, определяют значения  , при которых
, при которых  , т.е. эффект отрицателен, при перемещении вверх от кривой первое слагаемое в скобках растет, скобка становится больше нуля).
, т.е. эффект отрицателен, при перемещении вверх от кривой первое слагаемое в скобках растет, скобка становится больше нуля).
· Точки, лежащие ниже кривой, определяют  , при которых эффект положителен.
, при которых эффект положителен.
Кривая на рис.6.8 называется кривой инверсии.
Таким образом, знак и величина эффекта определяются начальной температурой и начальным объемом.
· При  эффект всегда отрицательный.
эффект всегда отрицательный.
·  При
При  эффект будет положительным только при достаточно большом начальном объеме (т.е. при достаточно малом начальном давлении).
эффект будет положительным только при достаточно большом начальном объеме (т.е. при достаточно малом начальном давлении).
При данном начальном объеме (давлении) величина  линейно изменяется с начальной температурой
линейно изменяется с начальной температурой  (рис.6.9).
(рис.6.9).
Чем ниже начальная температура, тем сильнее охлаждается газ в результате эффекта Джоуля-Томсона.
Эффект Джоуля-Томсона обусловлен только отклонением газа от идеальности.
Для идеального газа  и выражение (8) принимает вид
и выражение (8) принимает вид 
т.е. 
Дата добавления: 2015-08-21; просмотров: 147 | Нарушение авторских прав
| <== предыдущая страница | | | следующая страница ==> |
| Внутренняя энергия реального газа. | | | Достижений учащегося |