
|
Читайте также: |
Возьмем для примера комплексный ион аммиаката никеля: [Ni(NH3)6]2+. Классическая структурная модель предсказывает наличие в этом ионе шести одинаковых связей Ni—N между ионом-комплексообразователем и лигандами. Поскольку в рамках метода ЛМО каждой связи соответствует пара перекрывающихся АО, ион Ni2+ должен располагать шестью идентичными друг другу вакантными АО, необходимых для принятия электронных пар от лигандов:

В то же время, орбитальная модель иона никеля приводит к другой картине, где вакантные АО иона никеля относятся к трем разным типам:
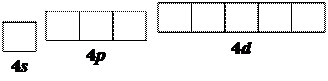
Следовательно, мы должны либо отказаться от применения метода ЛМО, либо предположить, что в процессе образования комплекса некоторые АО иона никеля претерпевают определенное изменение:

В результате такой "перегруппировки" из АО разных типов образуется такое же число одинаковых между собой орбиталей:
(4 s + 4 p' + 4 p'' + 4 p''' + 4 d' + 4 d'')Þ 6 j
Такой процесс называется гибридизацией, а образующиеся АО — гибридизованными или гибридными орбиталями (ГАО). Возможность такого преобразования вполне очевидна с точки зрения основного закона квантовой механики — принципа суперпозиции. Шаровые АО образуют всего лишь один их базисных наборов в пространстве состояний атома. Именно этот набор является стационарным в условиях полной изоляции атома, когда атом сферически симметричен. Однако когда атом взаимодействует с окружением из шести лигандов, расположенных по вершинам октаэдра, стационарным становится другой набор, а именно — набор гибридизованных АО. Отсюда вытекает и способ построения ГАО из исходных шаровых АО. Два любых базиса связаны линейным преобразованием посредством некоторого матричного оператора:

Другими словами, каждая ГАО является линейной комбинацией шаровых АО, задаваемой коэффициентами матрицы U. Конкретный тип гибридизации определяется симметрией окружения атома. Так, для иона никеля в октаэдрическом окружении шести лигандов стационарными являются ГАО sp 3 d 3 -типа, для атома углерода в тетраэдрическом окружении (метан, четыреххлористый углерод и др.) стационарным является базисный набор ГАО sp 3 -типа и т.д.
Несмотря на разнообразие геометрических форм молекул, обычно используется небольшой набор типов гибридизации, который соответствуют геометрически правильным многогранникам:
| Тип молекулы | Тип гибридизации АО центрального атома |
| Линейный L1—A— L2 | sp |
| Плоский треугольный АL3 | sp2 |
| Тетраэдрический AL4 | sp3 |
| Плоский квадратный ML4 | dsp2 |
| Тригональная бипирамида ML5 | sp3d или dsp3 |
| Октаэдр ML6 | sp3d2 или d2sp3 |
Можно отметить, что ГАО отличаются от шаровых АО в отношении пространственной формы. Если шаровые АО центрированы на ядре и принадлежат определенному типу симметрии группы О(3), то ГАО уже не являются центрально-симметричными. Хотя узловая структура сохраняется, части ГАО, разделенные узловой поверхностью, не равны друг другу. Следствием этого является наличие выделенной пространственной ориентации ГАО в пространстве. Для примера можно привести простейший случай sp - гибридизации: ГАО = s + px.

Из рисунка видно, что полученная sp - ГАО вытянута в положительном направлении оси Х и имеет не шаровую, а только аксиальную симметрию. Аналогичный вид имеет и вторая ГАО = s – px, но она ориентирована в противоположном направлении.
В случае молекулы метана исходный шаровой базис следует преобразовать так, чтобы в результате получить набор четырех ГАО, отличающихся друг от друга только ориентацией в пространстве около ядра атома С. Для решения этой задачи подходит следующее преобразование:


ГАО данного вида называются sp3 -гибридизованными (каждая является комбинацией s ‑ орбитали и трех р -орбиталей). Если построить полярные диаграммы этих ГАО, то будет ясно видна их идентичность друг другу. Единственное отличие между ними заключается в том, что они ориентированы по различным направлениям в пространстве, а именно — по вершинам тетраэдра.

Поскольку ГАО ориентированы вдоль определенных пространственных осей, соответствующих расположению химических связей в молекуле, геометрия совокупности ГАО всегда соответствует геометрии молекулы. Это позволяет, с одной стороны, подбирать тип гибридизации на основе информации о пространственной форме молекулы, а с другой стороны, по типу гибридизации предсказывать эту форму. Следует подчеркнуть, что концепция гибридизации АО необходима только в рамках приближенной модели ЛМО.
Дата добавления: 2015-07-20; просмотров: 250 | Нарушение авторских прав
| <== предыдущая страница | | | следующая страница ==> |
| Метод ЛМО | | | Эффекты сопряжения |