
Читайте также:
|
| хлороформ - ацетон 9:1 |
| барбитурат ы |
гексан - ацетон 4:1
неподвижная фаза силикагель
метанол - диэтиловый эфир - аммиак 98:1:1
4-
вещества основного характера
24.2.1. Методика получения плоскостной хроматограммы
Методика получения плоскостных хроматограмм включает в себя следующие этапы:
• предварительный этап - подготовка сорбента и исследуемой пробы, подготовка подвижной фазы, насыщение хроматографиче- ской камеры;
• нанесение исследуемой пробы на хроматографическую пластинку или бумагу;
• хроматографирование;
• высушивание хроматограммы;
• обнаружение пятен (зон) разделённых компонентов пробы.
Нанесение исследуемого раствора на хроматографическую пластинку или бумагу проводят градуированным капилляром, микрошприцом или микропипеткой. Капля наносится касанием капилляра или иглы поверхности пластинки (но не надавливанием, так как при этом можно повредить слой сорбента!). Для предотвращения смывания веществ с пластинки нанесение пятен проводят на линии, находящейся на расстоянии 1-2 см от нижнего края пластинки. Оптимальное количество исследуемого вещества (объём раствора), наносимого на пластинку, обычно определяется экспериментально. Если наносимое количество вещества слишком мало, то его можно не заметить при последующем проявлении. Нанесение на пластинку слишком
большого количества вещества приводит к перегрузке сорбента и, как следствие, размыванию пятна и уменьшению величины Rf (рис. 24.2).
После нанесения исследуемых веществ на хроматографическую пластинку или бумагу, последние помещают в хроматографи- ческую камеру и проводят хроматографиро- вание. Обычно процесс хроматографирова- ния ведут до тех пор, пока растворитель не поднимется на расстояние ~10 см от линии старта.
 Рис. 24.2. Изменение положения и формы пятна при увеличении количества вещества, нанесённого на пластинку
Рис. 24.2. Изменение положения и формы пятна при увеличении количества вещества, нанесённого на пластинку
|
| Способы получения плоскостных хроматограмм |
В зависимости от направления движения подвижной фазы различают следующие варианты плоскостной хроматографии (табл. 24.1)
Табл. 24.1.
|
После завершения процесса хроматографирования пластинку извлекают из хроматографической камеры и сушат. Высушенная пластинка представляет собой хроматограмму исследуемых веществ.
24.2.2. Анализ плоскостной хроматограммы
Разделяемые компоненты образуют на хроматографической пластинке или полоске хроматографической бумаги отдельные зоны (пятна). Примерный вид плоскостной хромато- граммы показан на рис. 24.3. Зоны окрашенных веществ можно обнаружить визуально. Для обнаружения неокрашенных соединений используют физические (например, облучение УФ- светом), химические (обработка хроматограммы различными реагентами- проявителями), а в некоторых случаях и биологические методы.
| фронт элюэнта |
| Q |
| L |
| x2 |
| x1 |
| линия старта |
| Рис. 24.3. Примерный вид плоско стной хроматограммы |
Некоторые из реагентов, используемых для проявления хроматограмм, показаны в табл. 24.2.
Табл. 24.2.
Некоторые реагенты-проявители, используемые в плоскостной хроматографии
|
Положение отдельных хроматографических зон на хромато- грамме характеризуют с помощью величины Rf, равной отношению расстояния, пройденного зоной вещества от стартовой линии до цен
тра зоны (x), к расстоянию от стартовой линии до границы фронта растворителя к концу опыта (L)
x
Rf =
L
Величина Rf может принимать значения от 0 до 1. Если Rf = 0, то вещество остаётся на старте, если Rf = 1, то оно поднимается с фронтом растворителя. Величина Rf является качественной хроматографи- ческой характеристикой вещества. Она зависит от природы вещества, подвижной и неподвижной фазы, условий хроматографирования и, в определённых пределах, не зависит от концентрации вещества.
Подвижность разделяемых веществ можно также сравнить с подвижностью вещества, принятого за стандарт

|
Величина Rf связана с коэффициентом распределения вещества (D) и коэффициентом емкости неподвижной фазы по отношению к данному веществу (k') следующими уравнениями:
| V D = m Vs | f 1 - ll V Rf J | k ' =1 - Rf Rf |
 Рис. 24.4. Расчёт эффективности разделения в плоскостной хроматографии
Рис. 24.4. Расчёт эффективности разделения в плоскостной хроматографии
|

Для того чтобы оценить эффективность разделения в плоскостной хроматографии, измеряют расстояние от стартовой линии до нижнего края пятна данного вещества (x') и расстояние от нижней до верхней границы этого пятна (w) - рис. 24.4. Число теоретических тарелок (N) и высоту эквивалентную теоретической тарелке (H) рассчитывают по формулам:
| L | |
| H = — | |
| N |
Коэффициент разделения (а) и разрешение (RS) в плоскостной хроматографии рассчитывают следующим образом:

|
24.2.3. Практическое применение
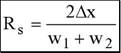
|
Плоскостная хроматография используется, главным образом, для обнаружения и идентификации веществ.
| г> ч. У о о | о • V / | ||
| окраска зоны вещества либо появление окраски при взаимодействии с реагентом-проявителем |

|
| использование других методов анализа / |
| 4 2 PPM |
| о |

|
| положение зоны вещества (величина Rf) |
| 4 Щ |
ОБНАРУЖЕНИЕ И ИДЕНТИФИКАЦИЯ ВЕЩЕСТВ

|
| использование стандартных веществ |

|
 lgC
lgC
|
С целью количественного определения веществ тонкослойную и бумажную хроматографию применяют значительно реже.
24.3. Колоночная жидкостная хроматография
В колоночной жидкостной хроматографии сорбент находится в стеклянной или металлической трубке (колонке).
В классическом варианте колоночной хроматографии используются сорбенты с диаметром частиц более 100 мкм. Колонка может иметь длину до нескольких метров. Элюент продвигается по колонке под действием силы тяжести.
В высокоэффективной жидкостной хроматографии (ВЭЖХ) используются сорбенты, обладающие особыми свойствами (однородность частиц, ненабухаемость и т.д.). Диаметр частиц этих сорбентов не превышает 50 мкм. Часто в ВЭЖХ применяют сорбенты с различными привитыми группами (см. рис. 24.1). Скорость движения подвижной фазы и эффективность разделения в ВЭЖХ значительно выше, чем в классическом варианте хроматографии.
24.3.1. Устройство жидкостного хроматографа
Основные узлы жидкостного хроматографа показаны на рис.
24.5.
ввод пробы
 Рис. 24.5. Принципиальная схема жидкостного хроматографа
Рис. 24.5. Принципиальная схема жидкостного хроматографа
|
Подвижная фаза подаётся в колонку с помощью насоса. Блок подачи элюента может включать в себя также систему дегазации, устройство для градиентного элюирования, измерители давления. До попадания в насос подвижная фаза должна быть профильтрована и освобождена от растворённых в ней газов ("дегазирована"), так как пузырьки газа при попадании в колонку приводят к снижению её эффективности, а при попадании в детектор вызывают беспорядочные колебания нулевой линии.
Ввод пробы в жидкостный хроматограф может проводиться с помощью петлевого дозатора, микрошприца (роль шприца может выполнять сам насос) и др.
Хроматографические колонки в ВЭЖХ, в отличие от газохрома- тографических колонок, прямые. Они имеют длину 10 - 30 см и внутренний диаметр 4 - 6 мм, а в микроколоночных хроматографах, соответственно, 5 - 7 см и 1-2 мм. Корпус колонки представляет собой цилиндрическую трубку, изготовленную из стекла, нержавеющей стали или полимерного материала. На верхнем и нижнем концах колонки расположены фильтры, представляющие собой диски из пористой нержавеющей стали. Назначение фильтров - удерживание сорбента в колонке и задержка механических примесей, которые могут находиться в подвижной фазе.
В табл. 24.3 перечислены детекторы, наиболее часто используемые в ВЭЖХ.
Табл. 24.3
Характеристика некоторых детекторов, используемых в жидкостных хроматографах
|
24.3.2. Практическое применение
Высокоэффективная жидкостная хроматография используется для разделения, в том числе и препаративного выделения, обнаружения и идентификации, а также количественного определения веществ различной химической природы (как полярных, так и неполярных, как ионов, так и молекул, как низкомолекулярных, так и высокомолекулярных).
В фармацевтическом анализе метод ВЭЖХ используется чаще, чем метод газовой хроматографии, поскольку многие лекарственные вещества представляют собой сложные органические соединения, имеющие высокие температуры кипения или разрушающиеся при нагревании. Основные области применения ВЭЖХ в фармацевтическом анализе:
• идентификация лекарственных веществ, присутствующих в лекарственных формах;
• определение примесей в лекарственных веществах (как в индивидуальных образцах, так и в лекарственных формах);
• количественное определение лекарственных веществ, входящих в состав лекарственных форм (особенно в случае лекарственных форм сложного состава или при малом содержании определяемого компонента);
• определение лекарственных веществ в биологических объектах.
24.4. Характеристика отдельных видов жидкостной хроматографии
Хроматографическое разделение в жидкостной хроматографии может быть обусловлено различными процессами: адсорбцией, распределением веществ между двумя несмешивающимися жидкими фазами, ионным обменом, распределением молекул в соответствии с их размерами и т.д
24.4.1. Ионообменная хроматография
В основе ионообменной хроматографии лежит процесс обмена ионов, связанных с неподвижной фазой, на ионы элюента, попадающие в колонку.
Дата добавления: 2015-09-07; просмотров: 274 | Нарушение авторских прав
| <== предыдущая страница | | | следующая страница ==> |
| Детекторы | | | Неподвижные и подвижные фазы |