
Читайте также:
|
| возбуждённое электронное состояние |
| основное электронное состояние |
Молекулярные абсорбционные спектры в УФ- и видимой области состоят не из отдельных чётко определённых линий, а из широких полос. Это вызвано следующими причинами. Как и атомы молекулы могут поглощать только такое электромагнитное излучение, энергия которого точно равна раз-
ности между энергиями основного
Рис. 20.9. Электронные переходы в J г
гипотетической молекуле и возбуждённого состояния. Одна
ко, полная энергия молекулы является суммой энергии электронного состояния (Еэл), энергии колебания атомов, входящих в её состав (Екол) и энергии вращения данной молекулы (Евр), причём Еэл > Екол >> Евр. Каждому электронному состоянию молекулы соответствует целая группа колебательных, а каждому колебательному, в свою очередь, большое число вращательных состояний. Энергия электромагнитного излучения УФ- и видимого диапазона соответствует энергии возбуждения валентных электронов. Для того чтобы произошёл переход молекулы из одного колебательного состояния в другое без изменения её электронного состояния, достаточно энергии ИК-излучения, а между двумя вращательными энергетическими уровнями в пределах одного и того же колебательного - энергии излучения микроволнового диапазона.
 200 250 300 350 400 450
Рис. 20.10. Спектр поглощения берберина бисульфата (водныйраствор) Основными характеристиками полосы поглощения являются её положение и интенсивность (рис. 20.11).
200 250 300 350 400 450
Рис. 20.10. Спектр поглощения берберина бисульфата (водныйраствор) Основными характеристиками полосы поглощения являются её положение и интенсивность (рис. 20.11).
|

|
| А,,нм |
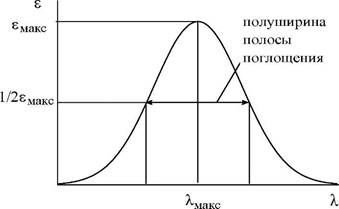 Рис. 20.11. Основные характеристики полосы поглощения
Рис. 20.11. Основные характеристики полосы поглощения
|
При поглощении электромагнитного излучения УФ- или видимого диапазона молекула переходит из некоторого колебательного и вращательного состояния основного электронного уровня в некоторое колебательное и вращательное состояние следующего электронного уровня (рис. 20.9). Каждый образец вещества содержит огромное число молекул. Даже если все они находятся в основном электронном состоянии, то при этом они могут находиться в разных колебательном и вращательном состояниях. Поэтому вещество будет поглощать не только электромагнитное излучение, соответствующее переходу между самыми низкими колебательными и вращательными состояниями основного и возбуждённого электронного уровней, но и излучение с близкими длинами волн. Кроме того, в многоатомных молекулах возможно много электронных переходов и они могут быть близки по энергии, поэтому в спектре поглощения отдельные полосы поглощения могут сливаться друг с другом. В качестве примера на рис. 20.10 приведен спектр поглощения алкалоида берберина.
Положение максимума полосы поглощения (Хмакс) соответствует длине волны такого электромагнитного излучения, энергия которого равна энергии необходимой для электронного перехода. Для характеристики ширины полосы поглощения используются величиной полуширины полосы поглощения. Интенсивность поглощения, которую можно охарактеризовать с помощью молярного коэффициента поглощения, зависит от вероятности данного электронного перехода. Поглощение с емакс > 104 считается интенсивным (максимально возмож-
5 3
ное значение s составляет примерно 2-10), поглощение с 8макс < 10 считается малоинтенсивным.
Объектами исследования в спектрофотометрии чаще всего являются органические вещества. Зависимость между строением органических соединений и их способностью поглощать электромагнитное излучение УФ- и видимого диапазона обычно изучается в курсе органической химии. Напомним лишь, что в органических соединениях могут происходить 4 типа электронных переходов: а ^ а*, n ^ а*, л ^ л* и n ^ л*. Энергия переходов первых двух типов соответствует энергии УФ-излучения вакуумного диапазона (например, а ^ а* в молекуле этана - 135 нм, n ^ а* в молекуле метанола - 183 нм). Энергия л ^ л* переходов изолированных л-связей соответствует ЭМИ с X < 200 нм, например в молекуле этилена - 165 нм. При сопряжении нескольких л-связей полосы поглощения смещаются в более длинноволновую область спектра.
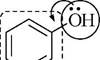
Группы, обуславливающие появление полос поглощения в молекулярных спектрах, называются хромофорами. Атомы или группы атомов, которые сами по себе не обуславливают появление полос поглощения, но влияют на характер поглощения хромофоров, называются ауксохромами.
|
| хромофор |
| ауксохром |
Ауксохромы имеют неподелённые электронные пары, находящиеся в сопряжении с л-электронной системой хромофора, и могут сдвигать полосу поглощения хромофора в более длинноволновую область (батохромный сдвиг) или в более коротковолновую область (гипсохромный сдвиг), увеличивать её интенсивность (гиперхром- ный эффект) или уменьшать её (гипохромный эффект).
Дата добавления: 2015-09-07; просмотров: 336 | Нарушение авторских прав
| <== предыдущая страница | | | следующая страница ==> |
| Практическое применение | | | Измерение аналитического сигнала |