
|
Читайте также: |
Железо является биологически активным элементом и в природе существенно влияет на интенсивность развития фитопланктона и качественный состав микрофлоры в водоемах.
Главные источники соединений железа в природной воде - продукты химического выветривания горных пород. Значительное количество его поступает с подземным стоком и со сточными водами предприятий металлургической, металлообрабатывающей, текстильной, лакокрасочной промышленности и с сельскохозяйственными стоками.
В поверхностных водах соединения железа находятся в растворенном, коллоидном и взвешенном состояниях. Соотношение форм железа зависит от химического состава вод, рН, температуры.
В растворенной форме железо существует в виде катионов  и
и  , гидроксокомплексов типа
, гидроксокомплексов типа  ,
,  ,
,  ,
, 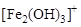 ,
,  и комплексов с другими неорганическими и органическими, главным образом гумусовыми, веществами.
и комплексов с другими неорганическими и органическими, главным образом гумусовыми, веществами.
Коллоидная форма железа представлена его гидроксидом и комплексами с органическими веществами, взвешенная форма - частицами железосодержащих минералов и соединениями железа, сорбированными на частицах взвесей.
До операции определения содержания железа в воде все его соединения либо предварительно окисляются до растворимых соединений железа (III), либо восстанавливаются до соединений железа (II).
Ион железа (III) с ионами роданида образует комплексные ионы кроваво-красного цвета, имеющие различную интенсивность окраски в зависимости от концентрации роданид-ионов:
 ,
,
где n - число роданид-ионов, связанных в железороданидном комплексе (может изменяться от 1 до 6).
Для фотометрирования в растворе необходимы строго определенные соотношения концентраций различных комплексных ионов, которые достигаются добавлением реактива в количестве, дающем возможность создать постоянную концентрацию роданида. В настоящей работе избыток роданид-ионов составляет 0,13 моль/л. Такому избытку роданида соответствует преимущественное образование комплексного иона 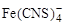 .
.
Со временем раствор бледнеет вследствие восстановления ионов железа ионами роданида, особенно в присутствии некоторых катализаторов, поэтому фотометрировать его необходимо сразу же после приготовления. Область максимального поглощения света окрашенным раствором - 400 - 450 нм.
Чувствительность метода составляет 2,5 мкг железа в 50 мл конечного объема анализируемого раствора при толщине фотометрического слоя 5 см.
Измерение оптической плотности эталонов и исследуемых растворов всегда осуществляют по отношению к нулевому раствору сравнения. В качестве нулевого раствора можно использовать чистую воду или раствор "холостого" опыта, содержащий все добавляемые компоненты, кроме реагента. Нулевой раствор приготавливают следующим образом: к небольшому количеству дистиллированной воды добавляют реагент и все компоненты, кроме определяемого, в тех же количествах, что и при приготовлении серии растворов определяемого вещества. Затем раствор разбавляют водой до требуемого объема и перемешивают. Результаты фотометрических измерений заносят в форму табл.5.
Дата добавления: 2015-10-26; просмотров: 285 | Нарушение авторских прав
| <== предыдущая страница | | | следующая страница ==> |
| Фотометрическое определение примесей тяжелых металлов в пресной воде | | | Внешний вид пленки нефти на поверхности воды в зависимости от ее толщины и количества нефти |