
|
Читайте также: |
Хром образует два ряда устойчивых солей: соли хрома (III) и соли хрома (VI). Соли хрома (III) в основном содержат его в виде катиона  , а соли хрома (VI) - в виде анионов
, а соли хрома (VI) - в виде анионов  и
и  . Растворы солей хрома (III) имеют сине-зеленую или фиолетовую окраску, хроматов (
. Растворы солей хрома (III) имеют сине-зеленую или фиолетовую окраску, хроматов ( ) - желтую, а бихроматов (
) - желтую, а бихроматов ( ) - оранжевую.
) - оранжевую.
а) Определение катиона Сr3+ щелочью.
Катион хрома (III) образует с сильными гидроксидами (щелочами) осадок  серо-зеленого цвета. При действии на осадок избытка щелочи хром переходит в раствор в виде хромит-иона зеленого цвета (цвета травы)
серо-зеленого цвета. При действии на осадок избытка щелочи хром переходит в раствор в виде хромит-иона зеленого цвета (цвета травы)
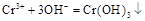 ;
;
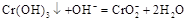 .
.
К 2 каплям раствора соли хрома (III) добавьте 1 каплю 2 н раствора гидроксида натрия  Наблюдайте образование серо-зеленого осадка гидроксида хрома. Затем к осадку добавьте избыток щелочи до его полного растворения. Отметьте цвет осадка и раствора. Напишите уравнения соответствующих реакций.
Наблюдайте образование серо-зеленого осадка гидроксида хрома. Затем к осадку добавьте избыток щелочи до его полного растворения. Отметьте цвет осадка и раствора. Напишите уравнения соответствующих реакций.
Б) Окисление хрома (III) до хрома (VI).
Катион хрома (III) легко окисляется пероксидом водорода в щелочной среде до  :
:
 .
.
К 2 - 3 каплям раствора соли хрома (III) добавьте несколько капель 2 н раствора гидроксида натрия до полного растворения образующегося вначале осадка гидроксида хрома, 2 - 3 капли 3%-ного раствора пероксида водорода и нагрейте несколько минут до изменения зеленой окраски раствора в желтую.
Проведите соответствующие реакции, отметьте исходный, промежуточный и конечный цвет раствора, напишите уравнения реакций.
В) Смещение равновесия между хромат- и бихромат-ионами.
Хром (VI) может присутствовать в растворе в виде хромат-ионов  желтого или бихромат-ионов
желтого или бихромат-ионов  оранжевого цвета. Между ними существует равновесие
оранжевого цвета. Между ними существует равновесие
 ,
,
которое в кислой среде смещается в сторону иона  , а в щелочной - иона
, а в щелочной - иона  .
.
К 2 - 3 каплям раствора, содержащего анион  , добавьте 2 - 3 капли 2 н раствора серной кислоты. Наблюдайте изменение желтой окраски в оранжевую:
, добавьте 2 - 3 капли 2 н раствора серной кислоты. Наблюдайте изменение желтой окраски в оранжевую:
 .
.
К 2 - 3 каплям раствора, содержащего анион  , добавьте 2 - 3 капли 2 н раствора гидроксида натрия. Наблюдайте изменение оранжевой окраски в желтую:
, добавьте 2 - 3 капли 2 н раствора гидроксида натрия. Наблюдайте изменение оранжевой окраски в желтую:
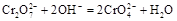 .
.
Дата добавления: 2015-10-26; просмотров: 125 | Нарушение авторских прав
| <== предыдущая страница | | | следующая страница ==> |
| Окрашенные ионы | | | Определение ионов тяжелых металлов |