
Читайте также:
|
КАТАЛИЗ – ПРОЦЕСС УСКОРЕНИЯ ХИМИЧЕСКОЙ РЕАКЦИИ ПОД ВЛИЯНИЕМ КАТАЛИ-ЗАТОРОВ, КОТОРЫЕ УЧАСТВУЮТ В ДАННОМ ПРОЦЕССЕ, НО К КОНЦУ РЕАКЦИИ ОСТАЮТСЯ ХИМИЧЕСКИ НЕИЗМЕННЫМИ.
КАТАЛИЗАТОРАМИ МОГУТ БЫТЬ: НЕОРГАНИЧЕСКИЕ И ОРГАНИЧЕСКИЕ ВЕЩЕСТВА.
НЕОРГАНИЧЕСКИЕ КАТАЛИЗАТОРЫ – ЭТО, КАК ПРАВИЛО, НИЗКОМОЛЕКУЛЯРНЫЕ ВЕЩЕСТВА, ОБЛАДАЮТ НИЗКОЙ СПЕЦИФИЧНОСТЬЮ, АКТИВНЫ:
1) ПРИ ВЫСОКОЙ ТЕМПЕРАТУРЕ (100◦С И ВЫШЕ),
2) ОПТИМУМ PН ДЛЯ НИХ – СИЛЬНОКИСЛАЯ ИЛИ СИЛЬНОЩЕЛОЧНАЯ СРЕДА;
3) ПРИ ДАВЛЕНИИ ВЫШЕ АТМОСФЕРНОГО;
4) УВЕЛИЧИВАЮТ СКОРОСТЬ ХИМИЧЕСКОЙ РЕАКЦИИ В 102-106 РАЗ.
ФЕРМЕНТЫ – ОРГАНИЧЕСКИЕ ВЕЩЕСТВА (БИОЛОГИЧЕСКИЕ КАТАЛИЗАТОРЫ) – ЭТО ВЫСОКОМОЛЕКУЛЯРНЫЕ ПОЛИМЕРЫ, КОТОРЫЕ:
- ОБЛАДАЮТ ВЫСОКОЙ СПЕЦИФИЧНОСТЬЮ
- ОПТИМУМ ТЕМПЕРАТУРЫ 35-450 С (370)
- АКТИВНЫ ПРИ ОПРЕДЕЛЕННЫХ ФИЗИОЛОГИЧЕСКИХ ДИАПАЗОНАХ PН СРЕДЫ
(ПЕПСИН – 1,5- 2,0; ТРИПСИН – 7,8 – 8,2)
- УВЕЛИЧИВАЮТ СКОРОСТЬ ХИМИЧЕСКОЙ РЕАКЦИИ В 108 – 1011 РАЗ.
1. ХАРАКТЕРИСТИКА ФЕРМЕНТАТИВНОГО КАТАЛИЗА.
МЕХАНИЗМ КАТАЛИТИЧЕСКОГО ДЕЙСТВИЯ ФЕРМЕНТОВ: ОДНА ИЗ НАИБОЛЕЕ ВАЖНЫХ ПРОБЛЕМ ЭНЗИМОЛОГИИ, ИЗУЧЕНИЕМ КОТОРОЙ ЗАНИМАЛИСЬ МИХАЭЛИС И МЕНТОН.
РАЗЛИЧАЮТ НЕСКОЛЬКО СТАДИЙ КАТАЛИЗА:
 I - ПРИСОЕДИНЕНИЕ S + E
I - ПРИСОЕДИНЕНИЕ S + E


 II - ОБРАЗОВАНИЕ SE- КОМПЛЕКСА E + S ES P + E,
II - ОБРАЗОВАНИЕ SE- КОМПЛЕКСА E + S ES P + E,
III - ОТРЫВ P И ОСВОБОЖДЕНИЕ E
ГДЕ Е – ФЕРМЕНТ, S – СУБСТРАТ, Р – ПРОДУКТ РЕАКЦИИ, ES – ФЕРМЕНТ-СУБСТРАТНЫЙ КОМПЛЕКС.
САМАЯ БЫСТРАЯ I СТАДИЯ;
МОЛЕКУЛЯРНАЯ МАССА ФЕРМЕНТА В 100-1000 РАЗ БОЛЬШЕ ЧЕМ МОЛЕКУЛЯРНАЯ МАССА S, ПОЭТОМУ МОЛЕКУЛА S ПРИ ФЕРМЕНТАТИВНОЙ РЕАКЦИИ СВЯЗЫВАЕТСЯ НЕ СО ВСЕМ ФЕРМЕНТОМ, А ТОЛЬКО С ЕГО ОПРЕДЕЛЕННЫМ УЧАСТКОМ, КОТОРЫЙ НАЗЫВАЕТСЯ АКТИВНЫМ ЦЕНТРОМ (ИЛИ КАТАЛИТИЧЕСКИМ УЧАСТКОМ), АЦ – ЭТО УНИКАЛЬНАЯ КОМБИНАЦИЯ АК ОСТАТКОВ В МОЛЕКУЛЕ ФЕРМЕНТА, КОТОРАЯ ОБЕСПЕЧИВАЕТ НЕПОСРЕДСТВЕННОЕ ВЗАИМОДЕЙСТВИЕ ФЕРМЕНТА С МОЛЕКУЛОЙ СУБСТРАТА И ПРИНИМАЕТ НЕПОСРЕДСТВЕННОЕ УЧАСТИЕ В АКТЕ КАТАЛИЗА. ИМЕННО АЦ ФЕРМЕНТА ОПРЕДЕЛЯЕТ ЕГО СПЕЦИФИЧНОСТЬ И КАТАЛИТИЧЕСКУЮ АКТИВНОСТЬ.
БИЛЕТ 7
6. СВОЙСТВА ФЕРМЕНТОВ: ОБРАТИМОСТЬ И СПЕЦИФИЧНОСТЬ.
А) СПЕЦИФИЧНОСТЬ ДЕЙСТВИЯ ФЕРМЕНТА – ЭТО СПОСОБНОСТЬ ФЕРМЕНТА КАТАЛИЗИРОВАТЬ ОПРЕДЕЛЕННЫЕ ХИМИЧЕСКИЕ РЕАКЦИИ.
АБСОЛЮТНАЯ – КОГДА ФЕРМЕНТ КАТАЛИЗИРУЕТ ТОЛЬКО ОДНУ РЕАКЦИЮ (Н-Р УРЕАЗА-РАСЩЕПЛЕНИЕ МОЧЕВИНЫ, УРИКАЗА – РАСЩЕПЛЕНИЕ МОЧЕВОЙ КИСЛОТЫ)
ОТНОСИТЕЛЬНАЯ – КОГДА ФЕРМЕНТ КАТАЛИЗИРУЕТ НЕСКОЛЬКО РОДСТВЕННЫХ РЕАКЦИЙ (ДЕЙСТВУЕТ НА СЛОЖНЫЕ ХИМИЧЕСКИЕ СОЕДИНЕНИЯ, ИМЕЮЩИЕ ХОТЯ БЫ ОДНУ СТРОГО ОПРЕДЕЛЕННУЮ ХИМИЧЕСКУЮ ГРУППУ: ЭСТЕРАЗЫ, ФОСФОТАЗЫ И Т.Д.)
Б) ОБРАТИМОСТЬ ДЕЙСТВИЯ ФЕРМЕНТА, Т.Е. СПОСОБНОСТЬ ФЕРМЕНТА КАТАЛИЗИРОВАТЬ КАК ПРЯМУЮ, ТАК И ОБРАТНУЮ РЕАКЦИЮ (Т.Е. РЕАКЦИЮ СИНТЕЗА И РАСПАДА)
ЛДГ – ОБРАЗОВАНИЕ И ОКИСЛЕНИЕ МК.
7.КИНЕТИКА ФЕРМЕНТАТИВНОЙ РЕАКЦИИ.
ФАКТОРЫ, ВЛИЯЮЩИЕ НА СКОРОСТЬ ФЕРМЕНТАТИВНОЙ РЕАКЦИИ:
ТЕМПЕРАТУРА, PН, КОНЦЕНТРАЦИЯ Е И S, НАЛИЧИЕ АКТИВАТОРОВ И ИНГИБИТОРОВ.
1.  ФЕРМЕНТЫ ТЕРМОЛАБИЛЬНЫ
ФЕРМЕНТЫ ТЕРМОЛАБИЛЬНЫ
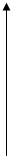



 ПРИ T +800 С ФЕРМЕНТЫ РАЗРУШАЮТСЯ
ПРИ T +800 С ФЕРМЕНТЫ РАЗРУШАЮТСЯ

 ПРИ T НИЖЕ 00С- ТЕРЯЮТ АКТИВНОСТЬ, НО НЕ
ПРИ T НИЖЕ 00С- ТЕРЯЮТ АКТИВНОСТЬ, НО НЕ


 РАЗРУШАЮТСЯ
РАЗРУШАЮТСЯ
ПРИ T 35-450 С ПРОЯВЛЯЮТ MAX АКТИВНОСТЬ



 (Т.Е. ЭТО T ОПТИМУМ ДЛЯ ФЕРМЕНТА)
(Т.Е. ЭТО T ОПТИМУМ ДЛЯ ФЕРМЕНТА)
 | |
 |






 T (0С)
T (0С)

10 20 30 40 50 60 70
2. АКТИВНОСТЬ ФЕРМЕНТА ЗАВИСИТ ОТ PH СРЕДЫ:
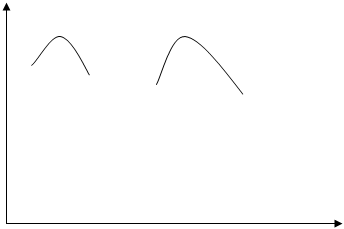
ОПТИМУМ РН ДЛЯ ПЕПСИНА 1.0-2,5 (А)
ДЛЯ АМИЛАЗЫ 6,8- 7,2 (Б)
А) Б)
1 2 3 4 5 6 7 8 9 10 РН
3.КОНЦЕНТРАЦИЯ S И Е.
СКОРОСТЬ ФЕРМЕНТАТИВНОЙ РЕАКЦИИ ПРЯМО ПРОПОРЦИОНАЛЬНА КОНЦЕНТРАЦИИ S И Е., ОДНАКО СЛИШКОМ ВЫСОКАЯ КОНЦЕНТРАЦИЯ S МОЖЕТ ИНГИБИРОВАТЬ СКОРОСТЬ ФЕРМЕНТАТИВНОЙ РЕАКЦИИ.
КОНСТАНТА МИХАЭЛИСА (КМ) БЫЛА ВЫВЕДЕНА МИХАЭЛИСОМ И МЕНТЕНОМ В 1913ГОДУ.
КМ = КОНЦЕНТРАЦИИ S(ММОЛЬ), ПРИ КОТОРОЙ V ФЕРМЕНТАТИВНОЙ РЕАКЦИИ = ½ V MAX
ЗНАЯ КМ МОЖНО РАССЧИТАТЬ ОПТИМАЛЬНУЮ КОНЦЕНТРАЦИЮ S ДЛЯ ПРОВЕДЕНИЯ ДАННОЙ ФЕРМЕНТАТИВНОЙ РЕАКЦИИ.
4. АКТИВАТОРЫ И ИНГИБИТОРЫ.
АКТИВАТОРЫ – ВЕЩЕСТВА, КОТОРЫЕ ПОВЫШАЮТ АКТИВНОСТЬ Е
НАПРИМЕР: ИОНЫ CL ДЛЯ L-АМИЛАЗЫ, ПЕПСИНА; ЖЕЛЧНЫЕ КИСЛОТЫ ДЛЯ ЛИПАЗЫ;
АКТИВНЫЙ ПЕПСИН ДЛЯ ПЕПСИНОГЕНА.
ИНГИБИТОРЫ – ВЕЩЕСТВА, КОТОРЫЕ СНИЖАЮТ АКТИВНОСТЬ Е.
ИНГИБИРОВАНИЕ М. Б. КОНКУРЕНТНЫМ И НЕКОНКУРЕНТНЫМ (ИЛИ РЕТРОГРАДНЫМ)
КОНКУРЕНТНОЕ ИНГИБИРОВАНИЕ ВОЗМОЖНО, ЕСЛИ S И I ОДИНАКОВЫЕ ПО СТРОЕНИЮ, Т.Е. МЕЖДУ НИМИ ИДЕТ КОНКУРЕНЦИЯ ЗА ВЗАИМОДЕЙСТВИЕ С АЦ ФЕРМЕНТА. ЕСЛИ БОЛЬШЕ S, ТО ОБРАЗУЕТСЯ SE- КОМПЛЕКС, А ЕСЛИ БОЛЬШЕ I,ТО IЕ-КОМПЛЕКС.
ИНГИБИТОРАМИ М.Б. ВЕЩЕСТВА, КОТОРЫЕ СВЯЗЫВАЮТ АЦ ФЕРМЕНТА: СОЛИ ТЯЖЕЛЫХ МЕТАЛОВ В MIN КОНЦЕНТРАЦИЯХ СВЯЗЫВАЮТ- SH ГРУППЫ ФЕРМЕНТА, А ЗНАЧИТ ТОРМОЗЯТ АКТИВНОСТЬ Е (МОНОЙОДУКСУСНАЯ КИСЛОТА), СИНИЛЬНАЯ КИСЛОТА И ЕЁ СОЛИ СВЯЗЫВАЮТ FE В ГЕМСОДЕРЖАЩИХ Е И ДР.
ИНГИБИТОРАМИ МОГУТ БЫТЬ АНТИФЕРМЕНТЫ: Н-Р АКТИВНОСТЬ ТРИПСИНА ТОРМОЗЯТ L1- АНТИТРИПСИН (ИЛИ АНТИПРОТЕАЗНЫЙ I);
АНТИФЕРМЕНТЫ СВЯЗЫВАЮТ Е ВРЕМЕННО, А ПРИ ОПРЕДЕЛЕННЫХ УСЛОВИЯХ ЛЕГКО ОТДЕЛЯЮТСЯ ОТ Е, И АКТИВНОСТЬ ЕГО ВОССТАНАВЛИВАЕТСЯ.
РЕТРОГРАДНОЕ ИНГИБИРОВАНИЕ – ЭТО ИНГИБИРОВАНИЕ АКТИВНОСТИ Е ПРОДУКТОМ РЕАКЦИИ (Р), ТОЧНЕЕ ОПРЕДЕЛЕННОЙ ЕГО КОНЦЕНТРАЦИЕЙ, КОТОРЫЕ (Р) ЛИБО ИЗМЕНЯЮТ РН СРЕДЫ (КАК ДЛЯ ПЕПСИНА АК), ЛИБО САМИ ЯВЛЯЮТСЯ I ДЛЯ Е.
Дата добавления: 2015-08-17; просмотров: 96 | Нарушение авторских прав
| <== предыдущая страница | | | следующая страница ==> |
| ГЕМОФИЛИЯ А, РАЗВИВАЕТСЯ ПРИ ДЕФИЦИТЕ VIII ПЛАЗМЕННОГО ФАКТОРА, ВСТРЕЧАЕТСЯ У 80-85 % ВСЕХ СЛУЧАЕВ ЗАБОЛЕВАНИЯ. | | | ПАТОЛОГИЯ ЛИПИДНОГО ОБМЕНА. |