
|
Читайте также: |
Основные природные запасы водорода на Земле – это вода и вся органическая материя. В частности, живущие растения и они же уже умершие (древесина, торф, уголь), а также нефть, природный газ и т.п.
Во всех этих веществах водород имеет наиболее устойчивую для него степень окисления +1. Поэтому получают 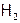 восстановлением, и чаще из воды.
восстановлением, и чаще из воды.
В лаборатории можно вытеснить водород из Н2О, например, с помощью ЩМ. Но обычно используют более безопасный (хотя тоже дорогой способ) – взаимодействие цинка с разбавленными растворами кислот:
 ,
,
При этом 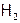 образуется на поверхности цинка в виде пузырьков, которые отрываются и всплывают, создавая видимость кипения. Накапливающуюся в растворе соль, содержащую ионы цинка, можно обнаружить, выпарив каплю этого раствора и рассмотрев образовавшиеся кристаллы под микроскопом.
образуется на поверхности цинка в виде пузырьков, которые отрываются и всплывают, создавая видимость кипения. Накапливающуюся в растворе соль, содержащую ионы цинка, можно обнаружить, выпарив каплю этого раствора и рассмотрев образовавшиеся кристаллы под микроскопом.
В промышленности используют более дешевые методы получения 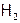 , в частности, электролиз воды (для хорошей проводимости к ней добавляют, например, серную кислоту.); дорогой способ – восстанавление раскаленным углем:
, в частности, электролиз воды (для хорошей проводимости к ней добавляют, например, серную кислоту.); дорогой способ – восстанавление раскаленным углем:
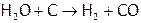 .
.
Однако ученые ищут и разрабатывают еще более дешевые методы синтеза 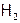 . Например, такие, как фотолиз (разложение воды в присутствии катализатора под действием солнечных лучей). Кроме того, пытаются генетически изменять растения, в частности, водоросли, чтобы усилить выделение ими
. Например, такие, как фотолиз (разложение воды в присутствии катализатора под действием солнечных лучей). Кроме того, пытаются генетически изменять растения, в частности, водоросли, чтобы усилить выделение ими 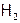 при дыхании.
при дыхании.
Эти задачи являются злободневными, т.к. водород не только незаменимый реагент во многих технологиях, но и из всех энергоносителей максимально отвечает требованиям, предъявляемым к современному топливу.
Рассмотрим эти требования, а также то, насколько водород им отвечает.
1). Большие запасы. Запасы водорода на Земле в виде воды практически неисчерпаемы, т.к. при сжигании 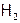 они возобновляются.
они возобновляются.
2) Высокая энергоемкость. При сгорании 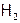 выделяется 242 кДж/моль. А моль
выделяется 242 кДж/моль. А моль 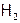 – это всего 2 г топлива. Поэтому в расчете на 1 г получается в 4 раза больше энергии, чем при сжигании каменного угля.
– это всего 2 г топлива. Поэтому в расчете на 1 г получается в 4 раза больше энергии, чем при сжигании каменного угля.
3) Безопасность и компактность хранения. И то, и другое обеспечивается, если хранить 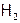 в виде твердого раствора в специальных сплавах (например, полученных на основе титана и железа). К тому же, при небольшом нагревании водород выделяется из сплава, причем частично в виде атомов Н. При сгорании такого атомарного водорода получается значительно больше тепла, чем при сжигании молекулярного (
в виде твердого раствора в специальных сплавах (например, полученных на основе титана и железа). К тому же, при небольшом нагревании водород выделяется из сплава, причем частично в виде атомов Н. При сгорании такого атомарного водорода получается значительно больше тепла, чем при сжигании молекулярного (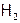 ), т.к. не затрачивается энергия на разрыв очень прочной связи Н–Н.
), т.к. не затрачивается энергия на разрыв очень прочной связи Н–Н.
4) Экологическая чистота (это главное требование). Испытания автомобилей на водородном топливе показали, что их выхлопные газы чище, чем засасываемый воздух. В таких странах, как США, Германия, Швейцария, Италия и др., уже используют водород в быту вместо природного газа.
Таким образом, по мнению ученых, мы находимся на пороге водородной энергетики (мировое производство 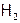 уже составляет несколько миллионов тонн в год, но требуется несопоставимо больше).
уже составляет несколько миллионов тонн в год, но требуется несопоставимо больше).
В заключение (чтобы еще раз подчеркнуть роль H как в химии, так и в биологии) укажем, что молекулы голубого пигмента василька и красного пигмента мака различаются по составу лишь одним атомом водорода.
Дата добавления: 2015-07-25; просмотров: 65 | Нарушение авторских прав
| <== предыдущая страница | | | следующая страница ==> |
| Особенности водорода | | | Общая характеристика. Нахождение в природе |