
Читайте также:
|
При нанесенні покриттів хімічним способом пред'являють підвищені вимоги до підготовки поверхні покриваються деталей. Поверхня деталей перед хімічним нанесенням покриття готують тими ж способами, що і при нанесенні гальванічних покриттів. Деталі знежирюють в органічних розчинниках і лужних розчинах; травлення здійснюють у кислотах у присутності інгібіторів корозії так само, як і активація. Склади розчинів для хімічного нікелювання наведені у ГОСТ 9 047-75. Однак у виробничих умовах застосовують більш широкий асортимент складів [31, 38, 39].
Основні показники ефективності розчинів - швидкість утворення покриттів при тій чи іншій щільності завантаження; маса покриття, отриманого з 1 л розчину (тобто вихід металу), стабільність, залежність цих величин від різних факторів (кислотності, температури і т. д.).
Кислі розчини (рН 4,0-6,5) застосовують при нанесенні покриттів на деталі з чорних і деяких кольорових металів (мідь, латунь тощо), особливо коли їх робочі поверхні повинні мати високі твердість, зносостійкість і корозійно-захисні властивості.
З плином часу швидкість нікелювання в некорректіруемих кислих розчинах поступово зменшується і через 6 год роботи процес утворення покриттів майже припиняється. При цьому кислотність розчинів зростає, вони каламутніють, на дно ванни випадає нерозчинний осад. Перегрів розчинів і зміна оптимальної концентрації компонентів призводять до саморазряду і освіти нікелю в обсязі ванни. Практично встановлено, що розчини з янтарнокіслим натрієм дозволяють отримувати за той же час більш товстий шар покриття ніж розчини з оцтово-або лимоннокислого натрію. Крім того, чим більша щільність завантаження ванни, тим менше швидкість осадження покриття за рівний проміжок часу.
Необхідно мати на увазі, що підтримка в ході реакції оптимальної величини рН, наприклад, гідроксилом натрію, мало підвищує швидкість осадження хімічного нікелю, що пояснюється порушенням оптимальної концентрації його основних компонентів, а також накопиченням в розчині побічних продуктів реакції.
Періодичне коригування кислих розчинів гіпофосфіти сприяє збільшенню виходу нікелю на 6-12%. Одночасне коригування кислих розчинів солями нікелю та гіпофосфіти не дає істотного підвищення виходу нікелю в порівнянні з коригуванням одним гіпофосфіти.
Рис. 7 Залежність швидкості осадження покриття від тривалості нікелювання в кислому розчині. 1 - з 15 мг / л сульфіду свинцю і коригуванням; 2 - те ж, без коригування; 3 - з 15 мг / л аллілчепа і коригуванням; 4 - те саме, без коригування.
На рис. 6 показано залежність швидкості осадження покриття від тривалості нікелювання в кислому некорректіруемом і коригуються розчинах з сульфідом свинцю як стабілізатор. Для цих цілей застосовують розчин наступного складу (г / л), хлористий нікель 21, гіпофосфіт натрію 24, уксуснокислий натрій 10, рН 5,2, температура 97-98 ° С, щільність завантаження 1 дм 2 / л. В обох випадках початкова швидкість нікелювання в свіжоприготовлених розчинах становить близько 60 мкм / год, однак некорректіруемий розчин вже після 1 год роботи майже повністю виробився і осадження нікелю в ньому припинилося. У коректованим розчині, коли концентрація компонентів і рН підтримувалися на оптимальному рівні, така швидкість нікелювання зберігається тривалий час. При використанні у тому ж розчині як стабілізатор 15 м / л аллілчепа (замість сульфіду свинцю) швидкість нікелювання знижується на 20-22% в порівнянні з першим випадком, проте і тоді за допомогою коригування можна використовувати розчин тривалий час. Застосування в кислих розчинах зазначених стабілізаторів дозволяє вести процес при максимальній температурі і на найбільшій швидкості. При цьому можливо багаторазове коригування розчинів, що є надзвичайно важливим чинником у виробничій практиці так само, як зростання виходу металу з кислих розчинів до 50% [31, 33, 34].
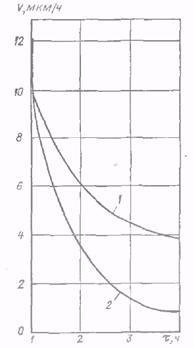
На рис. 7 показано залежність швидкості осадження покриття від тривалості нікелювання в розчині з малеїновим ангідридом і без нього. З малюнка видно, що в розчині наступного складу (г / л), сірчанокислий нікель 21, гіпофосфіт натрію 24, уксуснокислий натрій 10, рН 5.0-5,2 і температура 82-84 ° С. при щільності завантаження 1 дм 2 / л, що містить 1.5-2 г / л малеїнового ангідриду, швидкість покриття на четвертій годині роботи ванни майже в чотири рази вище, ніж без цього стабілізатора.
 .
.
Рис. 8. Залежність швидкості осадження покриття від тривалості нікелювання у водному розчині. 1 - з малеїновим ангідридом (1,5-2,0 г / л), 2 - без малеїнового ангідриду.
Дата добавления: 2015-07-11; просмотров: 120 | Нарушение авторских прав
| <== предыдущая страница | | | следующая страница ==> |
| Структура і фізико-хімічні властивості Ni - Р-покриттів | | | Хімічне нікелювання металів |