
Читайте также:
|
Розв’язок.
Слід згадати, що епімерами називають діастереомери, що розрізняються конфігурацією тільки одного вуглецевого атому.
Отже, щоб написати всі проекційні формули епімерів Д-глюкози, необхідно послідовно змінювати на протилежну - конфігурацію у кожного з асиметричних атомів вуглецю, відповідно одержимо чотири епімери для Д-глюкози:

4. Як, використовуючи різницю у властивостях, ідентифікувати D-глюкозу і метил-D-глюкозид?
Розв’язок:
а) Перш за все слід згадати, що моносахариди можуть існувати як у відкритій ланцюговій, так й у циклічній формі. Остання утворюється за рахунок взаємодії альдегідної (або кетонної) групи з гідроксильною групою атомів вуглецю С-4 або С-5, що й призводить до утворення циклічного напівацеталю (при взаємодії з С-4 утворюється п’ятичленний цикл, що називається фуранозним, а з С-5 – шестичленний, що називається піранозним). Напівацетальна група, що утворюється, називається глікозидною. В обох випадках утворюється додатковий асиметричний центр (С-1), що призводить до появи ще двох стереоізомерів – α- та β-аномерів.

Циклічна форма вільно переходить у розчині у відкриту, яка зберігає відновні властивості моносахаридів.
Похідні циклічної форми, що утворюються при взаємодії глікозидної ОН-групи з гідроксилвмісними сполуками (спиртами, фенолами і т.п.) називаються глюкозидами. Наприклад, в результаті взаємодії з метиловим спиртом в умовах кислотного каталізу утворюються метилглюкозиди. Для глюкозид ів перехід у відкриту форму з вільною альдегідною групою стає неможливим, отже, вони втрачають відновні властивості.
Отже, головною відмінністю глюкозидів від моносахаридів є відсутність відновних властивостей.
Розв’язуючи запропоновану задачу, необхідно написати реакції, що доводять відновні властивості D-глюкози:

D-метилглюкозид не відновлює ці сполуки, оскільки не має вільної альдегідної групи.
5. Як повинен бути побудований вiдновлюючий олiгосахарид, що складається з двох молекул a-D-глюкози?
Розв’язок:
Дисахарид буде відновлюючим, якщо у своєму складі він має хоча б одну вільну напівацетальну групу. Тільки у такому випадку він зберігатиме здатність до розкриття циклу та буде реагувати з реактивами Фелінга і Толенса за рахунок наявної карбонільної групи.

Отже, розв’язок задачі можна записати у такому вигляді:

Задачі для самостійного розв’язку:
1. Напишіть схему окислення Д(+)ксилози до моно- та дикарбонових кислот. Чи будуть ці кислоти оптично активними?
2. На глюкозу подійте: а) аміачним розчином оксиду срібла, б) гідроксиламіном, в) оцтовим ангідридом, г) метиловим спиртом (НСl).
3. Скільки ізомерних спиртів утворюється при відновленні ізомерних альдотетроз? Чи всі вони будуть оптично активними?
4. Напишiть проекцiйнi формули моноз, епiмерних D-галактозi.
5. Зообразiть будову a- i b-метил-Д-глюкозидiв у виглядi пiранозних та фуранозних формул.
Аміни, амінокислоти, білки.
1. Синтезуйте N-пропіланілін, виходячи із бензену та подійте на нього: а) оцтовим ангідридом, б) ізобутилхлоридом, в) нітритом натрію в присутності хлороводневої кислоти, г) розведеною нітратною кислотою.
Розв’язок:
Спочатку треба згадати методи одержання ароматичних амінів. Анілін можна одержати, наприклад, виходячи із похідних бензену – хлоробензену або нітробензену. Таким чином, спочатку із бензену синтезуємо хлоробензен:
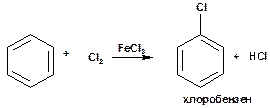
Діючи на хлоробензен аміаком в присутності каталізатора, при певній температурі і тиску одержуємо анілін:

N-пропіланілін – це змішаний вторинний амін, який легко синтезувати із аніліну за наступною реакцією:

Далі необхідно звернутися до хімічних властивостей ароматичних амінів. При дії на первинні і вторинні ариламіни галогенангідридів або ангідридів карбонових кислот (реакція ацилювання) атоми водню при азоті аміногрупи заміщуються на ацильний залишок і утворюються заміщені аміди карбонових кислот.

Наступне завдання – дія ізобутилхлоридом – реакція алкілування, за якою одержується третинний змішаний амін.

При дії нітриту натрію в присутності хлороводневої кислоти на вторинні ариламіни утворюються N-нітрозоаміни:
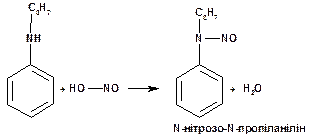
Ариламіни є слабкими основами, тому вони утворюють солі тільки із сильними мінеральними кислотами, наприклад, розведеною нітратною кислотою:

Якщо діяти концентрованою нітратною кислотою, ариламіни легко окиснюються, тому їх пряме нітрування здійснити неможливо.
2. Напишіть схему одержання a-аміноізомасляної кислоти, виходячи з ізопропілового спирту. В якому вигляді дана сполука буде знаходитись в нейтральному, лужному та кислому середовищах?
Розв’язок:
Зрозуміло, що синтезувати a-аміноізомасляну кислоту з ізопропілового спирту в одну стадію неможливо, необхідний цілий ряд перетворень за наступною схемою:

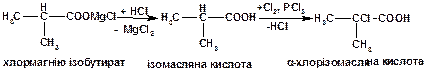

У нейтральному середовищі ця амінокислота існує у вигляді внутрішньої солі (біполярного іону): 
У лужному та кислому середовищах амінокислота буде існувати у вигляді солей:

3. Синтезуйте гліцилаланін.
Розв’язок:
Оскільки гліцилаланін – це дипептид, який складається із залишків амінокислот гліцину та аланіну, необхідно згадати пептидний синтез. В основі синтезу пептидів лежить процес утворення пептичного (амідного) зв’язку між карбоксильною групою однієї a-амінокислоти та аміногрупою – іншої. В процесі синтезу виникають складнощі, пов’язані з необхідністю сполучати залишки амінокислот у певній послідовності. Наприклад, при взаємодії гліцину і аланіну можливе утворення чотирьох дипептидів: гліцилалініну, аланілгліцину, гліцилгпіцину і аланілаланіну. Тому для проведення цілеспрямованого синтезу слід створити такі умови, за яких одна з амінокислот взаємодіяла б карбоксильною групою, а інша – аміногрупою. З цією метою здійснюють захист функціональних груп, які не беруть участі в утворенні пептидного зв’язку.
1. Для захисту аміногруп використовують реакцію ацилювання, наприклад оцтовим ангідридом:

2. Щоб захистити карбоксильну групу аланіну, проводять реакцію естерифікації:

3. Утворення пептидного зв’язку та зняття захисту:

4. Запропонуйте декілька методів синтезу дипропіламіну. Для нього напишіть рівняння реакцій з: а) HCl, б) HNO2, в)СН3СОСl.
Розв’язок:
Синтезувати алкіламіни можна наступними методами: а) реакцією Гофмана, б) синтезом Габріеля, в) перегрупуванням Гофмана.
а) Діючи аміаком на пропілбромід, можна одержати пропіламін. Якщо він провзаємодіє ще з однією молекулою пропілброміду – продуктом є дипропіламін:

б) Цей метод заснований на взаємодії фталіміду калію і галогеналканів з наступним гідролізом утвореного N-алкілфталіміду:

Із одержаного пропіламіну синтезують дипропіламін за реакцією, наведеною в попередньому методі.
в) При обробці незаміщених амідів карбонових кислот гіпобромідом натрію (або сумішшю брому і лугу) утворюються первинні аміни, в яких на один атом вуглецю менше, ніж у вихідному аміді:
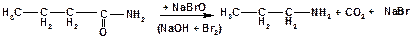
Із одержаного пропіламіну синтезують дипропіламін за реакцією, наведеною в методі а).
Для синтезованого дипропіламіну далі поставлене завдання написати рівняння наступних реакцій:
а) з хлоридною кислотою дипропіламін утворює сіль - хлорид дипропіламонію:

б) взаємодія з азотистою кислотою є для амінів якісною реакцією, яка відрізняє первинні, вторинні і третинні аміни. Оскільки дипропіламін є вторинним аміном, він в реакції з азотистою кислотою утворює N-нітрозоаміни:

в) з хлорангідридом оцтової кислоти відбувається реакція ацилювання і утворюється амід:

5. Напишіть схему перетворень 1,4-дибромобутану в 1,6-гександіамін.
Розв’язок:
Щоб одержати з 1,4-дибромобутану 1,6-гександіамін, необхідно подовжити вуглецевий ланцюг, тобто збільшити його на два атоми вуглецю. Це можна зробити за допомогою реакції між галогеналканом і натрієвою сіллю ціановодневої кислоти:

При відновленні бутилен динітрилу воднем в присутності нікелю або платини утворюється первинний амін - 1,6-гександіамін:

Задачі для самостійного розв’язку:
1. Синтезуйте кількома методами ізопропіламін і подійте на нього а) Н2SO4, б) HNO2, в) СН3СН2СОСl.
2. Напишіть рівняння реакцій, за якими утворюється дипептид: аланіллейцин.
3. Синтезуйте ізомерні хлораніліни.
4. Виходячи з етилену, синтезуйте етиламін, пропіламін, 1,2-діаміноетан, 1,4-діамінобутан.
5. Синтезуйте 4-амінобутанову кислоту. Для одержаної кислоти напишіть схеми реакцій з: а) t, °C, б) С2Н5ОН, в) Mg(OH)2, г) (СН3СО)2О.
Гетероциклічні сполуки.
1. Синтезуйте з фурану пірол, з піролу – тіофен. На останню сполуку подійте: а). H2SO4, б). HNO3, в). хлорангідридом кислоти у присутності SnCl2, г). Н2 у присутності Pd.
Розв’язок:
Переходи між фураном, тіофеном та піролом можна здійснити за допомогою реакції Юр’єва, яку проводять при температурі 400 оС у присутності каталізатора Al2O3:

Тіофен в реакціях електрофільного заміщення, на відміну від фурану та особливо піролу, є найбільш стійким щодо впливу мінеральних кислот, його можна беспосередьо сульфувати та нітрувати відповідними кислотами. При цьому заміщення відбувається в 2(a) – положення:


Ацилювання хлорангідридами кислот у присутності кислот Льюїса (наприклад, SnCl2) призводить до утворення a-тієніл кетонів:
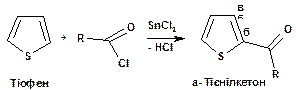
Відновлення тіофена у присутності паладієвого каталізатора призводить до тетрагідротіофена:

2. Визначити, які з наведених нижче структурних формул належать ароматичним сполукам:

Розв’язок:
Перш за все слід згадати умови прояву ароматичності в органічних сполуках. Сполука набуває ароматичних властивостей, якщо вона має плоский замкнений цикл та супряжену p-електронну систему, що охоплює всі атоми циклу та містить (4n+2) p-електронів (правило Хюккеля).
Виходячи з цього правила, можна зробити наступні висновки:
1. Дігідропірол та піпіридин не будуть мати властивостей ароматичних сполук (в циклі немає супряженої p-електронної системи).

2. Фуран, тіофен, пірол та піридин мають у супряженні 3 пари p-електронів, тобто, загальна кількість – 6 електронів, що відповідає n=1. Піридин відрізняється тим, що вільна електронна пара (позначена в структурних формулах як **) на гетероатомі N не бере участі в утворенні загальної p-електронної системи цикла.
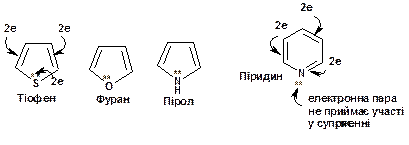
3. Нафталін та індол є прикладами ароматичних сполук, в яких p-електронна система цикла містить 5 електронних пар (10 електронів, n=2).
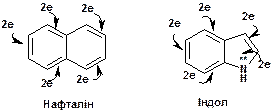
3. Пояснити причини амфотерних властивостей імідазола. Навести відповідні реакції.
Розв’язок:

Імідазол є прикладом гетероцикла з двома атомами Нітрогену, які знаходяться у положеннях 1 та 3 кільця. Ці атоми є відповідальними за амфотерний характер властивостей імідазола. Атом N у положенні 1 віддає свою неподілену електронну пару на утворення ароматичного секстету, тому він повністю втрачає свої основні властивості (так званий “атом пірольного типу”), отже, NH група відповідає за слабокислі властивості.
Натомість, атом N у положенні 3 зберігає електронну пору вільною, що надає імідазолу слабкі основні властивості.
Таким чином, імідазол є амфотерною сполукою, він утворює солі із сильними кислотами та з лужними металами:

4. З аденіна синтезувати гіпоксантін (6-гідроксипурин). Для останнього навести можливі форми існування.
Розв’язок:
Під дією нітритної кислоти на аденін відбувається його дезамінування з утворенням гіпоксантіна:

Гіпоксантін існує у кількох формах, наявність яких пов’язана з лактім-лактамною таутомерією та з мігріцією атома Н між положеннями 7 та 9:
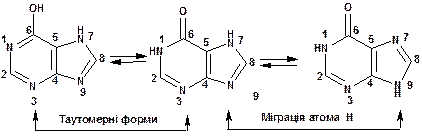
5. Порівняти умови проведення нітрування фурану та тіофену, поснити причини утворення 2-похідних в реакціях електрофільного заміщення цих сполук.
Розв’язок:
Фуран та тіофен відносяться до p-надлишкових сполук, тобто, до сполук з підвищеною електронною густиною в кільці. Для них характерна більша активність в реакціях електрофільного заміщення у порівнянні з бензеном. При відборі реагентів для реакції електрофільного заміщення слід враховувати ацидофобність фурану, який може протонуватися мінеральною кислотою та полімеризуватися:

Тому фуран нітрують в м’яких умовах з використанням ацетилнітриту:

Тіофен є більш стійким щодо дії кислот, він “витримує” нітрування беспосередньо нітратною кислотою:
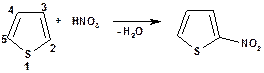
В реакціях електрофільного заміщення у фурані та тіофені (а також в піролі) найбільш реакційноздатним є 2 (a)-положення, що можна пояснити більшою делокалізацією заряда “+” у відповідному s-комплексі:

У випадку атакування b-положення можливостей для делокалізації заряду менше.

Задачі для самостійного розв’язку:
1. Порівняти активність в реакціях електрофільного заміщення бензен, піридин, пірол, фуран та тіофен. Навести відповідні реакції.
2. Порівняти основні властивості пірола та піридина, навести відповідні реакції.
3. Навести схеми лактім-лактамної таутомерії для урацилу (2,4-дігідроксипіримідину), тиміну (2,4-дігідрокси-5-метил-піримідину) та цитозину (4-аміно-2-гідроксипіримідину).
Література.
1. Грандберг И.И. Органическая химия. - М.,1987.
2. Ластухін Ю.О., Воронов С.А. Органічна хімія. – Л., 2000.
3. Нейланд О.Я. Органическая химия.- М.,1990.
4. Петров А.А., Бальян Х.В., Трощенко А.Т. Органическая химия. - М., 1981.
5. Усков И.А., Еременко Б.В., Нижник. В.В. Коллоидная химия. - К., 1989.
6. Черных В.П., Зименковский Б.С., Гриценко И.С. Органическая химия. – Х., 1995.
Дата добавления: 2015-10-24; просмотров: 808 | Нарушение авторских прав
| <== предыдущая страница | | | следующая страница ==> |
| Виходячи з ацетилену, синтезувати метилциклогексан. | | | Одержання метану і вивчення його властивостей |