
Спочатку необхідно синтезувати бензол за реакцією тримеризації ацетилену.

Далі реакцією електрофільного заміщення одержати гомолог бензолу – толуол.

Наступна реакція – каталітичне гідрування толуолу:

Задачі для самостійного розв’язку:
1. Із циклопропану синтезуйте відповідний алкен.
2. Із метилциклопентану синтезуйте бензол.
3. Як відбувається реакція галогенування для циклопропану та циклопентану? Порівняйте механізми цих реакцій.
Ароматичні вуглеводні.
1. Синтезуйте: а) бензен (бензол) з толуену (толуолу); б) толуол з бензолу. За допомогою яких якісних реакцій можна відрiзнити бензол i толуол?
Розв’язок:
Толуол з бензолу можна синтезувати в одну стадію за реакцією Фріделя-Крафтса (алкілування бензолу у присутності кислот Льюїса):

Присутність каталізатора – кислоти Льюїса – є обов’язковою, тому що з її допомогою генерується позитивно заряджена частинка електрофіл, що й атакує бензольне ядро:

Синтез бензолу з толуолу можна провести у дві стадії. Спочатку синтезують бензойну кислоту, при зтопленні якої з лугами відбувається її декарбоксилювання й утворюється бензол:


2. Напишiть реакцii нiтрування бензолу, толуолу, фенолу, нiтробензолу, хлоробензолу. Розмiстiть вихiднi продукти за легкiстю нiтрування. (При реакцiї нiтрування в молекулу вводять одну нiтрогрупу).
Розв’язок:
Реакція нітрування належить до реакцій електрофільного заміщення. Для її проведення найчастіше використовують нітруючу суміш, яка є сумішшю азотної та сірчаної (нітратної та сульфатної) кислот.
При нітруванні бензолу утворюється одне мононітропохідне:

Утворення електрофілу – катіона NO2+ можна показати так:
HNO3 + 2 H2SO4 Û NO2+ + H3O+ + 2HSO-4
Будова продуктів нітрування монопохідних бензолу буде залежати від природи замісника, який вже знаходиться у ядрі. Слід згадати, що вони поділяються на дві групи – замісники (орієнтанти) І та ІІ роду. Замісники І роду є електронодонорними, полегшують проходження реакції електрофільного заміщення (винятком є галогени!), спрямовують замісник, що входить, у о -, п -положення):

Кількість та співвідношення продуктів нітрування фенолу залежать від концентрації нітратної кислоти. У випадку надміру концентрованої кислоти буде утворюватися тринітропохідне:

За умовами задачі необхідно вводити одну нітрогрупу в бензольне ядро. Це можна зробити, якщо з фенолом буде реагувати розведена кислота при кімнатній температурі:

Щоб розмістити дані сполуки в ряд за легкістю нітрування, слід згадати вплив замісників І та ІІ роду на проходження реакцій електрофільного заміщення. Замісники ІІ роду є електроноакцепторними, дезактивують бензольне ядро у реакції електрофільного заміщення та спрямовують новий замісник у м -положення:
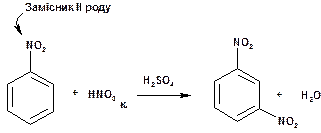
Усі замісники І роду, крім галогенів, активують бензольне ядро (підвищують електронну густину в о - та п -положеннях). За характером орієнтуючої дії вони поділяються на активуючі та дезактивуючі орієнтанти:
-O- > -NH2, -NR2 > -OH > -OR >-O-CO-R >-R (Alk) > C6H5 >
-F > -Cl > -Br > -I ( дезактивуючі)
· Усі замісники ІІ роду дезактивують бензольне кільце, утруднюючи реакцію електрофільного заміщення. За силою дезактивуючої дії їх розміщують у наступний ряд:
·
-N+R3> -NO2 >-CN>-SO3H>-CCl3 >-CO-Cl>-CO-H> -CO-R> - CO-OR >-CO-OH > -CO-NH2
Отже, за легкістю проходження реакції електрофільного заміщення вихідні сполуки можна розташувати у наступний ряд:

3. Напишіть реакції хлорування наступних сполук:

Розв’язок:
Необхідно згадати правила орієнтації для двозаміщених аренів:
· У разі наявності замісників І та ІІ роду місце вступу третього замісника визначатиме тільки замісник І роду. Отже, м-нітротолуол при хлоруванні утворює суміш трьох хлоропохідних, де атом хлору знаходиться у о - та п -положеннях відносно метильної групи (орієнтуюча дія нітрогрупи не враховується!):
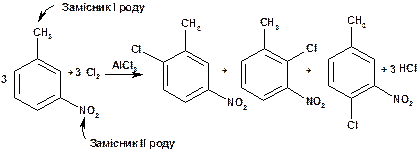
У випадку двох замісників І роду вступ третього замісника визначається тим із замісників, що є більш сильним орієнтантом (див. відповідний ряд у задачі 2).
Отже, у випадку о-хлоротолуолу атоми хлору входять у о - та п -положення щодо метильної групи:
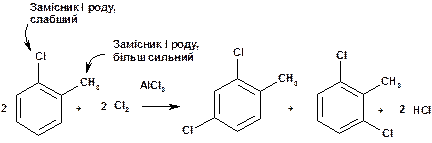
А у випадку п -крезолу місце входження третього замісника визначає ОН-група, яка є більш сильним орієнтантом І роду.

4. Встановiть будову ароматичного вуглеводню складу С8Н10, при окисненнi якого утворюсться бензолдикарбонова кислота, а при нiтруваннi тiльки один моно нiтропродукт. Напишiть вiдповiднi реакцiї.
Розв’язок:
Виходячи із запропонованої брутто -формули та умови, що це ароматична сполука, одразу можна зробити висновок, що цей вуглеводень є одним з ксилолів (тобто, диметилбензолом). Але яким саме ізомером (о -, м - або п -ксилолом) він є, поки що встановити ми не можемо.
Тому реакцію його окиснення пишемо без позначення точного положення метильних замісників:

Точне положення замісників допомагає встановити вказівка на те, що при нітруванні утворюється тільки один мононітропродукт. Дійсно, якщо проводити нітрування м - або о -ізомерів, кількість продуктів буде відповідно три та два:


Тільки п -ксилол при нітруванні дає одну мононітропохідну:
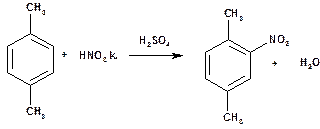
4. Завершiть схему:

Розв’язок:
Для кожного перетворення пишемо окрему реакцію. Перша реакція – алкілування бензолу за реакцією Фріделя-Крафтса:

Реакція сульфування призводить до утворення суміші двох ізомерів:

Реакцію окиснення пишемо для кожного з двох сульфопохідних окремо:

Задачі для самостійного розв’язку:
1. Запропонуйте схему синтезу етилбензолу. Подiйте на одержану сполуку водним розчином перманганату калiю, нітруючою сумішшю, бромом в присутності хлориду заліза (ІІІ).
2. Якi сульфокислоти можна одержати в результатi сульфування наступних сполук: бензолу, хлоробензолу, бензолсульфокислоти, бензойної кислоти, толуолу, нiтробензолу, фенолу. Назвiть одержанi сульфокислоти. Розташуйте вихiднi сполуки за легкістю сульфування.
3. Встановiть формулу речовини складу С7Н7Cl, яка при хлоруваннi надлишком хлору при сонячному опроміненні та пiдвищенiй температурi перетворюється на сполуку складу С7Н4Cl4. При окисненнi вихiдна сполука утворює о -хлоробензойну кислоту.
4. Напишiть реакцiї бромування толуолу i етилбензолу а) в присутностi каталiзатора, б) при сонячному опромiненнi. Дайте назви одержаним галогенопохiдним. Порiвняйте механiзми реакцiй.
5. Запропонуйте схему синтезу iзобутилбензолу, використовуючи реакцiю Вюрца -Фiттiга. Якi побічнi продукти будуть утворюватись за цiєю реакцiєю?
Спирти і феноли.
1. Напишіть рівняння реакції гідратації 1-бутену в присутності концентрованої сірчаної кислоти. Одержану сполуку окисніть і на продукт реакції подійте пропілмагнійбромідом.
Розв’язок:
При дії води (реакція гідратації) на алкени в присутності концентрованої сірчаної кислоти утворюються спирти, приєднання води до 1-бутену йде за правилом Марковнікова:

При окисненні спиртів утворюються альдегіди або кетони:

При взаємодії карбонільних сполук з магнійорганічними сполуками (реактивами Гриньяра) і наступному гідролізі утворюються відповідні спирти:

В результаті перетворень утворюється спирт 3-метил-3-гексанол.
2. Напишiть схеми одержання пiкринової кислоти iз хлоробензолу, фенолу, бензолсульфокислоти.
Розв’язок:
Пікринова кислота – це тривіальна назва 2,4,6-тринітрофенолу і синтезувати його в одну стадію неможливо. Щоб одержати пікринову кислоту з хлорбензолу (хлоробензену) або бензол сульфокислоти (бензенсульфокислоти) необхідно спочатку перетворити їх на фенол:

При дії концентрованої нітратної кислоти фенол перетворюється на пікринову кислоту:

3. З бензолу отримайте о -нітрофенол, м -нітрофенол, п -нітрофенол.
Розв’язок:
Щоб одержати о -і п -нітрофеноли із бензолу необхідно спочатку синтезувати фенол за наступною схемою:

При обробці фенолу розведеною нітратною кислотою при кімнатній температурі утворюється суміш о - і п -нітрофенолів:

Щоб одержати м -ізомер, необхідно спочатку синтезувати нітробензол (нітробензен):

Діючи на нітробензол хлором в присутності хлориду алюмінію, можна одержати м -нітрохлоробензол (м -нітрохлоробензен):
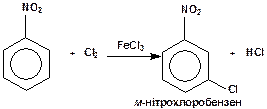
4. Яку будову має сполука складу С5Н12О, якщо вiдомо, що вона реагує з натрiєм, при окисненнi дає сполуку складу С5Н10О, а продукт її внутрiшньомолекулярної дегiдратацiї пiсля озонолiзу утворює ацетон i оцтовий альдегiд?
Розв’язок:
Виходячи з того, що сполука формули С5Н12О має у своєму складі кисень, її брутто -формула відповідає аліфатичним спиртам або етерам, крім того реагує з натрієм, відповідно вона є аліфатичним спиртом. При окисненні утворює сполуку, яка містить на два атоми водню менше і перетворюється на карбонільну сполуку. В результаті внутрiшньомолекулярної дегідратації вихідний спирт перетворюється на алкен. Алкен при озонолізі і подальшому гідролізі утворює ацетон (пропанон) і оцтовий альдегід (етаналь), тому потрібно виходити з кінцевих продуктів, конструюючи вихідний алкен.

Таким чином, вихідна сполука – 3-метил-2-бутанол (3-метилбутанол-2).
5. Запропонуйте найкращi методи синтезу iз етанолу - бромистого етилу, етилену, етилату натрію, етилпропіонату.
Розв’язок:
Щоб синтезувати бромистий етил (бромоетан) із етанолу необхідно подіяти, наприклад, Фосфор (V) бромідом на спирт:

Для синтезу етилену необхідно подіяти на спирт водовіднімаючим засобом при нагріванні, наприклад концентрованою сульфатною кислотою:
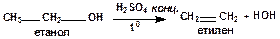
Етилат натрію одержують, діючи на спирт металічним натрієм:

Етилпропіонат (етиловий естер пропіонової кислоти) – продукт реакції естерифікації між етанолом і пропіоновою кислотою:
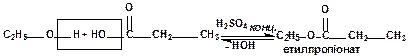
Задачі для самостійного розв’язку:
1. Напишіть структурну формулу сполуки складу С4Н8О, якщо вона знебарвлює бромну воду, реагує з натрієм, а при обережному окисненні утворює вінілоцтовий альдегід.
2. Використовуючи магнійорганічний синтез, отримайте 1-пропанол. Дегідратуйте його. Продукт дегідратації окисніть КМпО4(розв.).
3. Отримати з відповідних ненасичених сполук: ізопропіловий спирт, 2-метил-2-бутанол.
4. Виходячи з бензолу, синтезуйте а) о - і п -бромофеноли; б) трибромофенол; в) етиловий естер п -нітробензойної кислоти.
5. Виведіть формули ізомерних вторинних гептилових спиртів з п’ятьма атомами вуглецю в основному ланцюзі, назвіть їх.
Альдегіди і кетони
1. Запропонуйте схеми реакцій, які дозволяють відрізнити пропіоновий альдегід (пропаналь) від метилетилкетону (2-бутанону).
Розв’язок:
Альдегіди і кетони по-різному відносяться до дії окисників. Альдегіди легко окиснюються в присутності багатьох окисників до відповідних кислот, тому для ідентифікації широко використовують саме реакції їх окиснення.
Так під дією гідроксиду міді Cu(OH)2 пропіоновий альдегід окиснюється до пропіонової кислоти та утворюється Купрум (I) оксид яскраво-червоного кольору. Це – якісна реакція на альдегіди.

Ще однією якісною реакцією на альдегіди є “реакція срібного дзеркала”- окиснення альдегідів аміачним розчином оксиду срібла (реактив Толленса). Йон срібла в даной реакції відновлюється до вільного срібла, яке виділяється у вигляді дзеркала на стінках пробірки:

Кетони у наведені реакції не вступають. Окиснення кетонів відбувається складніше, з розривом вуглецевого ланцюга з обох боків карбонільної групи. При цьому утворюється суміш відповідних кислот. Так, при окисненні метилетилкетону утворюється суміш наступних кислот:

2. Отримайте сухою перегонкою кальцієвих солей відповідних карбонових кислот оцтовий альдегід (етаналь) та подійте на одержану сполуку: а) НСN, б) NaHSO3, в) H2O, г) CH3OH, д) C2H5MgBr.
Розв’язок:
При пропусканні суміші карбонових кислот над ZnO або MgO утворюються солі кислот, які при високих температурах розкладаються на відповідні карбонільні сполуки та карбонати. Кислотні залишки у цих солях можуть бути однаковими або різними. Так, якщо одна з кислот мурашина, утворюються альдегіди, у решті випадків - кетони. Тому, для одержання оцтового альдегіду потрібно взяти змішану сіль мурашиної та оцтової кислот:

Для альдегідів і кетонів характерними є реакції нуклеофільного приєднання, які в свою чергу, умовно можна поділити на дві основні групи: 1) просте приєднання по подвійному зв’язку карбонільної групи і 2) приєднання - відщеплення. Реакції оцтового альдегіду з НСN, NaHSO3, H2O, CH3OH та C2H5MgBrналежать до реакцій першої групи, в процесі яких утворюється новий хімічний зв’язок між електрофільним атомом вуглецю карбонільної групи та іншим, невуглецевим атомом О-нуклеофілу, S-нуклеофілу, H-нуклеофілу.
Так, синильна кислота (НСN) приєднується до карбонільних сполук з утворенням ціангідринів чи a-гідроксинітрилів. У випадку реакції оцтового альдегіду з НСN утворюється нітрил a-оксипропіонової кислоти:

Гідросульфіт (бісульфіт) натрію (NaHSO3) приєднується до альдегідів і метилкетонів з утворенням кристалічних продуктів алкансульфонових кислот, що дозволяє виділяти карбонільні сполуки з реакційного середовища для ідентифікації. Реакція відбувається без каталізатора, тому що гідросульфіт-йон достатньо сильний нуклеофіл:

При нагріванні з водним розчином мінеральної кислоти чи карбонату натрію відбувається руйнування бісульфітної сполуки з виділенням вільного альдегіду чи кетону. Дана реакція є не тільки якісною на карбонільну групу, а також використовується для виділення та очистки альдегідів та кетонів.
Вода, як слабкий О-нуклеофіл, реагує з активними карбонільними сполуками, що мають відносно великий позитивний заряд d+ на карбонільному атомі вуглецю (формальдегід, ацетальдегід, галогенозаміщені альдегіди, наприклад, такі як хлораль ССl3-CHO) з утворенням гідратів. Внаслідок цього оцтовий альдегід у водних розчинах існує практично весь у гідратній формі:

При взаємодії альдегідів із спиртами утворюються напівацеталі, а в присутності каталітичних кількостей мінеральних кислот - ацеталі:

Утворення ацеталів застосовують для захисту карбонільної групи при проведенні реакції в лужному середовищі, в якому вони не гідролізують. При нагріванні з розведеними кислотами ацеталі легко гідролізуються до вихідних сполук.
Альдегіди і кетони реагують з алкіл- та арилмагнійгалогенідами (реактиви Гріньяра) з утворенням продуктів приєднання по карбонільній групі, які гідролізують у присутності розведених мінеральних кислот до спиртів.
3. Запропонуйте декілька методів одержання ізомасляного альдегіду (2-метилпропаналю) та пропанону та подійте на одержані сполуки H2N-OH та H2N-NH2.
Розв’язок:
До основних методів одержання альдегідів і кетонів належать окиснення насичених та ненасичених вуглеводнів, спиртів, оксосинтез, гідроліз галагенопохідних, гідратація алкінів.
Так, для одержання ізомасляного альдегіду можна запропонувати реакцію окиснення алкенів. Як вихідний алкен потрібно використати 4-метил-2-пентен. Під дією сильних окисників (CrO3, HNO3, K2Cr2O7, KMnO4) відбувається розрив подвійного зв’язку з утворенням суміші альдегідів:

Алкени в присутності кобальтових каталізаторів під тиском взаємодіють з синтез-газом з утворенням альдегідів. Причому, реакцію з етиленом і пропіленом проводять у газовій фазі, а з алкенами С4-С20 - у рідкій фазі. Звичайно утворюється суміш ізомерів. З пропілену таким способом отримують суміш масляного та ізомасляного альдегідів:

При взаємодії алкенів з озоном утворюються озоніди - циклічні пероксидні сполуки, які легко розщеплюються цинком в оцтовій кислоті з утворення альдегідів чи кетонів:
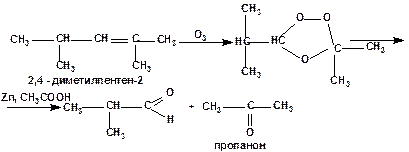
При гідролізі гем -дигалогеналканів (які містять галогени при одному вуглецевому атомі) з атомами галогену при першому атомі вуглецю утворюються альдегіди, а при другому – кетони:

Альдегіди та кетони взаємодіють з азотистими основами (H2N-Х, де Х- Alk, Ar, OH, NH2) з утворенням нестійких продуктів нуклеофільного приєднання, які стабілізуються завдяки відщепленню молекули води. Дана група реакцій одержала назву реакцій приєднання - відщеплення.
Взаємодія альдегідів та кетонів з гідроксиламіном (H2N-OH)застосовуєтьсядляїх кількісного визначення. Отримані продукти конденсації називаються оксимами (альдоксимами та кетоксимами відповідно). Взаємодія карбонільних сполук з H2N-OH відбувається наступним чином:

Альдоксими та кетоксими - це кристалічні сполуки з чіткою температурою топлення. В кислому середовищі вони легко гідролізують з утворенням вихідних сполук. Тому дану реакцію використовують для виділення та ідентифікації альдегідів та кетонів.
З гідразином (H2N-NH2) альдегіди та кетони реагують з утворенням гідразонів:
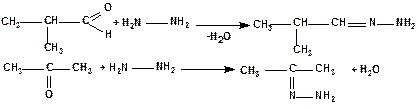
Дану реакцію також можна використовувати для ідентифікації альдегідів і кетонів. Одержані продукти реакцій є кристалічними речовинами, які можна виділити і визначити за температурою топлення.
4. Які властивості має альдегід наступної будови:  . Напишіть для нього рівняння реакцій з: а) H2O, б) HBr, в) HCN.
. Напишіть для нього рівняння реакцій з: а) H2O, б) HBr, в) HCN.
Розв’язок:
Сполуки, які містять у молекулі карбонільну групу і кратні зв’язки, називаються ненасиченими альдегідами та кетонами. Наведений альдегід має назву акролеїн (пропен-2-аль) та ще його відносять до α, b-спряжених карбонільних сполук. Хімічні властивості α, b-ненасичених альдегідів, що містять у своєму складі спряжену систему, мають деякі особливості. Приєднання до них галогеноводнів та води перебігає проти правила Марковнікова.
Так, спочатку відбувається приєднання бромистого водню по кінцях спряженої системи з утворенням нестійкого енолу, який одразу ізомеризується в альдегід:

Приєднання молекули води відбувається за аналогічним механізмом:

5. Синтезуйте за реакцією Фріделя-Крафтса кетони із а) бензолу і хлорангідриду оцтової кислоти; б) толуолу та суміші (CO+HCl).
Розв’язок:
Ароматичні кетони можна одержати за реакцією Фріделя-Крафтса. Синтез здійснюють шляхом ацилювання аренів карбоновими кислотами або їх похідними (галогенангідридами, ангідридами, нітрилами, амідами, естерами), які за ацилюючою ефективністю розташовуються в наступний ряд:
R-CO-Cl > (RCO)2O > R-CN > R-CO-OR > R-COOH.
Так при ацилюванні бензолу хлорангідридом оцтової кислоти в присутності кислот Льюїса одержують ацетофенон. Реакція відбувається за наступною схемою:

Одним з методів одержання ароматичних альдегідів є реакція Гаттермана-Коха. Даний метод базується на прямому введенні альдегідної групи у бензольне ядро, тому цю реакцію ще називають реакцією формілювання. Формілювання ароматичних вуглеводнів проводять сумішшю оксиду вуглецю (II) та хлороводню у присутності хлориду алюмінію та хлориду міді (I). Тому при дії на толуол суміші (CO+HCl) за реакцією Гаттермана-Коха можна одержати п -толуїловий альдегід:

6. Порівняти умови проходження альдольної, кротонової конденсації та конденсації Тищенка для пропіонового альдегіда, навести схеми реакцій.
Розв’язок:
Альдегіди з атомами Гідрогену в a-положенні здатні вступати в реакцію альдольної конденсації в присутності каталітичної кількості основ у відповідності до схеми:

Продукти альдольної конденсації - b-оксиальдегіди - при нагріванні легко втрачають воду, перетворюючись на a,b-ненасичені альдегіди (кротонова конденсація):
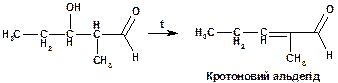
При нагріванні альдегідів з етилатом алюмінію (Al(OC2H5)3) утворюються естери карбонових кислот:

Задачі для самостійного розв’язку:
1. Речовина складу С6Н14О при окисненні дає сполуку С6Н12О, яка взаємодіє з фенілгідразином, але не дає реакції „срібного дзеркала”. Продукт дегідратації вихідної сполуки при окисненні утворює метилетилкетон та оцтову кислоту. Встановіть будову речовини та напишіть рівняння реакцій.
2. Як з бензолу одержати бензальдегід. Напишіть для нього рівняння реакцій з синильною кислотою, бісульфітом натрію.
3. Які карбонільні сполуки утворюються, якщо ввести в реакцію Кучерова 3-етилбутін-1, ацетилен? Запропонуйте інший метод одержання цих карбонільних сполук.
4. Які сполуки утворюються при дегідруванні спиртів: а) ізопропілового; б) 3-метилбутанолу-1; в) 3-метилпентанолу-2, г) 4-етилгептанолу-2. На одержані сполуки подійте аміачним розчином оксиду срібла.
5. Напишіть реакції гідробромування 2-метил-бутен-3-аль-1 та пропеналя. Що буде відбуватися при дії на ці сполуки хлору в кислому середовищі?
6. Написати рівняння реакцій альдольної та кротонової конденсації для наступних сполук: оцтового альдегіда; масляного альдегіда; метилетилкетона; ізомасляного альдегіда; диметилкетона.
Карбонові кислоти
1. Які реакції будуть відбуватися при нагріванні: а) щавелевої, б) малонової, в) глутарової та г) фталевої кислот?
Розв’язок:
Щавелева, малонова, глутарова та фталева кислоти по-різному відносяться до нагрівання та утворюють при цьому різні продукти. Так при нагріванні вище температур топлення щавелева та малонова кислоти піддаються декарбоксилюванню, тобто відщеплюють CO2 по одній карбоксильній групі. В результаті вони перетворюються у монокарбонові кислоти – мурашину та оцтову відповідно за наступною схемою:

Глутарова кислота при нагріванні утворює циклічний ангідрид за наступною схемою:

При нагріванні о -фталева кислота легко перетворюється в ангідрид наступної будови:
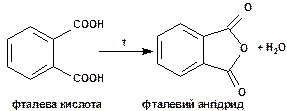
2. Використовуючи як вихідну сполуку бутен-2, запропонуйте декілька методів одержання 2-метилбутанової кислоти. Для одержаної кислоти напишіть рівняння реакцій з: а) NaOH; б) SOCl2; в) NH3; г) С2H5OH (H2SO4) та нагрійте її в присутності P2O5.
Розв’язок:
Одним з методів одержання монокарбонових кислот є гідрокарбоксилювання алкенів. Даний метод використовується в промисловості. Алкени з оксидом вуглецю (II) та водою в присутності кислого каталізатора при нагріванні та тиску утворюють карбонові кислоти. Тому його можна запропонувати як один з методів одержання 2–метилбутанової кислоти:

Можна запропонувати інший шлях одержання 2–метилбутанової кислоти. Відомо, що алкени взаємодіють з галогеноводневими кислотами з утворенням відповідних галогеналканів:

Галогеналкани вступають в реакцію з ціанідами лужних металів, з утворенням нітрилів:

При нагріванні нітрилів з водними розчинами кислот та лугів вони піддаються гідролізу з утворенням карбонових кислот. Як проміжні продукти реакції утворюються аміди кислот:

Карбонові кислоти при взаємодії з активними металами, основними оксидами, гідроксидами та карбонатами лужних металів утворюють солі. При дії NaOH на 2–метилбутанову кислоту утворюється сіль цієї кислоти - 2–метилбутаноат натрію:

При дії на карбонові кислоти хлоридів фосфору (III) PCl3 та фосфору (V) PCl5, броміду фосфору (III) PBr3 чи тіонілхлориду ( SOCl2) утворюються галогенангідриди карбонових кислот:

Галогенангідриди карбонових кислот – реакційноздатні речовини, які широко використовують в органічному синтезі.
При обробці карбонових кислот аміаком утворюється амонійна сіль, яка при нагріванні у сухому вигляді (піроліз), відщеплює воду та перетворюється на амід:
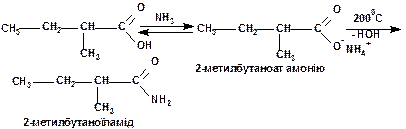
При нагріванні в присутності кислотного каталізатора кислоти реагують із спиртами з утворенням естерів. Реакція естерифікації зворотна. Естер, що утворився, у кислому середовищі піддається гідролізу до вихідних кислоти та спирту:

У присутності водовіднімаючих засобів, таких як оксид фосфору (V) P2O5, при нагріванні кислоти піддаються міжмолекулярній дегідратації з утворенням ангідридів:

3. Запропонуйте декілька методів одержання акрилової кислоти та напишіть для неї рівняння реакції з HBr.
Розв’язок:
Акрилова (пропен-2-ова) кислота відноситься до ненасичених монокарбонових кислот, для одержання яких можна використати методи синтезу насичених карбонових кислот. Тільки як вихідні речовини в даному випадку слід використати ненасичені сполуки, наприклад окиснення ненасичених первинних спиртів та альдегідів в м’яких умовах, гідроліз нітрилів. Однак є і специфічні методи одержання ненасичених кислот: гідрокарбоксилювання алкінів (реакція Реппе) та елімінування b-галоген- та b-гідроксикарбонових кислот.
У присутності карбонілів металів (реакція Реппе) алкіни взаємодіють з оксидом вуглецю у водному середовищі з утворення a, b-ненасичених монокарбонових кислот:

b-Галогенокарбонові кислоти при нагріванні з водою відщеплюють галогеноводень та перетворюються на a, b-ненасичені карбонові кислоти. Так, при нагріванні b-хлоропропіонова кислота відщеплює HCl та перетворюється при цьому на акрилову.

b-Гідроксипропіонова кислота при нагріванні відщеплює молекулу води за наступною схемою:

Реакційна здатність ненасичених монокарбонових кислот обумовлена наявністю в їх структурі карбоксильної групи та кратного (подвійного) зв’язку. За рахунок наявності карбоксильної групи ненасичені кислоти вступають в реакції, що характерні для насичених кислот, а за рахунок кратного зв’язку в вуглеводневому радикалі вони проявляють властивості алкенів (алкінів). Однак приєднання галогеноводнів до a, b-ненасичених кислот відбувається проти правила Марковнікова. Це пояснюється електроноакцепторним впливом карбоксильної групи за рахунок – М та – І- ефектів. Тому при дії HBr на акрилову кислоту утворюється b-бромопропіонова кислота:

4. Наведіть схеми реакцій бензойної кислоти з: хлоридом фосфору (V), оцтовим ангідридом (в кислому середовищі) та Br2 (в присутності FeBr3).
Розв’язок:
Реакційна здатність аренмонокарбонових кислот обумовлена наявністю у їх структурі карбоксильної групи та бензольного ядра. По карбоксильній групі для них характерні реакції, які властиві насиченим монокарбоновим кислотам, а саме, утворення солей, галогенангідридів, ангідридів, естерів, амідів. При взаємодії бензойної кислоти з хлоридом фосфору (V) утворюється хлорангідрид бензойної кислоти:
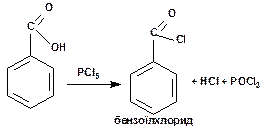
При дії оцтового ангідриду в кислому середовищі на бензойну кислоту відбувається реакція міжмолекулярної дегідратації, в результаті якої утворюється ангідрид бензойної кислоти та як побічний продукт - оцтова кислота:

За рахунок наявності бензольного кільця аренмонокарбонові кислоти вступають в реакції електрофільного заміщення (нітрування, сульфування, галогенування), характерні для ароматичних вуглеводнів. Карбоксильна група є орієнтантом другого роду, тому в реакціях електрофільного заміщення вона направляє замісник (групу, що атакує) в мета – положення:
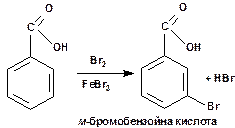
5. Синтезуйте янтарну кислоту та напишіть для неї рівняння реакцій з гідроксидом натрію та піддайте її нагріванню.
Розв’язок:
Янтарна кислота відноситься до дикарбонових кислот, тобто має у своєму складі дві карбоксильні групи. За замісниковою номенклатурою ІЮПАК вона має назву бутан-1,4-діова кислота. Для одержання дикарбонових кислот можна запропонувати ті ж самі методи, що і для монокарбонових, використовуючи як вихідні речовини відповідні біфункціональні сполуки. Наприклад, янтарну кислоту можна одержати при окисненні двупервинних гліколів:

При окисненні діальдегідів:

При окисненні гідроксикислот, в даному випадку 4 - гідроксибутанової кислоти:

За хімічними властивостями дикарбонові кислоти подібні до монокарбонових. Вони утворюють подібні похідні лише з різницею у тому, що реакції відбуваються за участю однієї чи двох карбоксильних груп. При дії гідроксиду натрію утворюються як нейтральні, так і кислі солі янтарної кислоти:

Разом з тим, наявність двох карбоксильних груп в одній молекулі обумовлюють деякі особливості хімічних властивостей двохосновних кислот.
При нагріванні янтарна кислота утворює циклічний ангідрид за наступною схемою:
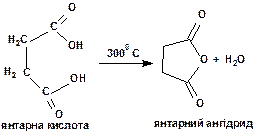
Задачі для самостійного розв’язку:
1. Запропонуйте методи синтезу із пропілену: а) масляної кислоти, б) ізомасляної, її амонійної солі та аміду.
2. Отримати пропіонову кислоту двома способами, виходячи з бромистого етилу двома способами. Для отриманої кислоти напишіть рівняння реакцій з п’ятихлористим фосфором, аміаком при нагріванні, із вторинним бутиловим спиртом (в присутності H2SO4).
3. Напишіть схеми реакцій, за допомогою яких можна відрізнити одну від одної: мурашину, оцтову та метакрилову кислоти.
4. Запропонуйте найбільш раціональну послідовність реакцій в такому перетворенні:

5. Напишіть рівняння реакцій гідролізу таких сполук:

Оксикислоти. Оптична ізомерія.
1. Дайте визначення за R,S-системою D-2-гідрокси-3-метилбутановій кислоті.
Розв’язок
Спочатку необхідно зобразити структурну формулу кислоти:

З чотирьох наявних атомів вуглецю тільки С-2 є асиметричним (С-3 має два однакових замісника СН3).
Наступним кроком є побудова проекційної формули таким чином, щоб конфігурація асиметричного атома вуглецю С-2 співпадала з конфігурацією асиметричного атома вуглецю D-гліцеринового альдегіду:
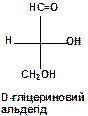
Для цього слід пам’ятати, що в проекційній формулі Фішера функціональні групи –OH, –NH2, галогени розташовані справа від вертикальної лінії, якщо сполука відноситься до D-ряду (для L-ряду - зліва):
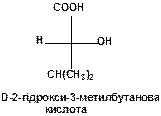
Далі:
· визначають старшинство замісників;
· проекційну формулу Фішера шляхом парного числа переміщень замісників асиметричного атома вуглецю переписують таким чином, щоб наймолодший замісник (Н) перемістився у низ вертикальної лінії (цьому перетворенню відповідає таке розташування молекули у просторі, коли наймолодший замісник займає найвіддаленіше положення щодо спостерігача). Число переміщень обов’язково повинно бути парним, тільки у такому випадку абсолютна конфігурація не змінюється!

· встановлюють старшинство замісників за величиною атомного номера елемента, зв’язаного з асиметричним (хіральним) центром; якщо атомні номери у замісників виявляються однаковими, для вирішення питання про старшинство враховують атомні номери елементів „другого шару”, у атомів „другого шару” з подвійним зв’язком номер слід подвоювати.
Отже, для –COOH сума атомних номерів розраховується як: 16*2+16=48, а для –СH(CH3)2: 1+12*2=25. Таким чином, група –COOH є старшою.
· встановлюють напрямок (за годинниковою стрілкою чи проти) зменшення старшинства замісників, зв’язаних із асиметричним атомом:
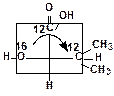
Якщо старшинство замісників зменшується за годинниковою стрілкою, така конфігурація позначається R (лат.„rectus”- правий), а проти – S (лат.“sinister”- лівий). У нашому випадку це R-ізомер.
2. За реакцією Реформатського синтезуйте 3-окси-3-метилпентанову кислоту.
Розв’язок:
Починаємо із побудови структурної формули:

Згадуємо, що реакція Реформатського є загальним методом синтезу b-оксикислот та схематично може бути зображена таким чином:

Тепер наводимо реакції для синтезу 3-окси-3-метилпентанової кислоти:
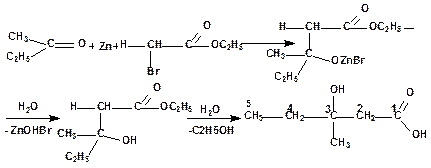
3. Для 3-окси-3-метилпентанової кислоти напишіть рівняння реакцій з металічним натрієм, PCl5, хлористим ацетилом (хлорангідридом оцтової кислоти).
Розв’язок:
Слід згадати, що оксикислоти є такими органічними сполуками, що поєднують властивості кислот та спиртів, тобто є біфункціональними. Отже, потрібно бути уважними під час написання хімічних реакцій для цього класу сполук: з деякими реагентами взаємодіє і спиртова і кислотна група, з іншими – тільки одна з них.
Так, Na та PCl5 реагуватимуть з двома функціональними групами, тому що і спирти і карбонові кислоти реагують з цими реагентами:
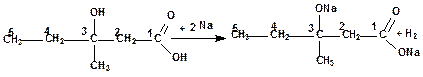

а з галогенангідридом кислоти (хлористий ацетил) буде реагувати тільки спиртова функціональна група:

4. Як синтезувати мигдальну кислоту із бензальдегіду?
Розв’язок:
Мигдальна кислота має наступну структурну формулу:

Тобто, мигдальна кислота є ароматичною α-оксикислотою. Слід згадати, що загальним методом синтезу α-оксикислот є циангідриновий синтез, за яким і можна синтезувати мигдальну кислоту з бензальдегіду:

5. Напишіть проекційні формули всіх стереоізомерних форм сполуки HOOC‑CH(CH3)‑CHBr‑COOH. Які з них є енантіомерами та які – діастереомерами?
Розв’язок:
Спочатку необхідно зобразити структурну формулу кислоти (назва сполуки за систематичною номенклатурою 2-бромо-3-метил-бутан-1,4-діова кислота).

Видно, що сполука має два атоми вуглецю (С-2 та С-3), кожний з яких містить по 4 різні замісники (H, Br, COOH та CH(CH3)COOH для С-2 і H, CH3, COOH та CH(Br)COOH для C-3) і тому є асиметричними. Тоді кількість можливих стереоізомерів складає 22 = 4.
Наводимо їх у вигляді проекційних формул Фішера, враховуючи деякі прийняті правила їх побудови:
· асиметричні атоми вуглецю знаходяться у точці перетину горизонтальної та вертикальної ліній і не позначаються символом С;
· для гідроксикислот (а також амінокислот та галогенокарбонових кислот) на вертикальній лінії розташовують карбоксильну групу, а на горизонтальній – атом водню та групи з гетероатомами (OH-, NH2-, галогени).
Тепер слід згадати, що енантіомерами (антиподами) є пари стереоізомерів, які характеризуються взаємопротилежним розміщенням атомних груп біля всіх асиметричних вуглецевих атомів. Отже, енантіомерами є пари А,В та C,D.
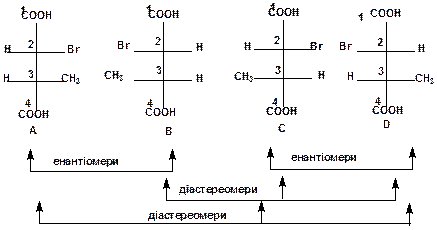
Стереоізомери, які характеризуються однаковим просторовим розміщенням атомних груп біля одного з асиметричних атомів та взаємопротилежним – у інших, називаються діастереомерами. Отже, діастереомерами є пари А,C (конфігурація атома С-2 співпадає, а С-3 – протилежна); B,C (конфігурація атома С-3 співпадає, а С-2 – протилежна); А,D (конфігурація атома С-2 співпадає, а С-3 – протилежна; B,D (конфігурація атома С-3 співпадає, а С-2 – протилежна).
Задачі для самостійного розв’язку:
1. Назвіть за номенклатурою ІЮПАК (систематична номенклатура) такі сполуки: а) (OH)CH2-CH2-COOH, б) (OH)CH2‑CH(OH)‑COOH, в) HO-C6H5-COOH, г) CH3‑CH(OH)‑CH(C2H5)‑CH2-COOH. Серед наведених сполук знайдіть такі, що можуть існувати у вигляді оптичних ізомерів і зобразіть ці ізомери за допомогою формул Фішера.
2. Чим відрізняються: а) молочна кислота та b-оксипропіонова кислота; б) (+) та (-) молочні кислоти? Напишіть формули оптичних ізомерів для бутандіол-2,3-діової-1,4-кислоти.
3. Дайте визначення за R,S-номенклатурою таким оптичним ізомерам:



4. Напишіть схеми наступних перетворень: а) 1-пропанолу на 3-оксибутанову кислоту; б) 1-пропанолу на 2-оксибутанову кислоту. Які продукти реакції утворюються при нагріванні синтезованих оксикислот, напишіть схеми відповідних реакцій. Назвіть сполуки, що утворилися.
5. Синтезуйте молочну кислоту з оцтового альдегіду. Подійте на неї NaOH, Na, оцтовим ангідридом, нагрійте цю кислоту.
Вуглеводи.
1. Запишiть по стадiях процес цiангiдринового синтезу, в якому вихiдною речовиною є маноза.
Розв’язок:
Необхідно згадати, що маноза є одним із стереоізомерів моносахариду, що містить альдегідну групу та має 6 вуглецевих атомів. Формулу стереоізомеру необхідно зображати за допомогою проекційної формули Фішера.
Далі згадуємо, що ціангідриновий синтез складається з чотирьох стадій. Слід бути уважними при написанні першої стадії - приєднання HCN. На цій стадії утворюються два стереоізомерних продукти за рахунок створення нового асиметричного атома вуглецю, отже, наступні стадії необхідно писати окремо для утворення двох стереоізомерів.
Перший стереоізомер:

Другий стереоізомер:
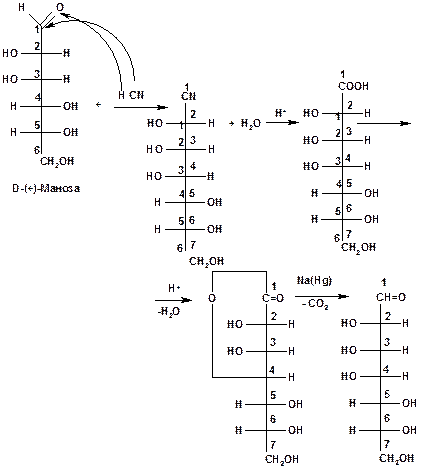
Отже, в результаті синтезу утворюються дві стереоізомерні альдогептози (загальна кількість атомів вуглецю – 7).
2. За допомогою яких реакцiй можна виконати перетворення D-глюкози у вiдповiднi пентози?
Розв’язок:
Враховуючи те, що глюкоза є альдогексозою (містить альдегідну групу та має 6 атомів вуглецю), а за умовою задачі необхідно синтезувати альдопентозу (сполуку з 5 атомами вуглецю), скористаємось розщепленням за Руфом для зменшення довжини вуглецевого ланцюга.

Отже, в результаті проведених перетворень утворюється D-(-)-Арабіноза.
Перехід від вищих моносахаридів до нижчих можна здійснити також через розщеплення за А. Волем з використанням гідроксиламіну:

Дата добавления: 2015-10-24; просмотров: 1562 | Нарушение авторских прав
| <== предыдущая страница | | | следующая страница ==> |
| Хімічні властивості | | | Напишiть проекцiйнi формули моноз, епiмерних D-глюкозi. |