
Реакция дегидрирования является обратной процессу гидрирования. Она также идет по свободнорадикальному механизму, как правило, на поверхности катализатора (соли меди, хрома, металлические серебро, палладий или платина). Для отрыва двух атомов водорода необходимо не только применение катализатора, но и высокая температура, т. к. процесс является равновесным и эндотермическим. Субстрат дегидрирования сорбируется на поверхности катализатора, происходит разрыв С-Н, CN-H или CО-Н связей с образованием двойной связи C=C, C=O, C=N и выделением молекулы водорода. При гидрировании после окончания процесса объем реакционной массы уменьшается, и для смещения равновесия используют повышенное давление. В случае дегидрирования наоборот – объем реакционной массы увеличивается, для смещения равновесия необходимо понижать давление. Так степень конверсии этилбензола в стирол при давлении 0,1 МПа составляет 40 %, а при 0,01 МПа уже 80 %. Необязательно реакции проводить при пониженном давлении, к тому же результату приводит разбавление реагентов инертным газом, т. к. их парциальное давление уменьшается.
Наиболее многотоннажным производством, в котором используется эта реакция, является получение бутадиена-1,3 и изопрена. Дегидрирование осуществляют как в одностадийном, так и двустадийном варианте. Степень конверсии бутана составляет около 50 %. На схемах приведены условия синтеза бутадиена-1,3:
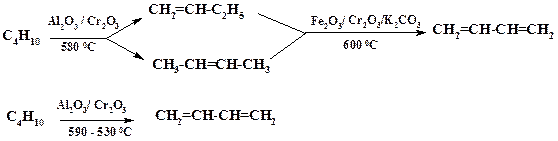
Технологическое оформление процесса довольно сложное (см. [2] к разделу 1.3). В случае одностадийного процесса энергозатраты ниже.
Стирол, метилстирол и дивинилбензол также получают дегидрированием соответствующих углеводородов. Для поддержания температуры и снижения парциального давления в пары этилбензола вводят перегретый пар.
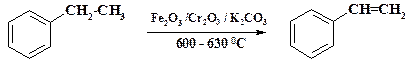
Формальдегид (водный раствор – формалин), его олигомеры и полимеры находят широкое применение в медицинской промышленности. По одному из способов формальдегид получают окислительным дегидрированием метанола на серебряном катализаторе. Серебро наносят на пемзу. Соотношение реакций окисления и дегидрирования составляет обычно 55 и 45 %.
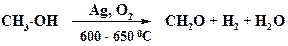
Из напорного бака 90 % водный метанол поступает в испаритель. Через распределительное устройство подают воздух так, чтобы в 1 л паровоздушной смеси содержалось около 0,5 г метанола, что существенно выше пределов взрываемости. Процесс контролируется автоматически, т. к. несоблюдение концентрации метанола в паровоздушной смеси может привести к взрыву. Смесь поступает в перегреватель, а затем в контактный аппарат. После прохождения процесса полученная смесь поступает в подконтактный теплообменник, где она охлаждается до 100 – 130 oС, а затем на абсорбер. Пар, полученный в этом теплообменнике, идет на перегреватель. Получают 36 – 37 % формалин, содержащий, в зависимости от аппаратурного оформления абсорбции, от 1 до 10 % метанола. Выход формальдегида составляет от 85 до 90 %. Синтез формальдегида проводят также и в режиме реакции окисления без дегидрирования. В этом случае применяют железо-молибденовый катализатор [твердый раствор MoO3 в Fe2(MoO4)3]. Аналогично формальдегиду окислительным дегидрированием получают глиоксаль из этиленгликоля.
Еще одним продуктом, который используют при получении полимеров и лекарственных средств, является циклогексанон. По одному из методов его получают дегидрированием циклогексанола (см. раздел 2.5.2). Процесс ведут в трубчатом теплообменнике при температуре 430 – 450 oС, катализатором служит оцинкованное железо. Основным побочным продуктом является циклогексен. Чистый продукт получают ректификацией.
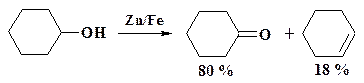
В производстве препарата папаверин (биологическое действие и полный синтез приведены в разделе 3.7, получение полупродуктов в разделе 2.3.4) на последней стадии используют реакцию дегидрирования:
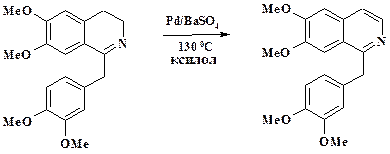
В качестве катализатора этой реакции применяют палладий, нанесенный на сульфат бария. Процесс вели при температуре 200 oС в очищенном тетралине. Недостатком этого метода являлось то, что папаверин приходилось очищать от примеси нафталина, который получался при дегидрировании тетралина. Тетралин был заменен на ксилол, при этом увеличилась чистота препарата.
В производстве трихопола (метронидазола) (биологическое действие препарата рассмотрено в разделе 2.3.1) при получении 2-метилимидазола проводят дегидрирование с использованием катализатора – формиата никеля. Реакцию ведут при температуре 250 oС в дифенилоксиде. Полный синтез препарата приведен на схеме:
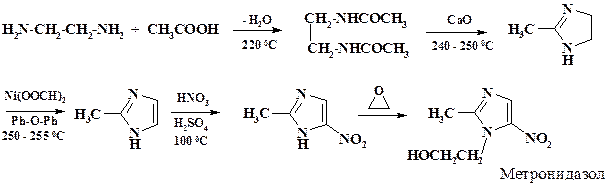
Следует отметить интересный метод ароматизации дигидропиразола, приведенный на схеме:
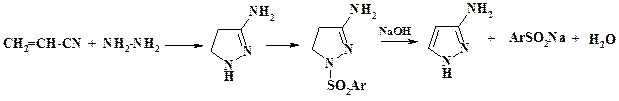
При обработке щелочью сульфаниламидного производного, полученного при взаимодействии 3-амино-4,5-дигидропиразола с безолсульфохлоридом, происходит внутримолекулярная окислительно-восстановительная реакция. В результате образуется 3-аминопиразол и натриевая соль бензолсульфиновой кислоты.
Дата добавления: 2015-09-04; просмотров: 161 | Нарушение авторских прав
| <== предыдущая страница | | | следующая страница ==> |
| Реакции окисления | | | Реакции конденсации |