
Читайте также:
|
Для обратимых процессов, как известно
dQ = T dS
Так как одновременно
dQ = c dT,
то из равенства правых частей этих уравнений получим
dS = c 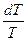 (153)
(153)
Из (153) и (142) для политропного процесса
dSn = 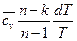 ,
,
Откуда после интегрирования окончательно получим:
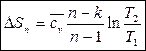 (154)
(154)
Подставляя в (154) отношения 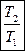 из (144*) и (146) получим еще две формулы для расчета ∆Sn:
из (144*) и (146) получим еще две формулы для расчета ∆Sn:
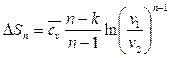
или
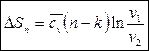 (155)
(155)
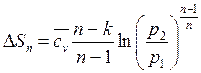
или
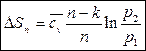 (156)
(156)
Как известно, в инженерных расчетах полагают, что энтропия равна нулю при нормальных физических условиях. Тогда, подставляя в (154) Тн вместо Т1 и Т вместо Т2 получим формулу для расчета энтропии:
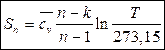 (157)
(157)
Из формул (155) и (156) аналогично получим:
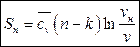 (158)
(158)
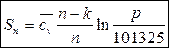 (159)
(159)
Дата добавления: 2015-09-01; просмотров: 170 | Нарушение авторских прав
| <== предыдущая страница | | | следующая страница ==> |
| IV.2. Работа, теплота и внутренняя энергия в политропном процессе. | | | Раздел V. Исследование изопроцессов. Работа, теплота, внутренняя энергия в изопроцессах. |