
|
Читайте также: |
В теплотехнике принято определять топливо как вещество или совокупность веществ, находящихся в любом агрегатном состоянии, способных в результате экзотермических химических реакций (го рения) образовывать высокотемпературные конечные продукты. Компонентом топлива называют отдельно подводимую к двигателю часть топлива, отличающуюся по составу от других его частей. Горючее — компонент топлива, окисляющийся в процессе горения. Окислитель — компонент топлива, служащий для окисления горюче го. При использовании этих определений бензины и дизельные топлива следует называть горючим, для окисления которого используется окислитель—воздух (точнее кислород воздуха). Однако исторически терминология ДВС сложилась так, что термин «топливо» применяется вместо термина «горючее». Для бензинов и дизельных топлив ниже использован термин «моторное топливо», или сокращенно «топливо».
§ 2.1. Классификация топлив
Топлива для ДВС разделяют по типу двигателя, для использования в котором они предназначены, на бензины и дизельные топлива; по агрегатному состоянию — на жидкие и газообразные; по химическому составу — на углеводородные и неуглеводородные; по виду исходного сырья — на нефтяные и альтернативные; по способу хранения на автомобиле — на одно- и многокомпонентные (последние называют топливами раздельной подачи).
Термины «бензин» и «дизельное топливо» используют для обозначения нефтяных топлив, применяемых соответственно для двигателей с принудительным воспламенением и для дизелей.
Различие между жидкими и газообразными топливами заключено в их разных агрегатных состояниях при нормальных атмосферных условиях. В современной транспортной технике преимущественное применение получили жидкие топлива. Под газообразными (газовыми) топливами понимается топливо, поступающее в систему топливоподачи двигателя в газовой фазе. Газообразные топлива могут находиться в топливном баке транспортного средства в сжатом или сжиженном состоянии. В первом случае газы называют сжатыми, во втором сжиженными. Такое деление условно. Агрегатное состояние газа определяется параметрами его хранения в топливных емкостях (баках) — температурой и давлением. В зависимости от конструкции бака один и тот же газ может находиться в них как в жидкой, так и в газовой фазе. Например, метан используется и как сжатый газ, находящийся в баках (баллонах) под высоким давлением (до 20 МПа), и как сжиженный, находящийся в термостатированных емкостях при температуре, равной или ниже температуры сжижения (—161°С).
Газообразные топлива — перспективный вид топлив для ДВС. Это объясняется следующими основными преимуществами этих топлив перед жидкими: меньшей стоимостью; снижением износа и повышением долговечности цилиндропоршневой группы двигателей; уменьшением потребности в высококачественных моторных маслах и увеличением срока их бессменной работы в двигателе; большей полнотой сгорания и, как следствие этого, меньшим загрязнением среды.
К нефтяным относят топлива, изготовленные из природной нефти. Нефтяные топлива являются основными топливами для сов ременных ДВС, что объясняется их преимуществами перед другими видами топлив: освоенностью производства, транспортировки, хранения и подачи в камеру сгорания, относительной простотой смесеобразования и пр.
К альтернативным топливам относят все виды топлив, для получения которых в качестве основного сырья не использована природная нефть.
Если смесь нефтяного и альтернативного топлив обладает достаточной физико-химической стабильностью при заданных эксплуатационных условиях, то такое топливо можно рассматривать как нефтяное топливо, в которое введены определенные добавки. В противном случае либо если это рационально по другим техникоэксплуатационным показателям, нефтяное и альтернативное топливо применяют как топлива раздельной подачи. Как показывает само название, под топливами раздельной подачи понимают двух- или более компонентные топлива, отдельные компоненты которых хранят на борту автомобиля раздельно. Смешиваются эти компоненты непосредственно во впускном тракте или в цилиндре двигателя. Применяют топлива раздельной подачи в случае физико-химической нестабильности компонентов при их предварительном смешении, а также при необходимости (или целесообразности) раздельного регулирования расхода отдельных компонентов. Например, для облегчения запуска холодного газового двигателя может использоваться нефтяное топливо, а для увеличения детонационной стойкости бензина на определенных режимах работы двигателя—добавка высокоактивных компонентов только на ЭТИХ режимах и т.п. Недостатком топлив раздельной подачи является усложнение конструкции, вызываемое наличием автономных систем хранения, подачи и регулирования каждого из компонентов топлива.
§ 2.2. Состав нефтяных топлив
Свойства топлив в определяющей степени зависят oт фракционного, элементного и группового составов входящих в них углеводородов, а также наличия и в топливах некоторых примесей.

Элементный состав топлива определяется видом и количеством входящих в него химических элементов. Для нефтяных топлив он в основном характеризуется элементным составом исходного сырья — нефти. От элементного состава зависят энергетические свойства топлива, которые оценивают его теплотой сгорания. Теплота сгорания водорода равна 120 МДж/кг, углерода — 33 МДж/кг. Отсюда, чем больше относительная масса водорода, содержащегося в топливе, тем выше его массовая теплота сгорания. Соответственно алканы (СnН2n+2) имеют большую теплоту сгорания (44 МДж/кг), чем нафтеновые (СnН2n) углеводороды (41 МДж/кг), а метан (СН4), содержащий наибольшую относительную массу водорода, обладает соответственно наибольшей теплотой сгорания (49 МДж/кг) среди всех углеводородных топлив.
Фракционный состав (ФС) топлива характеризуется количеством (в процентах по объему) содержащихся в нем отдельных фракций. ФС определяют путем перегонки топлива в специальном приборе (рис. 2.1). При перегонке фиксируют температуры начала кипения, пере гонки 10, 50 и 90 или 96 % (об.) топлива, а также конца кипения. Соответствующие температуры обозначают индексами  ,
, 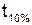 ,
,  ,
, 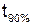 ,
,  и
и  .
.
За температуру  принимают температуру пара, соответствующую падению в холодильник первой капли конденсата. За температуру
принимают температуру пара, соответствующую падению в холодильник первой капли конденсата. За температуру  бензина принимают ту максимальную температуру, при которой ртутный столбик термометра останавливается на некоторой высоте, а после этого начинает опускаться. За
бензина принимают ту максимальную температуру, при которой ртутный столбик термометра останавливается на некоторой высоте, а после этого начинает опускаться. За  дизельных топлив принимают температуру 96 % выкипания. После конца кипения остается невыкипевший остаток— остаток в колбе. При оценке фракционного топлива по
дизельных топлив принимают температуру 96 % выкипания. После конца кипения остается невыкипевший остаток— остаток в колбе. При оценке фракционного топлива по  судят о присутствии наиболее легкокипящих фракций, по
судят о присутствии наиболее легкокипящих фракций, по 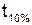 — об их количественном содержании, по
— об их количественном содержании, по  — о средней испаряемости топлива и по
— о средней испаряемости топлива и по 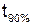 (или
(или  ), а также по
), а также по  — о содержании высококипящих фракции. Среднеобъемнаятемпература кипения топлива —
— о содержании высококипящих фракции. Среднеобъемнаятемпература кипения топлива —  рассчитывается по зависимости
рассчитывается по зависимости
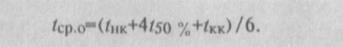
По полученным данным строят кривую перегонки (разгонки) топлива (рис. 2.2), которая в целом может быть охарактеризована углом наклонав градусах на 1 % (об.) разгонки:
O = (t90% - t10%)/80.
 При перегонке бензинов невозможно определить количество наиболее легкокипящих фракций, присутствие которых влияет на эксплуатационные свойства топлива, поэтому в нормативные требования к бензинам вводят контрольный параметр — давление насыщенных паров при температуре +38 °С. По температурам перегонки можно косвенно судить о давлении насыщенных паров — чем ниже
При перегонке бензинов невозможно определить количество наиболее легкокипящих фракций, присутствие которых влияет на эксплуатационные свойства топлива, поэтому в нормативные требования к бензинам вводят контрольный параметр — давление насыщенных паров при температуре +38 °С. По температурам перегонки можно косвенно судить о давлении насыщенных паров — чем ниже  и
и 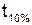 , тем выше давление насыщенных паров.
, тем выше давление насыщенных паров.
Групповой состав топлива определяется группами (классами) входящих в него углеводородов. В общем случае в состав топлива входят углеводороды, присутствующие в нефти (алканы, цикланы, ароматические углеводороды), могут находиться химически нестабильные непредельные углеводороды (олефины и диолефины), которые отсутствуют в природной нефти и образуются при химической переработке нефтепродуктов (например, при крекинге).
Большое влияние на качество топлива оказывают перешедшие в него из нефти некоторые гетероорганические соединения, вода и механические примеси. Вследствие относительно большой молярной массы и соответственно высоких температур кипения присутствие гетероорганических соединений характерно для дизельных топлив — это сернистые соединения, органические кислоты и смолисто-асфальтовые вещества. Влияние отдельных гетероорганических соединений изложено ниже при рассмотрении конкретных свойств топлив.
По техническим условиям наличие в топливе воды не допускается. Вода в значительной степени ухудшает ряд его эксплуатационных свойств (повышает коррозионную агрессивность и склонность к образованию отложений, ухудшает химическую стабильность, смазывающие и противоизносные свойства и пр.).
Кристаллы льда, образующиеся при замерзании воды, забивают трубопроводы и фильтры системы топливоподачи, уменьшая количество топлива, подаваемого в двигатель (рис. 2.3). Отложения кристаллов льда в жиклерах нарушают работу топливодозирующих устройств.
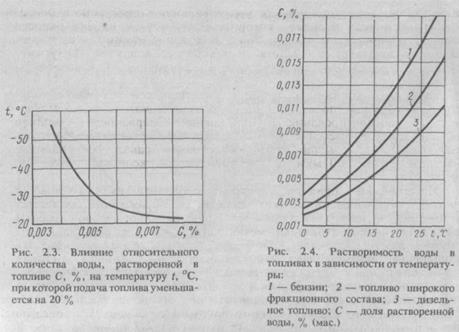
С некоторыми видами углеводородов, входящих в состав нефтяных топлив, вода при отрицательных температурах может образовывать ассоциированные комплексы. Объем образующейся при этом кристаллической массы увеличивается более чем в 2 раза. Вода попадает в топливо при его хранении, перевозке, заправке и эксплуатации автомобиля (отмечено, что практически полностью обезвоженное топливо при хранении быстро насыщается водой). При обычных условиях содержание воды в топливе по абсолютной величине не превышает 0,03% (маc.) при 20°С и изменяется при изменении атмосферных условий (влажности, температуры, давления).
Топливо соприкасается с водой вследствие конденсации ее паров из атмосферного воздуха на стенках топливных баков и поверхности жидкости в баке. Пары воды насыщают массу топлива вследствие диффузии. Способность вещества поглощать воду называется гигроскопичностью. С повышением температуры топлива (рис. 2.4), снижением относительной влажности воздуха и давления гигроскопичность топлива уменьшается. При изменении условий часть растворенной воды выделяется из топлива в виде эмульсии. Эмульсия может расслаиваться с образованием слоя воды в свободном состоянии. Эти три состояния (раствор, эмульсия, свободное состояние) могут переходить друг в друга при изменении метеорологических и эксплуатационных условий. Образование эмульсии облегчается, а ее устойчивость увеличивается в присутствии поверхностно-активных веществ, которые, адсорбируясь на поверхности капель, препятствуют их слиянию. В топливе такими веществами являются нафтеновые кислоты и смолистые вещества. С утяжелением фракционного состава топлива растворимость в нем воды уменьшается.
Основным источником механических примесей в топливе является атмосферная (почвенная) пыль. В зависимости от условий хранения, транспортирования и применения содержание в топливе механических примесей может достигать 400 г/т (в особо запыленных районах). Размеры частиц в основном равны 10 — 60 мкм. Частицы менее 60 мкм в топливе невооруженным глазом не различимы.
Механические примеси ухудшают прокачиваемость топлива в системе топливоподачи, служат основой для образования смолистых отложений и нагара, ведущих к нарушению нормальной работы двигателя, интенсифицируют механический износ и коррозию конструкционных материалов. Особенно большой вред наносят механические примеси системам топливоподачи дизелей, вызывая повышенный износ прецизионных пар топливного насоса и форсунок, потерю герметичности форсунок, подтекание топлива в цилиндр двигателя, засорение и эррозионный износ отверстий распылителей. В соответствии со статистическими данными от 30 до 95 % отказов дизелей в эксплуатации происходит из-за системы топливоподачи. В стандарты на дизельные топлива введен показатель, характеризующий наличие в топливе загрязнений (механических примесей, воды, натриевых мыл, нафтеновых кислот и смол) — коэффициент фильтруемости Кф. Этот коэффициент определяют по степени загрязнения (забивки) стандартного бумажного фильтра при протекании через него топлива. Большие значения Кф соответствуют наличию большего количества загрязнений.
§ 2.3. Горючая смесь
Количество воздуха l0 в горючей смеси, теоретически необходимое для полного сгорания 1 кг топлива, называют стехиометрическим. Величина l0 [кг/кг топлива] может быть рассчитана по уравнению
 (2.1)
(2.1)
где H, С и О—содержание в топливе в % (мас.) водорода, углерода и кислорода соответственно.
Из этого уравнения следует, что величина l0 зависит от элементного (чем больше доля водорода, тем больше l0) и от группового состава топлива. Потому значения l0 для топлив, имеющих различный состав, могут отличаться друг от друга. Значения l0 для некоторых топлив даны в табл. 2.1.
Таблица 2.1
| Топливо | Низшая теплота сгорания, кДж/кг | Стехиометрическое количество воздуха l0, кг/кг топлива | |
| топлива | горючей смеси | ||
| Авиабензин | 14,9 | ||
| Автобензин | 14,8 | ||
| Дизельное топливо | 15,0 | ||
| Этиловый спирт (этанол) | 9,0 | ||
| Метиловый спирт (метанол) | 6,5 | ||
| Бензол | 13,3 | ||
| Метан | 17,23 | ||
| Бутан | 15,6 | ||
| Пропан | 15,7 | ||
| Водород | 27,7 |
Количество действительно потребляемого воздуха l может отличаться от стехиометрического. Отношение действительного количества воздуха к стехиометрическому называют коэффициентом избытка воздуха а
а = l/lо. (2.2)
Горючую смесь, имеющую а < 1, называют богатой; смесь, имеющую а > 1,— бедной. Соответственно при уменьшении происходит обогащение, а при увеличении а — обеднение смеси.
 От величины а зависят скорость сгорания рабочей смеси и количество выделяющейся при этом теплоты. Из рис. 2.5 следует, что при значительном увеличении или уменьшении а скорость сгорания снижается, что в предельном случае может привести к прекращению горения смеси. Минимальную и максимальную концентрации топлива в смеси, при которых она может воспламеняться, называют концентрационными пределами воспламеняемости горючих смесей. Различают нижний и верхний концентрационные пределы, соответствующие предельным значениям обеднения и обогащения смеси, за которыми смесь не воспламеняется. Пределы воспламеняемости смеси зависят от вида топлива, состава и физических параметров смеси (температуры и давления)и характеристик источника воспламенения. Разность между нижним и верхним пределами воспламеняемости называют диапазоном воспламеняемости.
От величины а зависят скорость сгорания рабочей смеси и количество выделяющейся при этом теплоты. Из рис. 2.5 следует, что при значительном увеличении или уменьшении а скорость сгорания снижается, что в предельном случае может привести к прекращению горения смеси. Минимальную и максимальную концентрации топлива в смеси, при которых она может воспламеняться, называют концентрационными пределами воспламеняемости горючих смесей. Различают нижний и верхний концентрационные пределы, соответствующие предельным значениям обеднения и обогащения смеси, за которыми смесь не воспламеняется. Пределы воспламеняемости смеси зависят от вида топлива, состава и физических параметров смеси (температуры и давления)и характеристик источника воспламенения. Разность между нижним и верхним пределами воспламеняемости называют диапазоном воспламеняемости.
Наиболее широким диапазоном воспламеняемости обладает водород, что видно из приведенных ниже данных.
Таблица 2.2
| Топливо | Пределы воспламеняемости горючей смеси по a при р=0,1 МПа, Т=+20 С | |
| нижний | верхний | |
| Авиабензин | 1,13 | 0,675 |
| Автобензин | 1,10 | 0,650 |
| Дизельное топливо | 1,05 | 0,82 |
| Бензол | 1.11 | 0,798 |
| Оксид углерода | 1,95 | 0,57 |
| Водород | 8,7 | 0,32 |
Это, в частности, позволяет на двигателях, использующих водород в качестве топлива, применять качественный способ регулирования.
При увеличении температуры и давления горючей смеси диапазон воспламеняемости расширяется. Для устойчивой работы двигателя на различных режимах используемые топлива должны иметь возможно более широкий диапазон воспламеняемости. Особенно важно увеличить нижний предел воспламеняемости, определяющий возможность обеднения горючей смеси, а, следовательно, увеличения полноты сгорания и соответственно снижения расхода топлива и токсичности отработавших газов двигателя.
§ 2.4. Энергетические показатели топлив и горючих смесей
Теплотой сгорания топлива (ТСТ) называют количество тепловой энергии, выделяющейся при его полном сгорании. Различают высшую и низшую ТСТ. При определении высшей ТСТ QB учитывают теплоту, которая выделяется при конденсации воды, содержащейся в продуктах сгорания. Величину низшей ТСТ QH определяют без учета количества теплоты, выделяющейся при конденсации воды. В расчетах ДВС принимают значение Qн, так как пары воды в цилиндре не конденсируются. ТСТ, отнесенную к единице массы топлива, называют массовой, а отнесенную к единице объема топлива — объемной.
ТСТ определяют путем сжигания навески испытуемого топлива в калориметрической бомбе (при постоянном объеме) в среде сжатого кислорода, насыщенного водяным паром, и измерения количества выделяющейся теплоты. Некоторые значения ТСТ приведены в табл. 2.1.Для ориентировочных расчетовТСТ, кДж/кг, для нефтепродуктов можно определить по формулам, предложенным Д.И. Менделевым:

где С, Н, О и S — массовые доли соответствующих элементов в топливе (C + H + O + S=1); W —количество паров воды в продуктах сгорания 1 кг топлива.
Теплоту сгорания горючей смеси Hсм, кДж/кг, рассчитывают по уравнению

Это уравнение справедливо лишь при а > 1, так как при а < 1 часть топлива не сгорает и его теплота сгорания не реализуется.
Из табл. 2.1 следует, что теплоты сгорания горючих смесей на основе углеводородных топлив близки и что для сгорания топлив, обладающих большей теплотой сгорания, нужно большее количество воздуха. Это практически уравнивает энергетические возможности углеводородных топлив. Изложенное свидетельствует об ограниченной возможности повышения параметров ДВС путем увеличения энергетических свойств углеводородных топлив. В этом направлении решение лежит в использовании неорганических топлив и внедрении добавок к органическим топливам в виде веществ с более высокой теплотой сгорания.
Мощность, развиваемая поршневым ДВС, пропорциональна количеству теплоты, выделившейся в единице объема цилиндра, Hц,  . Величина Hц может отличаться от объемной теплоты сгорания горючей смеси Нсм,
. Величина Hц может отличаться от объемной теплоты сгорания горючей смеси Нсм,  , вычисляемой по формуле Нсм = =Нсм^3р, где р — плотность гомогенной топливовоздушной смеси,
, вычисляемой по формуле Нсм = =Нсм^3р, где р — плотность гомогенной топливовоздушной смеси, 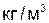 . Это объясняется различным агрегатным состоянием, в котором топливо может находиться после завершения такта выпуска (пар, пар + жидкость, жидкость), и соответственно разной долей объема цилиндра, занимаемой топливом. Рассмотрим изложенное более подробно. В конце такта впуска рабочий объем цилиндра Vh условно можно представить как сумму объемов, занятых воздухом — Vв, жидким топливом — V ж и парами топлива — V п:
. Это объясняется различным агрегатным состоянием, в котором топливо может находиться после завершения такта выпуска (пар, пар + жидкость, жидкость), и соответственно разной долей объема цилиндра, занимаемой топливом. Рассмотрим изложенное более подробно. В конце такта впуска рабочий объем цилиндра Vh условно можно представить как сумму объемов, занятых воздухом — Vв, жидким топливом — V ж и парами топлива — V п:

Слагаемые уравнения (2.6) определяются из соотношений:



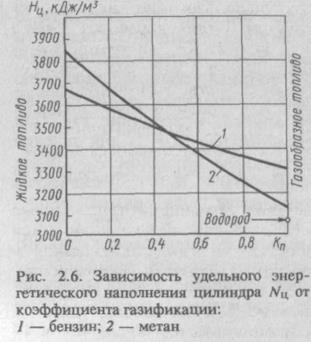
где a — коэффициент избытка воздуха; l0 — стехиометрическое количество воздуха, кг/кг; mт — масса топлива, поступившего в цилиндр, кг;  ,
,  ,
,  — плотность воздуха, жидкого топлива и паров топлива (газообразного топлива),
— плотность воздуха, жидкого топлива и паров топлива (газообразного топлива), 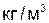 , соответственно;
, соответственно;  — коэффициент газификации топлива, равный отношению количества паров топлива (газообразного топлива) mп, кг, поступившего в цилиндр к концу такта впуска, к величине mт. Для двигателя, работающего на газообразном топливе, Kп = 1; для дизелей и бензиновых двигателей с непосредственным впрыском Кп = 0; для двигателей с внешним смесеобразованием 0< Кп<1. Количество теплоты, выделившейся в объеме цилиндра Нц, Дж, равно
— коэффициент газификации топлива, равный отношению количества паров топлива (газообразного топлива) mп, кг, поступившего в цилиндр к концу такта впуска, к величине mт. Для двигателя, работающего на газообразном топливе, Kп = 1; для дизелей и бензиновых двигателей с непосредственным впрыском Кп = 0; для двигателей с внешним смесеобразованием 0< Кп<1. Количество теплоты, выделившейся в объеме цилиндра Нц, Дж, равно

и количество теплоты, выделившейся в единице объема цилиндра (удельное энергетическое наполнение цилиндра), с учетом (2.6) — (2.10) определится из соотношения

Уравнение (2.11) позволяет в первом приближении, при прочих равных условиях, оценить сравнительное влияние на мощность, развиваемую двигателем, отдельных свойств топлива:
его элементного и группового составов (через Qн и lо),
агрегатного состояния (через Кп),
а также влияние метода регулирования двигателя (качественное по а; количественное по  ), величины наддува (по
), величины наддува (по  ) и совершенствование внешнего смесеобразования (по изменению Кп).
) и совершенствование внешнего смесеобразования (по изменению Кп).
При расчетах величиной  можно пренебречь, так как
можно пренебречь, так как  . Из анализа уравнения (2.11), в частности, следует: в сравнении с бензиновыми двигателями пониженная литровая мощность, развиваемая газовыми двигателями, объясняется величиной Кп=1 и низкими значениями QH; уменьшение литровой мощности дизелей — более высокими значениями а. Влияние совершенствования внешнего смесеобразования (изменения Кп) на Нц возрастает при уменьшении и и lо, поэтому, в частности, при использовании спиртов, имеющих относительно низкие значения lо, повышение доли топлива, испарившейся во впускном тракте двигателя, вызывает большую относительную потерю мощности, чем при использовании бензинов (рис. 2.6).
. Из анализа уравнения (2.11), в частности, следует: в сравнении с бензиновыми двигателями пониженная литровая мощность, развиваемая газовыми двигателями, объясняется величиной Кп=1 и низкими значениями QH; уменьшение литровой мощности дизелей — более высокими значениями а. Влияние совершенствования внешнего смесеобразования (изменения Кп) на Нц возрастает при уменьшении и и lо, поэтому, в частности, при использовании спиртов, имеющих относительно низкие значения lо, повышение доли топлива, испарившейся во впускном тракте двигателя, вызывает большую относительную потерю мощности, чем при использовании бензинов (рис. 2.6).
 Эффективность наддува увеличивается при снижении а в зависимости от отношения
Эффективность наддува увеличивается при снижении а в зависимости от отношения  . Например, одних и тех же результатов можно добиться снижением а или увеличением
. Например, одних и тех же результатов можно добиться снижением а или увеличением  (повышение давления наддува), поэтому в бензиновых двигателях, работающих при более низких значениях
(повышение давления наддува), поэтому в бензиновых двигателях, работающих при более низких значениях  , введение наддува сказывается сильнее, чем в дизелях. Расчет по (2.11) показывает, что (при
, введение наддува сказывается сильнее, чем в дизелях. Расчет по (2.11) показывает, что (при  и приведении плотности газов к нормальным условиям 0°С и 101,325 кПа) удельное энергетическое наполнение цилиндра при работе на бензине, метане и водороде равно соответственно 3666, 3847 и 3093 кДж/м3, что составляет (принимая бензин за 100%) соответственно 100, 105 и 84 % (несмотря на в 3 раза большую массовую теплоту сгорания водорода, использование его в качестве топлива обусловливает потерю не менее 15 % мощности). Из графика рис. 2.6 следует, что совершенствование внешнего смесеобразования двигателя путем увеличения полноты испарения топлива во впускном тракте (увеличения Кп до Кп=1) приведет к уменьшению энергетического наполнения цилиндров на 10 и 20 % при работе на бензине и метаноле соответственно. При одном и том же значении
и приведении плотности газов к нормальным условиям 0°С и 101,325 кПа) удельное энергетическое наполнение цилиндра при работе на бензине, метане и водороде равно соответственно 3666, 3847 и 3093 кДж/м3, что составляет (принимая бензин за 100%) соответственно 100, 105 и 84 % (несмотря на в 3 раза большую массовую теплоту сгорания водорода, использование его в качестве топлива обусловливает потерю не менее 15 % мощности). Из графика рис. 2.6 следует, что совершенствование внешнего смесеобразования двигателя путем увеличения полноты испарения топлива во впускном тракте (увеличения Кп до Кп=1) приведет к уменьшению энергетического наполнения цилиндров на 10 и 20 % при работе на бензине и метаноле соответственно. При одном и том же значении  двигатели с непосредственным впрыском топлива в цилиндр (Кп=0) развивают мощность большую, чем двигатели с внешним смесеобразованием (Кп > 0). Уравнение (2.11) позволяет относительно просто оценить влияние изменения
двигатели с непосредственным впрыском топлива в цилиндр (Кп=0) развивают мощность большую, чем двигатели с внешним смесеобразованием (Кп > 0). Уравнение (2.11) позволяет относительно просто оценить влияние изменения  на мощностные показатели двигателя. Например, принимая нижний концентрационный диапазон воспламеняемости смеси, равный 1,15 для бензина и 8 для водорода, получаем диапазон регулирования мощности по качеству смеси, равный 18 и 57 % соответственно.
на мощностные показатели двигателя. Например, принимая нижний концентрационный диапазон воспламеняемости смеси, равный 1,15 для бензина и 8 для водорода, получаем диапазон регулирования мощности по качеству смеси, равный 18 и 57 % соответственно.
§ 2.5. Альтернативные топлива
В связи с большим значением альтернативных топлив для транспортной энергетики будущего целесообразно более подробное рассмотрение некоторых видов этих топлив и методов их получения.
По производственным и эксплуатационным показателям альтернативные топлива можно разделять на две основные группы.
К первой группе относятся топлива, достаточно близкие к нефтяным по происхождению, физико-химическим и эксплуатационным свойствам. Такие топлива получают переработкой углеродсодержащих природных и промышленных веществ (угля, битуминозных песков, горючих нефтяных сланцев, природного и промышленного горючих газов и т.п.) — из альтернативных энергоресурсов. Получаемые в результате переработки жидкие продукты в некоторых работах называют синтетической нефтью. Характерной особенностью топлив, получаемых из нее, является то, что их использование не требует значительных изменений в конструкции или доработок ДВС, рассчитанных на топлива из природной нефти.
Ко второй группе относятся топлива, существенно отличающиеся как по физико-химическим, так и по эксплуатационным свойствам от нефтяных. К этой группе относят спирты, нефтяной и природный газы, водород, аммиак и некоторые другие энергоносители. К альтернативным условно относят также газоконденсатные топлива, являющиеся продуктом нефтяного происхождения, но не получаемые из нефти в процессе ее переработки.
Альтернативные энергоносители имеют большие потенциальные возможности, освоение которых практически еще только начинается (например, при сегодняшних потребностях энергии, заключенной в нефтяных сланцах и битуминозных песках, хватило бы человечеству более чем на 1000 лет).
Уголь. Установленные запасы угля на земном шаре в десятки раз превышают запасы нефти и газа и оцениваются более чем в 14 трлн.т. Около 25 % разведанных запасов угля в СССР сосредоточено в Сибири, в Канско-Ачинском бассейне.
Энергетической программой предусмотрена крупномасштабная комплексная переработка углей Канско-Ачинского месторождения с получением компонентов моторных топлив, аммиака, метанола и водорода. При решении проблемы использования угля в качестве энергоисточника для транспортных двигателей основная задача состоит в создании экономически рентабельных способов его переработки в жидкое топливо, сопоставимое по своим качественным показателям с нефтью. Различают два современных способа превращения угля в жидкое углеводородное топливо (синтетическую нефть): путем сжижения угольной массы и с предварительной газификацией угля.
Физическая основа первого способа основана на том, что агрегатное состояние углеводородных соединений зависит от количества в молекуле атомов водорода, приходящихся на один атом углерода,— чем их больше, тем при более низких температурах углеводороды становятся жидкими. Соответственно техническая реализация этого способа заключается в насыщении углеводородных компонентов угля водородом — в деструктивном гидрировании. В этом процессе измельченную угольную массу в смеси с жидкостью, выделяемой из конечного продукта гидрирования, подвергают действию высоких температур и давлений в атмосфере водорода в присутствии катализатора. При этом молекулярные связи исходных тяжелых углеводородов разрываются (происходит их деструкция) с образованием молекул с меньшей молярной массой и насыщением свободных молекулярных связей водородом. После вторичной переработки и очистки получают жидкие топлива, соответствующие по качеству современным требованиям к нефтяным топливам.
Первая установка по производству синтетической нефти из угля путем его гидрирования была создана в 1923 г. Во время второй мировой войны в Германии работало 12 заводов общей мощностью 2 млн. т бензина, 800 тыс. т дизельного топлива и 35 тыс. т смазочных материалов в год. Процесс проводился в громоздких установках при высоких давлениях и температурах (70 МПа, 180 С).
Работы по совершенствованию методов гидрирования угля ведутся в СССР в Институте горючих ископаемых. Разработанная в СССР технология дает до 45 % жидкого горючего от массы израсходованного угля при соотношении бензин: дизельное топливо от 1: 3 до 1: 5.
Другой промышленный способ получения синтетической нефти основан на окислении угля в присутствии воды с последующим гидрированием полученных продуктов. Схему протекания реакций можно представить следующим образом:
1. Исходный продукт окисляется водяным паром С + Н2О à СО + Н2.
2. Образовавшийся оксид углерода и водород очищают и смешивают с водородом до получения смеси, содержащей 1 часть СО на 2,0 — 2,5 части Н2.
3. Смесь газов подвергается обработке (t = 170 - 210 °С; Р - 1,0 МПа) на кобальтовом катализаторе. Получают жидкие и газообразные вещества. Жидкие продукты представляют собой одну из форм синтетической нефти (выход нефти до 650 кг из 1т угля). Из газообразных продуктов выделяют пропан-бутановую фракцию, используемую для изготовления сжиженных горючих газов. Этим способом синтетическая нефть может быть получена практически из любых углеродсодержащих веществ. Например, при эндотермической реакции воды с метаном
СН4 + Н2О à СО + ЗН2
получают газ с соотношением СО и Н2, близким к оптимальному, и далее по описанной выше схеме.
Большие ресурсы оксида углерода для получения синтетической нефти заключены в попутных газах металлургических производств (доменного, кислородно-конверторного, ферросплавного и др.). Расчеты показывают, что использование только этих ресурсов достаточно для удовлетворения до 20 % потребности страны в автомобильном бензине.
Однако массовое использование топлив, полученных из угля, станет экономически целесообразным лишь после завершения всех работ по созданию высококачественных катализаторов, промышленной технологии и строительства соответствующих предприятий.
В нашей стране разработан один из наиболее экологически чистых способов производства углеводородов. По этому способу из атмосферы выделяют углекислый газ, который разлагают на оксид углерода и кислород. Для этого требуются большие затраты энергии, которую можно выработать, например, в атомных реакторах. Затем оксид углерода соединяют с водородом и получают группы углеводородов, входящих в состав синтетической нефти (рис. 2.7).

Для получения синтетической нефти и горючих газов из угля и твердых углеводородных веществ применяют также процессы полукоксования и коксования.
Полукоксование (или низкотемпературное коксование) заключается в нагреве сырья в печах без доступа воздуха (для угля температура нагрева 500 — 600 °С). В результате полукоксования получают: полукокс — твердое топливо, из которого удалены значительная часть летучих компонентов и влага; первичную смолу (смолу полукоксования) — жидкие продукты, сконденсированные путем охлаждения выделяющихся летучих веществ; газы полукоксования — газообразные продукты, несконденсировавшиеся при охлаждении летучих веществ. Эти газы состоят в основном из метана, в меньшем количестве они содержат непредельные углеводороды, примеси СО, СО2, H2S и др.
Коксование. При увеличении температуры выше температуры полукоксования (для угля до 750— 1200°С) расщепление сырья углубляется, в результат чего уменьшается количество выделяющихся смол и увеличивается количество газа.
Горючие газы. Основными компонентами горючих газов являются низкокипящие углеводороды (см. табл. 4.7). Сырьевой базой для получения этих веществ служит природный газ, нефтяные газы, a также газы, получаемые при нефтепереработке, доменные газы и биогаз.
Наибольшее значение для промышленности ТиС имеет приходный газ, который получают из газовых или и газоконденсатных месторождений. В залежах нефти также присутствует природный газ.

В зависимости от месторождения природный газ содержит от 92 до 98 % метана (CH4) с примесями других, в том числе и более тяжелых углеводородов, диоксида углерода, сероводорода (содержание которого в газе некоторых месторождений достигает 20 %), гелия (получение гелия из природного газа имеет промышленное значение).
После относительно несложной очистки природный газ может быть непосредственно использован в качестве моторного топлива. Освоены технологии массового получения из природного газа жидких моторных топлив, метилового спирта (распространенное промышленное название — метанол), водорода и других ценных химических продуктов. Мировые запасы метана в природных газах оценивают в 250 трлн. м3.
В качестве источника горючего газа на основе метана может рассматриваться биогаз, представляющий собой смесь метана (до 80 %) с углекислым и некоторыми другими газами. Биогаз получают биотехнологическими методами практически из любых органических веществ (в том числе отходов) с помощью термофильных, метано-образующих бактерий. Процесс преобразования, называемый биоконверсией или анаэробной ферментацией, проходит в специальных емкостях — метатенках, в которые подается теплота, вода и органические отходы (рис. 2.8). В результате получают биогаз (0,3 — 0,7 м3 из 1 кг сухого органического вещества), содержащий до 70% метана, и шлам, являющийся высокоэффективным азотно-фосфорным удобрением (1 т такого шлама эквиваленты 2 —4 т промышленных удобрений). Биогаз очищают от примесей с целью увеличения содержания метана и используют в качестве моторного топлива наравне с природным газом. В ряде городов действуют промышленные установки по производству биогаза из промышленных отходов и жидких коммунальных стоков.
Перспективные ресурсы метана, намного превосходящие запасы природного газа, сосредоточены в метановом гидрате — веществе, имеющем консистенцию льда и состоящем из молекул метана, заключенных в трехмерной решетке молекул воды. Это вещество стабильно при достаточно высоких давлениях и минимальных положительных температурах, поэтому его месторождения сосредоточены на дне морей и океанов. Под залежами гидратов расположен газообразный метан. По предварительным оценкам такие метановые залежи содержат около 1 млн. км газа. Другим перспективным источником метана является газ угольных месторождений (рудничный газ). Только в Донецком и Карагандинском каменноугольных месторождениях запасы метана оценивают в 80 км.
Все углеводородные горючие газы (как природный, так и промышленный и биогаз) могут быть использованы для получения синтетической нефти.
Распространенными процессами, используемыми для переработки газообразных углеводородов в жидкие, являются ал копирование и полимеризация. Реакция алкилирования заключается в присоединении олефинового углеводорода к парафиновому или ароматическому с образованием насыщенной молекулы большей молярной массы. В результате алкилирования получают алкилат, являющийся высококачественным компонентом бензинов.
Реакция полимеризации заключается в соединении двух или большего числа одинаковых молекул. В реакции полимеризации способны участвовать только непредельные углеводороды. В природном горючем газе такие углеводороды отсутствуют, поэтому сырьем для полимеризации являются промышленные горючие газы, богатые непредельными углеводородами. Полимеризация производится при температуре 180 — 200°С и давлении 20 — 30 МПа в присутствии катализатора.
Большие потенциальные энергетические ресурсы заключены в горючих сланцах и битуминозных песках. В 1 т сланцев содержатся 80— 100 кг органических веществ (встречаются месторождения, содержащие до 300 кг таких веществ).
Жидкое синтетическое топливо из сланцев получают путем их нагрева без доступа воздуха при температурах 500 — 550 °С. Выделяющаяся при этом сланцевая смола подвергается перегонке для отделения легких фракций, которые после гидрирования и очистки используют в качестве добавок к нефтяным топливам.
Огромные запасы нефтепродуктов в виде природного битума — вещества, состоящего из высокомолекулярных, преимущественно нафтеновых углеводородов, содержатся в битуминозных песках. Например, месторождения битуминозного песка в Азербайджане содержат до 150 кг нефти на 1 м3 песка.
Широкое использование промышленных методом получения синтетической нефти сдерживается относительно (по сравнению с нефтью) высокой стоимостью процессов переработки. Объем производства этих продуктов будет возрастать по мере постоянно проходящего изменения соотношения между производственными затратами и стоимостью природной нефти.
Реальной и практически осуществляемой заменой нефтяных топлив являются спирты — метиловый (метанол) и этиловый (этанол). Наибольшее внимание уделяется метанолу. Это объясняется большими масштабами его производства (мировое производство метанола достигло 180 млн. т и продолжает увеличиваться в перспективе до 200 млн. т к 2000 г.), освоенной крупномасштабной технологией (производительность отдельных агрегатов достигает 100 тыс. т в год) и разнообразием сырьевых источников. В качестве сырья для получения метанола могут быть использованы тяжелые нефтяные остатки (гудрон, битум), уголь, природный газ и пр. Метанол может быть использован в качестве основного топлива для ДВС, как добавка к нефтяному топливу и как сырье для производства синтетического высокооктанового бензина. Из метанола получают эффективную высокоактивную добавку к бензину: метил-трет-бутиловый эфир (МТБЭ).
Этанол по своим эксплуатационным характеристикам близок к метанолу, но производство его отличается большей энергоемкостью, что обусловливает более высокую его стоимость. В промышленности этанол получают путем гидратации этилена или биотехнологической переработкой органических продуктов. Возможно также получение этанола из метанола путем реакции его с оксидом углерода на катализаторе (СН3ОН + СО + 2Н2 -+ СН3СН2ОН + Н2О).
Биотехнологические методы переработки на этанол растительных веществ представляют особый интерес, так как позволяют получать альтернативные топлива из восстанавливаемых природных органических ресурсов — биомассы растений, побочных продуктов сельскохозяйственного производства и т.п.
Помимо отказа от использования природных горючих ископаемых такое решение дает возможность приблизиться к безотходной технологии, что имеет большое экологическое значение.
Наиболее распространенным источником сырья для биотехнологического получения этанола являются отходы от переработки растительных масс. Для удовлетворения растущего спроса на этанол культивируют специальные сельскохозяйственные растения. Основным препятствием в использовании такого способа являются ограничения по растительному сырью — посевные площади необходимы для удовлетворения продовольственных потребностей людей.
Как основной перспективный энергоноситель будущего рассматривают водород — экологически чистое топливо, обладающее неограниченными сырьевыми ресурсами. Наиболее распространенный современный промышленный способ получения водорода основан на частичном окислении метана и его конверсии с водяным паром:
2СН4 + О2 à 2СО + 4Н2;
СН4 + Н2О à СО + ЗН2.
Метан является ценным промышленным сырьем, поэтому предложены способы получения водорода из воды. К таким способам относят электролитическое (электролиз) и термическое (термолиз) разложение воды. Недостатком электролиза является относительно низкий КПД процесса. Несмотря на это, в дальнейшем роль электролиза возрастет в связи с удешевлением энергии АЭС и увеличением КПД электролизеров. Получение водорода с помощью электролиза нашло промышленное применение в ряде стран, обладающих дешевой гидроэнергией (Норвегия, Канада).
Прямой термолиз (разложение под действием высокой температуры) воды неприемлем из-за высоких температур, при которых протекает реакция (3000 — 3500 °С). Разработаны имеющие практическое значение методы многоступенчатого термолиза с использованием промежуточных окислительно-восстановительных реакций, например двухступенчатый цикл термолиза воды. В первой ступени при относительно низкой температуре проходит реакция взаимодействия металла с водой. Продукты реакции — свободный водород и оксид металла. Во второй ступени при температурах (200 — 1300 °С) проходит восстановление оксида. Теплота для осуществления такого цикла может быть получена от атомного реактора. Подсчитано, что термоядерный реактор тепловой мощностью 10 млн. кВт при работе по такому циклу даст 1 млн.т водорода в год.
К преимуществам использования водорода в качестве энергоносителя относится также возможность аккумулирования больших его количеств в естественных и искусственных подземных резервуарах (выработанные месторождения нефти и газа, горные выработки, соляные каверны и пр.), что важно для согласования режимов выработки и потребления энергии. Водород можно транспортировать по трубопроводам.
Приближенные расчеты показывают, что капитальные и эксплуатационные расходы на транспортировку единицы энергии в виде водорода, благодаря его малой плотности и вязкости, сопоставимы с расходами по транспортировке природного паза и для расстояний свыше 1500 км примерно вдвое ниже, чем на передачу электроэнергии по воздушным линиям. В ФРГ и США действуют водородные трубопроводы протяженностью в несколько сотен километров. Дополнительное преимущество такого решения заключено и в том, что АЭС вырабатывают энергию непрерывно, при практически постоянном режиме, их регулирование или отключение невыгодно, а потребление электроэнергии переменно по времени суток, дням недели и погодным условиям. Необходимо аккумулировать образующуюся в этих случаях избыточную энергию. Возможное решение - использование этой энергии для производства промежуточных энергоносителей, например метанола, водорода, которые могут быть использованы и в качестве топлива для ДВС.
Контрольные вопросы
I. Почему в качестве топлива для ДВС не используют пиротехнические составы (например, порох)? 2. Для каких топлив угол наклона кривой фракционной разгонки равен 90°? 3. Как связан концентрационный диапазон воспламеняемости горючей смеси с топливной экономичностью двигателя? 4. Почему использование газообразных топлив увеличивает долговечность цилиндро-поршневой группы? 5. Как нужно изменить рабочий процесс поршневого двигателя, чтобы можно было полезно использовать разность между высшей и низшей теплотами сгорания топлива? 6. Теплота сгорания этанола меньше, чем бензина (см. табл. 2.1), однако иногда этанол используют в качестве топлива на спортивных автомобилях. Почему?
ГЛАВА 3. СВОЙСТВА ТОПЛИВ
Топлива, применяемые для ДВС, должны в наибольшей степени удовлетворять оптимальным условиям протекания рабочего процесса и эксплуатации двигателя. Наряду с этим топлива должны быть обеспечены широкой сырьевой базой и не требовать сложных и дорогостоящих процессов при их изготовлении. Сочетание этих условий определяет комплекс требований к свойствам топлив.
§ 3.1. Испаряемость топлив
Испаряемость топлива (ИТ) характеризуется скоростью перехода его из жидкой фазы в пар. ИТ является важнейшим показателем, в значительной степени определяющим процессы смесеобразования и сгорания рабочей смеси в двигателе. ИТ оказывает комплексное влияние на безотказность, долговечность, токсичность отработавших газов и другие показатели, связанные с химмотологической надежностью двигателя. Испаряемость зависит от ряда свойств топлива, в первую очередь от фракционного состава и давления насыпанных паров. Соответственно ИТ количественно оценивают по кривой разгонки с характерными температурными точками и давлению насыщенных паров при температуре 38°С (для бензинов).
ИТ зависит от внешних и внутренних факторов. К внешним относятся: теплообмен с окружающей средой, скорость движения газа относительно капли (пленки) концентрация паров топлива вокруг жидкого топлива и скорость диффузии парой в окружающее пространство; к внутренним — температура капли и влияющие на испаряемость физические параметры топлива; давление насыщенных паров, теплоемкость, теплопроводность, теплота парообразования и температуры кипения компонентов, входящих в состав топлива (для нефтяных топлив — фракционный считан). На ИТ оказывают большое влияние конкретные условия, зависящие от конструкции и эксплуатационных особенностей работы двигателя. Например, под влиянием вибраций испаряемость может увеличиваться в 4 раза и более.
ИТ характеризуется скоростью испарения — количеством пара, образующегося с единицы поверхности жидкости в единицу времени. Скорость испарения топлива dmT/dr при прочих равных условиях определяется скоростью подвода теплоты dQ/dτ к его поверхности: dm/dτ ~ dQ/dτ. Для конвективного теплообмена между топливом и газом величина dQ/dτ определяется уравнением Ньютона

где  — коэффициент теплопередачи от газа к топливу; SТ — поверхность топлива, омываемая газом; Tг и Тт — соответственно температуры газа и топлива.
— коэффициент теплопередачи от газа к топливу; SТ — поверхность топлива, омываемая газом; Tг и Тт — соответственно температуры газа и топлива.
Полагая, что вся теплота, подводимая к топливу, расходуется только на его испарение (так как теплоемкость топлива значительно меньше теплоты парообразования, см. табл. 3.1), получим  , где у — теплота парообразования. Тогда (3.1) примет вид
, где у — теплота парообразования. Тогда (3.1) примет вид

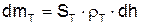 , где dh — уменьшение толщины слоя топлива по нормали к его поверхности; pТ — плотность топлива.
, где dh — уменьшение толщины слоя топлива по нормали к его поверхности; pТ — плотность топлива.
Таблица 3.1
| Топливо | Теплота парообразования, кДж/кг | Теплоемкость, кДж/(кг°С) | Понижение температуры смеси при полном испарении топлива, °С |
| Этиловый спирт | 919,0 | 2,39 | 80,4 |
| Метиловый спирт | 1102,8 | 2,43 | 123,1 |
| Бензин: | |||
| А-76 | 297,3 | 2,09 | 17,7 |
| АИ-93 | 305,6 | 1,97 | 18,8 |
| Дизельное топливо | 210,0 | 1,88 | 18,2 |
| Бензол | 381,0 | 1,67 | 26,4 |
Соответственно (3.2) можно представить в виде

Выражение (3.3) является уравнением теплового баланса при испарении топлива. Вводя в него конкретные граничные условия, можно получить зависимости для различных частных случаев. Например, для испарения капельно-жидкого топлива при относительно малых диаметрах капли dK величину аТ можно определить из эмпирического уравнения

При dK à 0 справедливо Re à 0. Тогда в соответствии с (3.4) Nu =2. Учитывая, что  , получаем:
, получаем:

где λ — коэффициент теплопроводности; тогда уравнение (3.3) примет вид

Решая (3.6) относительно т, получаем уравнение для определения времени испарения капли

Из (3.7) следует, что время испарения капли линейно зависит от плотности топлива и пропорционально квадрату ее диаметра. Скорость испарения  определяется уравнением
определяется уравнением

где ps p n и ро — соответственно давление насыщенных паров топлива при температуре насыщения, парциальное давление паров топлива и парциальное давление воздуха в среде, в которую происходит испарение; D — коэффициент диффузии; К - коэффициент пропорциональности.
Из (3.8) следует, что скорость испарения определяется двумя основными характеристиками: коэффициентом диффузии и давлением насыщенных паров. Коэффициент диффузии D определяет скорость, с которой пары топлива проникают (диффундируют) в воздух. В общем случае значение D увеличивается с ростом температуры и снижением давления среды, в которую происходит диффузия, в соответствии с уравнением

где То, po, Do — соответственно исходные температура, давление и коэффициент диффузии; р и T—заданные условия.
При увеличении скорости движения воздуха v относительно поверхности топлива величина D возрастает пропорционально  . Различают молекулярную и турбулентную (конвективную) диффузию паров топлива. При молекулярной — перенос вещества осуществляется за счет различия в его концентрациях в заданном объеме, а при турбулентной — за счет перемещения макроколичества молекул при турбулентных пульсациях среды. Определяющее влияние на условия переноса паров топлива в современных двигателях оказывает турбулентная диффузия, определяемая конструкцией и режимом работы двигателя, поэтому коэффициент диффузии можно использовать лишь для сравнительного анализа топлив.
. Различают молекулярную и турбулентную (конвективную) диффузию паров топлива. При молекулярной — перенос вещества осуществляется за счет различия в его концентрациях в заданном объеме, а при турбулентной — за счет перемещения макроколичества молекул при турбулентных пульсациях среды. Определяющее влияние на условия переноса паров топлива в современных двигателях оказывает турбулентная диффузия, определяемая конструкцией и режимом работы двигателя, поэтому коэффициент диффузии можно использовать лишь для сравнительного анализа топлив.

Давлением насыщенного пара называют давление пара в состоянии термодинамического равновесия с испаряющейся жидкостью. Давление насыщенных паров является индивидуальной характеристикой вещества, зависящей от ряда факторов, обусловливаемых влиянием внешней среды. К таким факторам относятся температура (рис. 3.1), соотношение между паровой и жидкой фазами (рис. 3.2), наличие в топливе растворенного газа и др. Зависимость давления насыщенных паров нефтяных топлив от отношения объемов паровой и жидкой фаз объясняется тем, что в первую очередь испаряются фракции топлива, обладающие наибольшим давлением насыщенных паров, и в оставшейся жидкой части увеличивается концентрация углеводородов с более низким давлением. Чем больше объем паровой фазы, тем сильнее влияние этого эффекта.
 Давление насыщенных паров определяется в лабораторном приборе (рис. 3.3), который состоит из двух соединенных друг с другом камер. В нижнюю камеру, имеющую объем в 4 раза меньший, чем у верхней, заливают исследуемый бензин. Прибор помещают в водяную баню, обеспечивающую поддержание заданной температуры, и замеряют давление паров бензина. Косвенно давление насыщенных паров можно охарактеризовать по фракционному составу топлива - чем больше в нем низкокипящих фракций (чем ниже tик и t10%), тем выше давление насыщенных паров топлива. При испарении первых порций топлива температура горючей смеси понижается. Понижение температуры Δt, вызываемое испарением топлива, определим из следующих условий. Для полного испарения 1 кг топлива нужно израсходовать Q единиц теплоты Q = γ, где γ — теплота парообразования. Теплота отнимается (при отсутствии теплопровода извне) от горючей смеси, обусловливая ее охлаждение от to до t1, т.е. Δt = to—t1; тогда
Давление насыщенных паров определяется в лабораторном приборе (рис. 3.3), который состоит из двух соединенных друг с другом камер. В нижнюю камеру, имеющую объем в 4 раза меньший, чем у верхней, заливают исследуемый бензин. Прибор помещают в водяную баню, обеспечивающую поддержание заданной температуры, и замеряют давление паров бензина. Косвенно давление насыщенных паров можно охарактеризовать по фракционному составу топлива - чем больше в нем низкокипящих фракций (чем ниже tик и t10%), тем выше давление насыщенных паров топлива. При испарении первых порций топлива температура горючей смеси понижается. Понижение температуры Δt, вызываемое испарением топлива, определим из следующих условий. Для полного испарения 1 кг топлива нужно израсходовать Q единиц теплоты Q = γ, где γ — теплота парообразования. Теплота отнимается (при отсутствии теплопровода извне) от горючей смеси, обусловливая ее охлаждение от to до t1, т.е. Δt = to—t1; тогда
γ = mCMCCM(to- t1), (3.10)
где mcм = 1 + alQ — масса смеси; Ссм — теплоемкость смеси.
Далее Ссм (1 + a lQ)= а10Св + СТ где Св и Ст — теплоемкости воздуха и топлива,
Ссм= (aloCB + Ст) / (1 +аl0). (3.11)
Подставляя значение mсм и Ссм в (3.10) и решая его относительно /, получаем
Δt = γ /(аl0Св + Ст). (3.12)
Из (3.12) следует, что с увеличением теплоты парообразования, уменьшением стехиометрического количества воздуха и коэффициента избытка воздуха температура понижается. Величины понижения температуры горючей смеси для некоторых топлив были приведены в табл. 3.1. В данном случае характерен пример метилового и этилового спиртов. Благодаря, главным образом, большой теплоте парообразования и малому стехиометрическому количеству воздуха температура при работе двигателя на спиртовоздушных смесях понижается в несколько раз больше, чем на бензовоздушных. В дизелях ИТ проходит при более благоприятных условиях (в первую очередь благодаря высокой температуре среды, в которую впрыскивается топливо), чем в двигателях с внешним смесеобразованием, поэтому ИТ в дизелях не играет такой важной, определяющей роли, как в бензиновых двигателях.
В двигателях с внешним смесеобразованием имеет место «низкотемпературное» смесеобразование, характеризующееся тем, что температура испаряющегося топлива не превышает температуры окружающей среды. Другими характерными особенностями смесеобразования в этих двигателях является нестационарное (пульсирующее) движение газового потока во впускном тракте, а также неидентичность газодинамических характеристик впускных трактов отдельных цилиндров (для карбюраторных двигателей с количеством карбюраторов меньше, чем число цилиндров).

Во впускном трубопроводе двигателя с внешним смесеобразованием происходит фракционирование топлива — испаряются низкокипящие компоненты, в результате чего на внутренних стенках впускного трубопровода образуется движущаяся с потоком газа пленка не испарившихся, наиболее высококипящих фракций топлива. Количество топлива в пленке возрастает с понижением его температуры (рис. 3.4), утяжелением фракционного состава, уменьшением скорости и турбулентности потока газа, а также под воздействием ряда других факторов. Наличие пленки неблагоприятно влияет на работу двигателя, снижая полноту сгорания топлива, и является причиной неравномерности распределения смеси в цилиндрах много цилиндрового двигателя. Скорость движения пленки по стенкам трубопровода меньше, чем скорость движения газа, что приводит к необходимости введения в конструкцию карбюратора устройства (ускорительного насоса), предназначенного для поддержания заданного качественного состава горючей смеси, поступающей в цилиндры двигателя при резком открытии дроссельной заслонки. Из-за наличия жидкой пленки и фракционирования топлива во впускном трубопроводе в отдельные цилиндры двигателя поступают заряды, отличающиеся по количеству топлива (т.е. по а, рис 3.5) и по фракционному составу, что обуславливает различные условия сгорания смеси в этих цилиндрах (в первую очередь по концентрационным пределам воспламеняемости и условиям возникновения детонации). Недостатки, связанные с фракционированием топлива во впускном тракте, характерны для бензиновых карбюраторных двигателей. В двигателях с непосредственным впрыском эти недостатки практически отсутствуют, что обеспечивает, в частности, повышение на 8 % и более топливной экономичности двигателей такого типа в сравнении с карбюраторными ДВС.
Подогрев горючей смеси. В двигателях с внешним смесеобразованием применяют различные методы интенсификации испарения топлива путем подвода теплоты (подогрева) к горючей смеси или жидкому топливу. К ним относятся предварительный подогрев топлива в карбюраторе, подогрев впускного трубопровода, создание высокотемпературных «площадок» и зон во впускном трубопроводе, обеспечивающих испарение попавшего на них жидкого топлива и т.п. В качестве источника теплоты используют отработавшие газы или теплоту из системы охлаждения двигателя.
 С точки зрения процессов смесеобразования и горения топлива рационально обеспечить возможно более высокую температуру горючей смеси (в пределах термической стабильности топлива). В пределе это дает возможность работать на смеси воздуха с сухим паром топлива, т.е. как бы превращать жидкое топливо в газовое. Кроме того, повышение температуры смеси расширяет концентрационные пределы ее воспламеняемости, что создает предпосылки для обеспечения устойчивой работы двигателя на обедненных смесях (рис. 3.6).
С точки зрения процессов смесеобразования и горения топлива рационально обеспечить возможно более высокую температуру горючей смеси (в пределах термической стабильности топлива). В пределе это дает возможность работать на смеси воздуха с сухим паром топлива, т.е. как бы превращать жидкое топливо в газовое. Кроме того, повышение температуры смеси расширяет концентрационные пределы ее воспламеняемости, что создает предпосылки для обеспечения устойчивой работы двигателя на обедненных смесях (рис. 3.6).
Величина подогрева горючей смеси ограничена тем, что с увеличением температуры уменьшается коэффициент наполнения, а следовательно, максимальная мощность, развиваемая двигателем. Поэтому у подавляющего большинства современных двигателей с внешним смесеобразованием горючая смесь подогревается до относительно невысоких температур.
Однако с помощью изменений конструкции можно обеспечить регулирование подогрева таким образом, чтобы он не влиял на максимальную мощность двигателя. Для этого на режиме максимальной мощности горючая смесь не должна подогреваться, а на всех частичных режимах должен быть обеспечен оптимальный с точки зрения смесеобразования (а, следовательно, достаточно интенсивный) подогрев.
Влияние испаряемости топлива на пуск холодного двигателя. При низких температурах запуск ДВС затруднен из-за повышенной вязкости моторного масла, ухудшения испаряемости топлива, меньших температур и давлений в конце такта сжатия. Вследствие относительно низкой частоты вращения коленчатого вала скорость воздуха во впускном тракте недостаточна для обеспечения эффективного механического дробления (распыла) жидкого топлива, поступающего из распылителя (форсунки). Это, а также повышенные вязкость и поверхностное натяжение холодного топлива обусловливают ухудшение процесса смесеобразования. Облегчают запуск, увеличивая испаряемость бензина путем повышения количества содержащихся в нем низкокипящих фракций. Количественно это определяется температурами tк, t10% и давлением насыщенных паров рн.п. В карбюраторных двигателях предельно низкую температуру пуска tв°С, ориентировочно определяют по эмпирической формуле
 .
.

Зависимость tв от рн.п. для бензиновых двигателей представлена на рис. 3.7. Понижение tн.к., t10% и повышение рн.п. для бензинов ограничено возможностью появления при высоких температурах паровых пробок в системе топливоподачи.
Дата добавления: 2015-08-26; просмотров: 1228 | Нарушение авторских прав
| <== предыдущая страница | | | следующая страница ==> |
| Основные положения химмотологии. | | | Детонационная стойкость топлив 1 страница |