
Читайте также:
|
В молекуле циклопропана все атомы углерода расположены в одной плоскости.
При таком расположении атомов углерода в цикле валентные углы должны быть равны 600, а величина их отклонения от нормального валентного угла (109028) должна составлять: α = (109028 – 600): 2 = 24044. Это наиболее напряженная циклическая система.
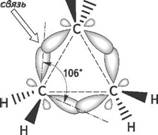
Однако в действительности, валентные углы между атомами углерода в циклопропановом цикле составляет 1060. Это объясняется тем, что σ-связи между атомами углерода в циклопропане отличаются от обычных σ-связей, образующихся при перекрывании sp3-гибридных орбиталей в алканах.
При образовании углерод-углеродных связей в циклопропановом цикле происходит только частичное перекрывание sp3-гибридных орбиталей, направленное не вдоль прямой, соединяющей центры связанных углеродных атомов, а за пределами плоскости циклопропана, что приводит к образованию изогнутых орбиталей или так называемых банановых или τ- (греч.«тау») связей.
Образование банановых (или τ-) связей в циклопропане приводит к уменьшению углового напряжения в цикле, так как угол между осями двух электронных облаков увеличивается от 600 до 1060, а сами τ-связи приобретают частично ненасыщенный характер и по прочности они занимают промежуточное положение между σ- и π-связями.
Этим объясняется склонность циклопропана к реакциям присоединения. О частичном ненасыщенном характере атомов углерода в молекуле циклопропана свидетельствует также повышенная протонная подвижность атомов водорода.
Дата добавления: 2015-07-12; просмотров: 110 | Нарушение авторских прав
| <== предыдущая страница | | | следующая страница ==> |
| Перегруппировки, приводящие к расширению цикла | | | Изомерия |