
Читайте также:
|
Внутрикомплексные соединения – солеобразные соединения, характеризующиеся донорно-акцепторными и ковалентными связями между лигандами и комплексообразователем.
Отличаются большой прочностью, т.к. лиганды захватывают центральный ион как клешни рака(клешневидный комплекс)
Внутрикомплексные соединения относят комплексы, в которых лигандами являются органические молекулы.
Пример: глицерин, этилендиамин, анион щавелевой кислоты с комплексообразователем например Сu
Бис(этилендиамино)меди(II)
 СН2 – NH2 - - - - NH2 - СН2
СН2 – NH2 - - - - NH2 - СН2
 Сu2+
Сu2+ 
СН2 – NH2 - - - - NH2 - СН2
Связь, соединяющие донорные атомы одной молекулы для удобства изображают в виде дуги.
 NH2 - - - - NH2 наиболее распространенны комплексные соединения в которых донорные атомы
NH2 - - - - NH2 наиболее распространенны комплексные соединения в которых донорные атомы
 Сu2+
Сu2+  лигандов заключены в единое кольцо – цикл и представляют собой порфирины
лигандов заключены в единое кольцо – цикл и представляют собой порфирины
NH2 - - - - NH2
Природные внутрикомплексные соединения. Общие представления о строении гема, хлорофилла, каталазы, цианокобаламина, цитохромов. Метаболические реакции с участием металлоферментов. Их роль в биологических процессах.
В качестве центрального атома может выступать Mg+2 (II) образуется хлорофилл (зеленый пигмент растений, играет ключевую роль в процессе фотосинтеза)
 N - - - - - N R1, R2, R3, R4 – углеводородные радикалы
N - - - - - N R1, R2, R3, R4 – углеводородные радикалы
 Mg
Mg  донорные атомы N расположенные по углам квадрата, т.е. жестко скомбинированы в
донорные атомы N расположенные по углам квадрата, т.е. жестко скомбинированы в
N - - - - - N пространстве, поэтому такие комплексы имеют прочную структуру.
Ион Fe2+ входит в состав гемоглобина, у него 6 координационных вакансий: 4 удерживают его в плоскости кольца порфирина, а 2 направлены перпендикулярно к плоскости.


 О2 координационное число = 6
О2 координационное число = 6
Комплексообразователь - Fe2+

 N - - - - - N
N - - - - - N
 ⋮ Fe2+ ⋮
⋮ Fe2+ ⋮
 N - - - - - N
N - - - - - N
N-глобин
Гемоглобин выполняет две биологические функции:
1. Связывает молекулы О2 с атомами железа и переносит из легких к мышцам: ННв + О2 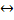 ННвО2
ННвО2
2. С помощью кольцевых аминогрупп связывает несколько метаболических молекул СО2 и переносит их в легкие
Компонент гемоглобиновой буферной системы
Каталаза:
Фермент катализирующий разложение перекиси


 Н2О2 координационное число = 6
Н2О2 координационное число = 6
Комплексообразователь – Fe3+

 N - - - - - N
N - - - - - N
 ⋮ Fe3+ ⋮
⋮ Fe3+ ⋮
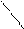
 N - - - - - N
N - - - - - N
ОН
Механизм действия каталазы:
katFeOH + H2O 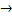 katFeOOH + H2O
katFeOOH + H2O
katFeOOH + H2O2 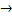 katFe – OH + O2 + H2O
katFe – OH + O2 + H2O
H2O2 + H2O3 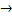 2H2O + O2
2H2O + O2
2 H2O2  2H2O + O2
2H2O + O2
Цитохром:


 N - гистидин координационное число = 6
N - гистидин координационное число = 6
Комплексообразователь – Fe3+, Fe2+

 N - - - - - N
N - - - - - N
 ⋮ Fe3+ ⋮
⋮ Fe3+ ⋮
 N - - - - - N
N - - - - - N
S-метионин
Участвует в переносе электронов в результате обратимого изменения валентности атома Fe, т.е. участвует в ОВР.
Витамин В12 (цианокобаламин)


 CN координационное число = 6
CN координационное число = 6
Комплексообразователь – Со3+

 N - - - - - N
N - - - - - N
 ⋮ Co3+ ⋮
⋮ Co3+ ⋮
 N - - - - - N
N - - - - - N
N-бензимидазол
Биологическая роль: участвует в синтезе гемоглобина, вызывает анемию; противоанемическое, противовоспалительное действие; применяется при заболеваниях нервной системы.
Образование комплексных соединений как основа хелатотерапии. Применение комплексонов при отравлениях тяжелыми металлами. Конкретные механизмы связывания металлов при использовании в качестве комплексонов этилендиаминтетрауксусной кислоты(Трилона А и Б), унитиола, тетацина.
Загрязнение окружающей среды токсичностью элементов тяжелых металлов(Ве, Рb, Cd) может приводить к отравлениям и токсичность таких соединений объясняется взаимодействиям тяжелых металлов с бионеорганическими комплексами.
МбL + Мт 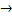 Мб + МтL
Мб + МтL
МбL – комплекс иона биогенного металла(Fe, Cu, Co, Zn)
Мт – ион тяжелого металла (Hg, Pb, Cd)
В настоящее время сложилось специальное направление в медицине, связанное с использованием лигандов для регуляции металла лигандного баланса.
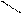 CH2 – SH CH2 – S
CH2 – SH CH2 – S
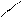 l l Hg+2
l l Hg+2
CH – SH + HgCI₂ 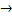 CH – S + 2HCI
CH – S + 2HCI
I l
CH2 – SО3Na CH2 – SО3Na
унитиол
С избытком унитиола образуется комплекс с координационным числом =4(Cd+2, Pd+2)
В качестве антидотов широко используются нуклесомы(ЭДТА)
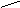
 НООС – СН2 СН2 – СООН
НООС – СН2 СН2 – СООН
 N – СН2 – СН2 – N
N – СН2 – СН2 – N
НООС – СН2 СН2 – СООН трилон А
Трилон Б Na2 – ЭДТА
 NaООС – СН2 СН2 – СООNa NaООС СН2 – СООNa
NaООС – СН2 СН2 – СООNa NaООС СН2 – СООNa


 N – СН2 – СН2 – N
N – СН2 – СН2 – N  N – СН2 – СН2 – N
N – СН2 – СН2 – N
НООС – СН2 СН2 – СООН СН2 СН2

 I Са I
I Са I
О=С – О О – С = О тетацинкальций
Устойчивость комплексных соединений. Первичная и вторичная диссоциация комплексных соединений. Константы нестойкости и устойчивости комплекса. Константы устойчивости комплексных соединений.
Внутренняя и внешняя структура комплекса сильно различается по устойчивости. В растворах комплексных соединений имеет место первичная и вторичная диссоциация.
Первичная диссоциация – отщепление сферы внешней от внутренней протекает как у сильных электролитов практически полностью(необратимо)
[Ag(NH₃)₂]Cl 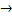 [Ag(NH₃)₂]+ + Cl-
[Ag(NH₃)₂]+ + Cl-
Вторичная диссоциация характеризует диссоциацию самого иона, а т.к. лиганды находятся во внутренней сфере и связаны с центральным ионом значительно прочнее, поэтому отщепляются лишь в небольшой степени(обратимый процесс)
[Ag(NH₃)₂]+ 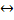 Ag+ + 2NH₃
Ag+ + 2NH₃
Вторичная стадия диссоциации подчиняется закону действующих масс и характеризуется константой нестойкости – характеризует неустойчивость комплекса иона.
Kн = 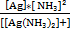 = 6,8 * 10-8
= 6,8 * 10-8
Величина обратная Kн называется Куст
Куст = 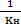
Дата добавления: 2015-07-11; просмотров: 221 | Нарушение авторских прав
| <== предыдущая страница | | | следующая страница ==> |
| Комплексные соединения. Состав и строение, исходя из теории лигандообменных равновесий А. Вернера. | | | Биогенные элементы. Органогенные элементы и их роль в живой клетке. Металлы жизни. |