
Читайте также:
|
Бикарбонатная буферная система: NaHCO3/ H2CO3:
Наиболее важная буферная система крови, на её долю в крови приходится больше 50% буферного действия. Кислоты, образованные в организме в результате метаболизма попадают в кровь, где связываются с бикарбонатной буферной системой: NaHCO3 + HCl⤑ NaCl + H2CO3
Угольная кислота переносится кровью в легкие, что обеспечивает выделение CO2 в воздух: H2CO3⤑ CO2 + H2O таким путем организм освобождается от избытка кислоты, накапливаемой соли и H2O удаляются с мочой и потом. Убыль бикарбоната пополняется в процессе тканевого дыхания.
Если в кровь попадает щелочь: H2CO3 + NaOH  NaHCO3 + H2O
NaHCO3 + H2O
Расчет pH бикарбонатной буферной системы происходит по уравнению Гендерсона-Гессельбаха:
pH= pKa (H2CO3)+lg  pKa (H2CO3)=6,36
pKa (H2CO3)=6,36
Фосфатная буферная система: Na2HPO4/NaH2PO4
Имеет наибольшее значение в биологических жидкостях(моче, крови, соке пищеварительных желез) и главным образом сосредоточено в почках.
Расчет pH= pK (H2PO4-)+lg 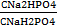
Имеет более высокую емкость по кислоте, чем по щелочи, поэтому она эффективно нейтрализует кислые метаболиты, поступающие в кровь.
Т.к. буферная емкость по кислоте и по щелочи данной буферной системы мало отличается друг от друга поэтому фосфатная система участвует в нейтрализации основных продуктов
Щелочь, попадая в почки, то происходит нейтрализация кислоты щелочью: NaH2PO4 + NaOH  Na2HPO4 + H2O
Na2HPO4 + H2O
Белковая буферная система:
Значительную долю буферной емкости крови обеспечивают белковые системы(гемоглобин, оксигемоглобин, белки плазмы)
Благодаря белкам клетки и ткани организма проявляют значительные буферные действия.
Молекула белков содержит остатки аминокислот: NH2 – CH(R) – COOH

 Аминокислоты – амфотерные электролиты. COOH COO-
Аминокислоты – амфотерные электролиты. COOH COO-
 Белковая буферная система состоит из протеинов: Pt ↔ Pt
Белковая буферная система состоит из протеинов: Pt ↔ Pt
: NH2 NH3 сопряженное основание(внутр. соль)
Изоэлектрическая точка – значение pH при котором аминокислота или белки находятся в виде внутренней соли и количество COO- и NH3 равны.

 COOH COOH
COOH COOH

 Pt + HCl ⤑ Pt
Pt + HCl ⤑ Pt
NH3 NH3Cl солянокислый протеин
При добавлении кислоты ионы Н+ связываются соленой формой. Количество незначительной кислоты повышается, а солевая форма белка понижается, поэтому pH остается постоянным.
При добавлении щелочи к данному буферному раствору:

 COOH COONa
COOH COONa

 Pt + NaOH ⤑ Pt
Pt + NaOH ⤑ Pt
NH3 NH3OH протеинат натрия
Количество солевой формы белка повышается, а внутренние соли понижаются. pH практически не меняется
Гемоглобиновая буферная система:
Сосредоточена в эритроцитах.
Состоит из четырех компонентов, поэтому обладает высокой буферной емкостью.
ННв↔ НВ- + Н+ ННВ – гемоглобиновая кислота
ННвО2 ↔Н+ + НВО2- ННвО2 – оксигемоглобиновая кислота
Гемоглобиновая буферная система в организме работает в сочетании с бикарбонатной. В легких гемоглобин взаимодействует с О2 воздуха образуется оксигемоглобин: ННв + О2 ⤑ ННвО2
Оксигемоглобин как более сильная кислота взаимодействует с HCO3- с образованием более слабой H2CO3 ⤑ удаляется легкими
ННв + О2 + HCO3- = НВО2- + H2O + СО2 процесс, протекающий в легочных капиллярах
НВО2- + H2CO3 = О2 + ННв + HCO3- процесс, протекающий в тканевых капиллярах
Дата добавления: 2015-07-11; просмотров: 584 | Нарушение авторских прав
| <== предыдущая страница | | | следующая страница ==> |
| Буферная емкость. Влияние добавления или щелочи на pH среды буферных систем. Буферная емкость по кислоте(Ва) и по щелочи(Вв). Факторы, определяющие буферную емкость. | | | Нарушение кислотно-щелочного равновесия. Ацидоз, алкалоз. Способы их устранения. |