
Читайте также:
|
Точную зависимость скорости химической реакции от температуры устанавливает уравнение Аррениуса.
1899г. – Аррениус выдвинул теорию активации: во взаимодействие вступают только те молекулы, которые обладают определенным запасом энергии, необходимым для осуществления той или иной реакции.
Энергия активации(Еа) – избыточная энергия которую необходимо передать 1молю вещества чтобы перевести все молекулы в активное состояние.
Нормальное температурное поведение скорости различных реакций определяется следующей зависимостью константы скорости от температуры: К = 
Еа и А – постоянные не зависящие от температуры величины
Т – абсолютная температура
Для биохимических процессов, когда трудно определить константу, уравнение Аррениуса можно представить:
V =  Ас = А
Ас = А  САna
САna  САnв
САnв
Уравнение Аррениуса в дифференциальной форме:  =
= 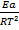
 =
= 
Решая уравнение Аррениуса совместно с уравнением изобары получим: Еа = ∆Н + RT
При незначительных значениях RT: Еа = ∆Н
Расчет Еа по уравнению Аррениуса: lg  =
= 
Ea =  * lg
* lg 
Дата добавления: 2015-07-11; просмотров: 274 | Нарушение авторских прав
| <== предыдущая страница | | | следующая страница ==> |
| Зависимость скорости реакции от температуры. Правило Вант-Гоффа. | | | Понятие о теории переходного состояния. Катализ и катализаторы. Механизм действия гомогенного катализа. |