
Читайте также:
|
Химические свойства спиртов
Кислотные свойства спиртов выражены очень слабо. Низшие спирты бурно реагируют с щелочными металлами с образованием алкоголятов (в данном примере – этилалкоголята калия):

Спирты вступают в реакции замещения с галогеноводородами:

С кислотами (органическими или неорганическими) спирты вступают в реакцию этерификации в присутствии серной кислоты с образованием сложных эфиров:
O О
// H+ //
H3C—С—OH + HO—C2H5 → H3C—C—O—C2H5 + H2O
При нагревании спирта в присутствии сильной кислоты происходит отщепление молекулы воды от двух молекул спирта в результате межмолекулярной дегидратации и образуется простой эфир (в данном примере – диэтиловый эфир):

Амины
Амины - производные аммиака, полученные замещением атомов водорода на углеводородные радикалы.
По числу замещённых атомов водорода различают соответственно первичные, вторичные и третичные амины:
первичные (R–NH2),вторичные (R–NH–R') и третичные (R–N–R") амины.
I
R
Четвертичная аммониевая соль вида [R4N]+Cl- является органическим аналогом аммониевой соли.
По характеру органического радикала R амины подразделяют на алифатические (насыщенные, ненасыщенные) и ароматические амины.
По числу NH2-групп в молекуле амины делят на моноамины, диамины, триамины и т. д.
Построение названий аминов производится прибавлением приставки амино- к названию соответствующего углеводорода (первичные амины) или окончания -амин к перечисленным названиям радикалов, связанных с атомом азота (для любых аминов).
Амины, являясь производными аммиака, имеют сходное с ним строение и проявляют подобные ему свойства. Амины, как и аммиак, обладают основными свойствами, а значит, способны взаимодействовать с кислотами с образованием соответствующих аммониевых солей.
Амины вступают в реакции алкилирования с галогеналканами с образованием вторичных и третичных аминов. Алкилирование – это реакция введения в молекулу R- алкильного радикала.
CH3-NH2 + C2H5Br = CH3-NH-C2H5 +НBr (метилэтиламин)
Окисление аминов. Качественные реакции на амины.
Качественной реакцией на амины является реакция с азотистой кислотой с выделением газа азота и спирта.
C2H5NH2 + HNO2 → C2H5OH + N2↑+H2O
В ароматических аминах аминогруппа ориентирует другие заместители в орто- и пара-положения бензольного кольца. Поэтому галогенирование анилина происходит быстро и в отсутствие катализаторов, причем замещаются сразу три атома водорода бензольного кольца, и выпадает белый осадок 2,4,6-триброманилина (о,о,п-триброманилина):
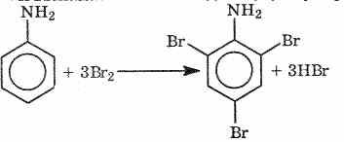
Эта реакция бромной водой используется как качественная реакция на анилин.
Алифатические амины окисляются под действием сильных окислителей. В отличие от аммиака, низшие газообразные амины способны воспламеняться от открытого пламени.
Реакция горения (полного окисления) аминов на примере метиламина:
4СH3NH2 + 9O2 -> 4CO2 + 10H2O + 2N2
Дата добавления: 2015-10-21; просмотров: 2182 | Нарушение авторских прав
| <== предыдущая страница | | | следующая страница ==> |
| ОЧИСТИТЕЛЯ ЗЕРНА СЕТЧАТОГО ОЗС-50 | | | Альдегиды и кетоны. РЕакция присоединения. |