
Читайте также:
|
| 13,60 0,75 2,1 0,046 0,0741 436,1 |
Молекула водорода состоит из двух атомов. Приведем некоторые свойства, характеризующие атом и молекулу водорода;
Энергия ионизации атома, эВ Сродство атома к электрону, эВ Относительная электроотрицательность Радиус атома, нм
Межъядерное расстояние в молекуле, нм Стандартная энтальпия диссоциации молекул при 25 °С, кДж/моль
115. Водород в природе. Получение водорода. Водород в свободном состоянии встречается на Земле лишь в незначительных количествах. Иногда он выделяется вместе с другими газами при вулканических извержениях, а также из буровых скважин при добывании нефти. Но в виде соединений водород весьма распространен. Это видно уже из того, что он составляет девятую часть массы воды. Водород входит в состав всех растительных и животных организмов, нефти, каменного и бурого углей, природных газов и ряда минералов. На долю водорода из всей массы земной коры, считая воду и воздух, приходится около 1 %. Однако при пересчете на проценты от общего числа атомов содержание водорода в земной коре равно 17 % [79].
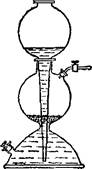
Рис. 105. Аппарат Киппа.
Водород — самый распространенный элемент космоса. На его долю приходится около половины массы Солнца и большинства других звезд. Он содержится в газовых туманностях, в межзвездном газе, входит в состав звезд. В недрах звезд происходит превращение ядер атомов водорода в ядра атомов гелия. Этот процесс протекает с выделением энергии, для многих звезд, в том числе для Солнца, он служит главным источником энергии. Скорость процесса, т. е. количество ядер водорода, превращающихся в ядра гелия в одном кубическом метре за одну секунду, мала. Поэтому и количество энергии, выделяющейся за единицу времени в единице объема, мало. Однако, вследствие огромности массы Солнца, общее количество энергии, генерируемой и излучаемой Солнцем, очень велико. Оно соответствует уменьшению массы Солнца приблизительно на 4 млн. т в секунду.
В промышленности водород получают главным образом из при«родного газа. Этот газ, состоящий в основном из метана, смешивают с водяным паром и с кислородом. При нагревании смеси га«зов до 800—900 °С в присутствии катализатора происходит реакция, которую схематически можно изобразить уравнением1
2СН4 + 02 + 2HsO => 2С02 + 6Н2
Полученную смесь газов разделяют. Водород очищают и либр используют на месте получения, либо транспортируют в етальныЯ баллонах под повышенным давлением.
Важным промышленным способом получения водорода служит также его выделение из коксового газа или из газов переработки нефти. Оно осуществляется глубоким охлаждением, при котором все газы, кроме водорода^.сжижаются.
В лабораториях водород получают большей частью электролизом водных растворов NaOH или КОН. Концентрация этих растворов выбирается такой, которая отвечает их максимальной электрической проводимости (25 % Для NaOH и 34 % для КОН), Электроды обычно изготовляют из листового никеля. Этот металл не подвергается коррозии в растворах щелочей, даже будучи анодом. В случае надобности получающийся водород очищают от паров воды и от следов кислорода. Из других лабораторных методой наиболее распространен метод выделения водорода из растворов серной или соляной кислот действием на них цинка. Реакцию обычно проводят в аппарате Киппа (рис. 105).
|
116. Свойства и применение водорода. Водород — бесцветный газ, не имеющий запаха. При температуре ниже —240 °С (критическая темлература водорода) он под давлением сжижается}
температура кипения жидкого водорода —252,8 °С (при нормальном атмосферном давлении). Если быстро испарять эту жидкость, то получается твердый водород в виде прозрачных кристаллов, плавящихся при —259,2 °С.
Водород-—самый легкий из всех газов, он в 14,5 раза легче воздуха; масса 1 л водорода при нормальных условиях равна 0,09 г. В воде водород растворим очень мало, но в некоторых металлах, например в никеле, палладии, платине, растворяется в значительных количествах.
С растворимостью водорода в металлах связана его способность диффундировать через металлы. Кроме того, будучи самым легким газом, водород обладает наибольшей скоростью диффузии: его молекулы быстрее молекул всех других газов распространяются в среде другого вещества и проходят через разного рода перегородки. Особенно велика его способность к диффузии при повышенном давлении и высоких температурах. Поэтому работа с водородом в таких условиях сопряжена со значительными трудностями.
Диффузия водорода в сталь при высоких температурах может вызвать водородную коррозию стали. Этот совершенно особый вид коррозии состоит в том, что водород взаимодействует с имеющимся в стали углеродом, превращая его в углеводороды (обычно в метан), что приводит к резкому.ухудшению свойств стали.
Химические свойства водорода в значительной степени определяются способностью его атомов отдавать единственный имеющийся у них электрон и превращаться в положительно заряженные ионы. При этом проявляется особенность атома водорода, отличающая его от атомов всех других элементов: отсутствие промежуточных электронов между валентным электроном и ядром. Ион водорода, образующийся в результате потери атомом водорода электрона, представляет собой протон, размер которого на несколько порядков меньше размера катионов всех других элементов. Поэтому поляризующее действие протона очень велико, вследствие чего водород не способен образовывать ионных соединений, в которых он выступал бы в качестве катиона. Его соединения даже с наиболее активными неметаллами, например с фтором, представляют собой вещества с полярной ковалентной связью.
Атом водорода способен не только отдавать, но и присоединять один электрон. При этом образуется отрицательно заряженный ион водорода с электронной оболочкой атома гелия. В виде таких ионов водород находится в соединениях с некоторыми активными металлами. Таким образом, водород имеет двойственную химическую природу, проявляя как окислительную, так и восстановительную способность. В большинстве реакций он выступает в качестве восстановителя, образуя соединения, в которых степень его окисленности равна +1- Но в реакциях с активными металлами он выступает в качестве окислителя: степень окисленности его в соединениях с металлами равна —1.
Таким образом, отдавая один электрон, водород проявляет сходство с металлами первой группы периодической системы, а присоединяя электрон, — с неметаллами седьмой группы. Поэтому водород в периодической системе обычно помещают либо в первой группе и в то же время в скобках в седьмой, либо в седьмой группе и в скобках в первой.
Соединения водорода с металлами называются гидридами. Гидриды щелочных и щелочноземельных металлов представляют собой соли, т. е. химическая связь между металлом и водородом в них ионная. Это кристаллы белого цвета. Все они нестойки и при нагревании разлагаются на металл и водород. При действии на них воды протекает окислительно-восстановительная реакция4 в которой гидрид-ион Н~ выступает в качестве восстановителя, а водород воды — в качестве окислителя:
Н" = Н° + е"; Н20 + е" = Н° + ОН-
В результате реакции образуются водород и основание. Например, гидрид кальция реагирует с водой согласно уравнению: СаН2 + 2Н20 = 2H2f + Са(ОН)2
Эта реакция используется для определения следов влаги и для их удаления.
Кроме солеобразных известны металлообразные и полимерные гидриды. По характеру химической связи в металлообразных гидридах последние близки к металлам. Они обладают значительной электрической проводимостью и металлическим блеском, но очень хрупки. К ним относятся гидриды титана, ванадия, хрома. В полимерных гидридах (например, в гидридах цинка и алюминия) атомы металла связаны друг с другом водородными «мостиками», подобно тому, как это имеет место в молекулах бороводородов (стр. 612).
Если к стр^е водорода, выходящей из какого-нибудь узкого отверстия, поднести зажженную спичку, то водород загорается и горит несветящимся пламенем, образуя воду:
2Н2 + 02 — 2Н20
При поджигании смеси 2 объемов водорода с 1 объемом кислорода соединение газов происходит почти мгновенно во всей массе смеси и сопровождается сильным взрывом. Поэтому такую смесь называют гремучим газом. Стандартная энтальпия этой реакции в расчете на 1 моль образующейся жидкой воды равна —285,8 кДж, а в расчете на 1 моль водяного пара — 241,8 кДж. Таким образом, при горении водорода выделяется большое количество теплоты. Температура водородного пламени может достигать 2800°С. Водородно-кислородным пламенем пользуются для сварки и резки металлов, для плавления тугоплавких металлов.
При низких температурах водород с кислородом практически не взаимодействуют. Если смешать оба газа и оставить смесь, то и через несколько лет в ней нельзя обнаружить даже признаков воды. Если же смесь водорода с кислородом поместить в запаянный сосуд и держать в нем при 300 °С, то уже через несколько дней образуется немного воды. При 500 °С водород полностью соединяется с кислородом за несколько часов, а при нагревании смеси до 700 °С происходит быстрый подъем температуры и реакция заканчивается практически мгновенно. Поэтому, чтобы вызвать взрыв смеси, нужно нагреть ее хотя бы в одном месте до 700 °С.
Малая скорость взаимодействия водорода с кислородом при низких температурах обусловлена высокой энергией активации этой реакции. Молекулы водорода и кислорода очень прочны; любое столкновение между ними при комнатной температуре оказывается неэффективным. Лишь при повышенных температурах, когда кинетическая энергия сталкивающихся молекул делается большой, некоторые соударения молекул становятся эффективными и приводят к образованию активных центров.
Применение катализатора может сильно увеличить скорость взаимодействия водорода с кислородом. Внесем, например, кусочек платинированного (т. е. покрытого мелко раздробленной платиной)' асбеста в смесь водорода с кислородом. Взаимодействие между газами настолько ускоряется, что через короткое время происходит взрыв.
Напомним, что реакция между водородом и кислородом является цепной и протекает по разветвленному механизму (см. § 62),
При высокой температуре водород может отнимать кислород от многих соединений, в том числе от большинства оксидов металлов. Например, если пропускать водород над накаленным оксидом меди, то происходит восстановление меди:
СиО + Н2 = Си + Н20
Поэтому водород применяют в металлургии для восстановления некоторых цветных металлов из их оксидов. Главное применение водород находит в химической промышленности для синтеза хло- роводорода (см. § 121), для синтеза аммиака (см. § 138), идущего в свою очередь на производство азотной кислоты и азотных удобрений, для получения метилового спирта (см. § 169) и других органических соединений. Он используется для гидрогенизации [80] жиров (см.§ 173), угля и нефти. При гидрогенизации угля и нефти бедные водородом низкосортные виды топлива превращаются в высококачественные.
Водород используют для охлаждения мощных генераторов электрического тока, а его изотопы находят применение в атомной энергетике (см. стр. 108).
Атомарный водород. При высокой температуре молекулы водорода диссоциируют на атомы:
Н2:«=±: 2Н
Осуществить эту реакцию можно, например, раскаляя током вольфрамовую проволочку в атмосфере сильно разреженного водорода. Реакция обратима, и чем выше температура, тем сильнее равновесие сдвинуто вправо. При 2000°С степень диссоциации (т.е. доля молекул, подвергшихся диссоциации) составляет только 0,1%, при 3000 °С — 9%, при 4000 °С — 62,5 %, при 5000 °С — 94,7 % (все величины относятся к случаю, когда давление в системе равно нормальному атмосферному давлению).
Атомарный водород получается также при действии тихого электрического разряда- на молекулярный водород, находящийся под давлением около 70 Па. Образующиеся при этих условиях атомы водорода не сразу соединяются в молекулы, что дает возможность изучить их свойства.
При разложении водорода на атомы поглощается большое количество теплоты:
Н2 = 2Н —436 кДж
Отсюда понятно, что атомы водорода должны быть гораздо активнее его молекул. Чтобы молекулярный водород вступил в какую-либо реакцию, молекулы должны сперва распасться на атомы, для чего необходимо затратить большое количество энергии. При реакциях же атомарного водорода такой затраты энергии не требуется.
Действительно, атомарный водород уже при комнатной температуре восстанавливает многие оксиды металлов, непосредственно соединяется с серой, азотом и фосфором; с кислородом, он образует пероксид водорода.
117. Пероксид водорода Н202. Пероксид (перекись) водорода представляет собой бесцветную сиропообразную жидкость плотностью 1,45 г/см3, затвердевающую при —0,48°С. Это очень непрочное вещество, способное разлагаться со взрывом на воду и кислород, причем выделяется большое количество теплоты: 2Н202(ж) = 2Н20(ж) + 02 +197,5 кДж
Водные растворы пероксида водорода более устойчивы; в прохладном месте они могут сохраняться довольно долго. Пергидроль — раствор, который поступает в продажу, — содержит 30 % Н202. В нем, а также в высококонцентрированных растворах пероксида водорода содержатся стабилизирующие добавки.
Разложение пероксида водорода ускоряется катализаторами. Если, например, в раствор пероксида водорода бросить немного диоксида марганца Мп02, то происходит бурная реакция и выделяется кислород. К катализаторам, способствующим разложению пероксида водорода, принадлежат медь, железо, марганец, а также ионы этих металлов. Уже следы этих металлов могут вызвать распад Н202.
Пероксид водорода образуется в качестве промежуточного продукта при горении водорода, но ввиду высокой температуры
Рис. 106. Схема строения молекулы Н202.
/ н / Угол 8 близок к 100°, угол ф —к 95°. Длины связей: О-
/ о—-А? °'097 нм' 0 — 0 °>149 нм-
IF-^h
водородного пламени тотчас же разлагается на воду и кислород. Однако если направить водородное пламя на кусок льда, то в образующейся воде можно обнаружить следы пероксида водорода.
Пероксид водорода получается также при действии атомарного водорода на кислород.
В промышленности пероксид водорода получают в основном электрохимическими методами, например анодным окислением растворов серной кислоты или гидросульфата аммония с последующим гидролизом образующейся при этом пероксодвусерной кислоты H2S208 (см. § 132). Происходящие при этом процессы можно изобразить схемой:
2H2S04 = H2S208 + 2Н+ + 2е~ H2S208 + 2Н20 = 2H2S04 + Н202
В пероксиде водорода атомы водорода ковалентно связаны с атомами кислорода, между которыми также осуществляется простая связь. Строение пероксида водорода можно выразить следующей структурной формулой: Н—О—О—Н.
Молекулы Н2О2 обладают значительной полярностью (ц = = 2,13D), что является следствием их пространственной структуры (рис. 106).
В молекуле пероксида водорода связи между атомами водорода и кислорода полярны (вследствие смещения общих электронов в сторону кислорода). Поэтому в водном растворе под влиянием полярных молекул воды пероксид водорода может отщеплять ионы водорода, т. е. он обладает кислотными свойствами. Пероксид водорода— очень слабая двухосновная кислота (Ki = 2,6-10~12); в водном растворе он распадается, хотя и в незначительной степени, на ионы:
Нг02 ч=з= Н* + Н02"
Диссоциация по второй ступени
но: н+ + о'-
практически не протекает. Она подавляется присутствием воды — вещества, диссоциирующего с образованием ионов водорода в бблыней степени, чем пероксид водорода. Однако при связывании ионов водорода (например, при введении в раствор щелочи) диссоциация по второй ступени происходит.
С некоторыми основаниями пероксид водорода реагирует непосредственно, образуя соли. Так, при действии пероксида водорода на водный раствор гидроксида бария выпадает осадок ба-,.
риевой соли пероксида водорода:
Ва(ОН)2 + Н202 = Ва02| + 2Н20
Соли пероксида водорода называются пероксидами или перекисями. Они состоят из положительно заряженных ионов металла и отрицательно заряженных ионов 0|~, электронное строение которых можно изобразить схемой:
Дата добавления: 2015-08-21; просмотров: 175 | Нарушение авторских прав
| <== предыдущая страница | | | следующая страница ==> |
| X КОЛЛОИДЫ | | | Ность, ослабевают неметаллические свойства и окислительная способность элементов. |