
|
Читайте также: |
Индивидуальное домашнее задание по теме «Общая химия» №1.
Вариант 7
Глава 1. Атомно-молекулярное учение.
Задача №12.
Чему равна масса азота, содержащаяся в нитрате натрия и в нитрате аммония, взятых по 5 моль?
Решение:
Дано:
νNaNO3=5 моль;
νNH4NO3=5 моль.
Найти mN -?
1)MNaNo3=85г/моль, MN=14г/моль.
 1 моль NaNO3 содержит 14 г. Азота, а 5 моль 14*5=70г.
1 моль NaNO3 содержит 14 г. Азота, а 5 моль 14*5=70г.
2) MNH4NO3=80г/моль.
1 моль NH4NO3 содержит 14*2=28г.азота, так как в 1 молекуле NH4NO3 содержится 2 атома азота) следовательно в 5 молях NH4NO3 содержится: 5*28=140г.азота.
Ответ: 70 и 140 г.
Задача №26. Определить эквивалентные массы металла и серы, если в 1,2 г металла образует2,0 оксида и 2,8 сульфида.
Решение:
Дано: mMe=1,2 г; mоскида=2; mсульфида=2,8г.
Найти MЭMe -?, MЭS-?
Оксид это вещество состоящее из двух элементов, один из которых кислород следовательно MO=mокс-mMe=2-1,2=0,8. mO=0,8г.
Аналогично: mS=2,8-1,2=1,6. mS=1,6г.
По закону эквивалентов найдем:
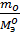 =
= 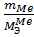
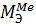 =
= 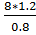 = 12 г/моль.
= 12 г/моль.
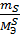 =
= 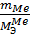
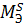 =
= 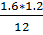 = 16 г/моль.
= 16 г/моль.
Ответ: 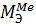 =12г/моль;
=12г/моль; 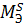 =16г/моль.
=16г/моль.
Дата добавления: 2015-08-17; просмотров: 135 | Нарушение авторских прав
| <== предыдущая страница | | | следующая страница ==> |
| Решение практических задач с использованием уравнений, неравенств и систем | | | Глава 3. Окислительно-восстановительные реакции. |