
Читайте также:
|
Все кислые соли являются твёрдыми кристаллическими веществами, большинство из них не имеет температур плавления, так как они при нагревании раньше разлагаются:
2 KHCO3 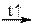 K2CO3 + CO2↑ + H2O↑
K2CO3 + CO2↑ + H2O↑
Или претерпевают другие превращения:
2 Na2HPO4  Na4P2O7 + H2O 2 NaH2PO4
Na4P2O7 + H2O 2 NaH2PO4  Na2H2P2O7 + H2O
Na2H2P2O7 + H2O
NaH2PO4  NaPO3 + H2O
NaPO3 + H2O
Однако, есть исключения. Например KHF2 (гидродифторид калия) – сначала плавится при 239оС и только при 310оС разлагается по уравнению:
KHF2 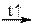 KF + HF↑(газ)
KF + HF↑(газ)
Большинство кислых солей бесцветно. Соль NH4HCr2O7 была бы оранжевой, однако её существование подвергается сомнениям.
Дата добавления: 2015-08-17; просмотров: 60 | Нарушение авторских прав
| <== предыдущая страница | | | следующая страница ==> |
| Способы получения кислых солей | | | Химические свойства кислых солей |