
Соли азотной и азотистой кислот стабильнее самих кислот, но при достаточном нагревании тоже разлагаются. В частности, нитраты ЩМ отщепляют атомарный кислород, переходя в достаточно устойчивые нитриты. А нитриты металлов от Mn до Cu (в ряду напряжений) термически не стабильны, поэтому N-содержащие соли этих М разлагаются с образованием их оксидов:
 ,
,
 .
.
Нитраты благородных М (тем более, их нитриты) дают при нагревании металл вместо оксида:
 ,
,
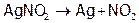 .
.
Термодинамически наименее устойчив из N-содержащих солей – нитрит аммония:
 .
.
Нестабилен и его нитрат, причем в зависимости от Т получаются разные продукты:
 ,
,
 ,
,
 .
.
Последняя реакция идет со взрывом. В ней (как промежуточный продукт) образуется атомарный кислород, поэтому NH4NO3 используют как составляющее аммонала (бездымного пороха) вместе с порошками угля и алюминия.
Качественная реакция на нитрат-ионы – появление бурого газа при действии на анализируемое вещество концентрированной серной кислотой в присутствии меди. (При этом вначале получается диоксид серы, который восстанавливает  до NO2.)
до NO2.)
Качественной реакцией на нитрит-ионы является обесцвечивание малинового раствора перманганата калия в сернокислой среде. (Основные продукты взаимодействия: нитрат-анионы и катионы марганца (II).)
Дата добавления: 2015-07-25; просмотров: 77 | Нарушение авторских прав
| <== предыдущая страница | | | следующая страница ==> |
| Свойства и применение | | | Кислородосодержащие соединения фосфора |