
Рекомендация 43. Возможно применение методики эндартерэктомии у пациентов с высоким риском стандартной реконструктивной операции при наличии у них участка локальной окклюзии поверхностной бедренной артерии и сохраненных путей оттока.
Сущность метода заключается в дезоб-литерации окклюзированной артерии, чаще всего поверхностной бедренной артерии, по полузакрытому типу, т.е. на протяжении между артериотомическими

|
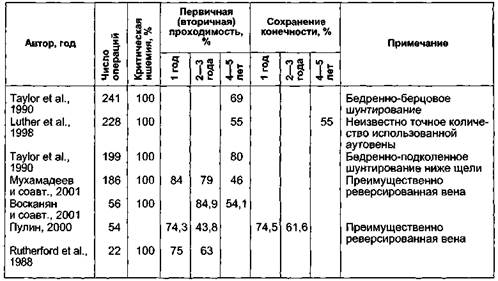
Таблица 7.6. Отдаленные результаты аутовенозного шунтирования ниже коленного сустава по методике in situ у пациентов с критической ишемией
Таблица 7.7. Отдаленные результаты шунтирования ниже коленного сустава реверсированной аутовеной у пациентов с критической ишемией
|
отверстиями проксимальнее и дисталь-нее места окклюзии. С 70—80-х годов для этих целей стали использовать низкочастотный ультразвук. Наибольший опыт (344 операции) опубликован Г.В.Саврасовым и Е.И.Данилиным в 1998 г., критическая ишемия наблюдалась у 91 % пациентов. Через 5 лет проходимость у прослеженных 82 пациентов составила 46,4 % при ишемии III степени и 32,1 % —
при ишемии IV степени. По-видимому, по аналогии с ангиопластикой бедренных артерий для этой операции существуют очень строгие показания, а именно: локальные участки окклюзии поверхностной бедренной артерии с хорошим дис-тальным руслом. Немаловажное значение будет иметь опыт выполняющего операцию хирурга. Единственное преимущество операции, на наш взгляд, за-
|
| 16* |
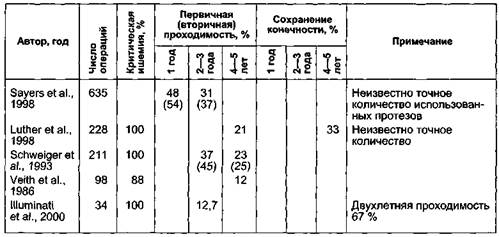
Таблица 7.8. Отдаленные результаты шунтирования ниже коленного сустава синтетическими протезами из ПТФЭ у пациентов с критической ишемией
Таблица 7.9. Отдаленные результаты бедренно (подколенно)-стопного шунтирования у пациентов с критической ишемией

|
ключается в ее меньшей длительности по сравнению со стандартной реконструктивной операцией, поэтому она будет показана у пациентов с крайне высоким риском стандартного вмешательства и невозможностью выполнения рентгено-эндоваскулярной процедуры.
Для улучшения отдаленных результатов А.В.Покровский и соавт. в 1999 г. предложили сочетать методику ультразвуковой эндартерэктомии с эндопроте-зированием тонкостенным протезом из ПТФЭ. Малое количество подобных операций пока не позволяет делать какие-либо конкретные выводы.
Нестандартные реконструктивные операции
Рекомендация 44. При отсутствии возможности выполнить стандартную реконструктивную операцию из-за окклюзии берцовых артерий и артерий голени возможна артериализация венозного кровотока стопы. Операцию необходимо выполнять в центрах с большим опытом подобных реконструкций.
Считают, что основными механизма-
ми купирования критической ишемии при артериализации венозного кровотока стопы в ближайшем периоде являются блокировка артериоловенулярного шунтирования крови, увеличение притока крови к капиллярам и улучшение оксигенации тканей. В отдаленном периоде артериализация стимулирует развитие коллатера-лей. Основное в этой операции — качественное разрушение клапанов в венах стопы. Разработано два вида операции: артериализация поверхностной и глубокой венозных систем. Интересен тот факт, что для предотвращения рецидива ишемии необходимо следующее время работы шунта: для артериализации поверхностной венозной системы — 6 мес, а для глубокой системы — 3 мес. Наибольший материал накоплен в отделении хирургии сосудов Института хирургии им. А.В.Вишневского, где эту операцию выполняют с 1986 г. В настоящее время отделение имеет опыт около 140 подобных операций у пациентов с критической ишемией. Артериализация позволила сохранить конечность и улучшить
ее состояние у 83,8 % пациентов. Через 5 лет число сохраненных конечностей в зависимости от вида артериализации составляло 79,4 и 93,3 % при использовании поверхностной и глубокой венозной систем соответственно. А.В.Вериго (1999) сообщает о результатах 28 операций: 85,7 % положительных ближайших результатов и 83 % сохраненных конечностей через 3 года. О хороших ближайших результатах операции сообщают и Lengua и соавт. (1995) — 73 % спасенных конечностей после 26 операций. На фоне энтузиазма, связанного с методикой, особо стоит работа, авторы которой сравнивали результаты артериализации поверхностной венозной системы (14 операций) с консервативным лечением (14) у пациентов с критической ишемией и получили незначительные различия: 57 % против 54 % соответственно [Matzke S. et al, 1999].
Рекомендация 45. Операция трансплантации большого сальника на голень с наложением микрососудистых анастомозов (что предпочтительнее) или пересадка свободного лоскута большого сальника достаточно эффективны у пациентов с критической ишемией, обусловленной облитерирующим тромбангиитом. У больных с атеросклерозом при критической ишемии эта операция малоэффективна.
Методика имплантации фрагмента большого сальника на голень большого распространения не получила, хотя отдельные авторы отмечают ее высокую эффективность. По данным некоторых хирургов, резекция задних большеберцо-вых вен для ликвидации патологического артериоловенулярного шунтирования используется у больных с облитерирующим тромбангиитом при наличии высокого венозного давления на лодыжечном уровне (>50 мм рт.ст.).
Послеоперационное ведение пациентов
Рекомендация 46. В послеоперационном периоде целесообразно продолжение таблетированной дезагрегантной терапии (ацетилсалициловая кислота и тикло-пидин или клопидогрель), внутривенной медикаментозной терапии (реополиглю-кин, пентоксифиллин) в течение 5—7 дней. При бедренно-дистальных реконструкциях желательно лечение нефракциониро-ванным гепарином или низкомолекулярными гепаринами (фрагмин, клексан, фраксипарин, тропарин) также в течение 5—7 дней.
Тромбозы трансплантатов. Случаи тромбозов трансплантатов следует делить на ранние (до 30 дней) и поздние (более 30 дней) после операции. Причиной ран-
них тромбозов обычно служат технические ошибки и погрешности при выполнении операции, например нарушения геометрии протеза, неправильная оценка состояния путей притока или оттока, т.е. технические и тактические ошибки. Более редки случаи тромбозов на фоне нарушения коагуляции.
Рекомендация 47. При раннем тромбозе трансплантата должна предприниматься попытка ревизии, тромбэктомии или повторной реконструкции.
Рекомендация 48. Необходимо строгое диспансерное наблюдение больных после сосудистых реконструкций. Состояние трансплантатов должно регулярно контролироваться, особенно в течение первого года после операции, для обнаружения участков стеноза и предотвращения возникновения последующего тромбоза. Предпочтительные сроки наблюдения — 3-й, 6-й и 12-й месяцы после операции.
Гораздо проще выполнить превентивную операцию при выявлении участка стеноза трансплантата, чем пытаться спасти конечность после тромбоза. Показано, что более 20 % аутовенозных трансплантатов могут тромбироваться на первом году из-за возникновения участков стенозов. Лучшее средство контроля в данном случае — измерение ЛПИ, а при его снижении — дуплексное сканирование трансплантатов.
Превентивные операции могут быть представлены как ангиопластикой и стентированием, так и открытой коррекцией суженного участка.
Рекомендация 49. При позднем тромбозе трансплантата перед повторным вмешательством необходимо выполнение ангиографического исследования и дуплексного сканирования, а во время операции — интраоперационной ангиографии для выявления состояния путей оттока.
Причиной поздних тромбозов трансплантатов служат прогрессирование патологического процесса в путях как притока, так и оттока, гиперплазия интимы в области анастомозов.
Другие способы купирования критической ишемии нижней конечности
Рекомендация 50. В настоящее время не существует точной информации о способности поясничной симпатэктомии купировать критическую ишемию.
В отсутствие возможностей прямой реваскуляризации применяются различные паллиативные операции, на первом месте из которых стоит поясничная сим-патэктомия в различных модификациях. В последнее время широкое распростра-
нение получила эндоскопическая методика выполнения операции. В отношении этой операции при критической ишемии сообщают о весьма противоречивых как ближайших — от 30 до 72,4 % сохраненных конечностей, так и отдаленных результатах — от 32,1 до 68,1 % сохраненных конечностей. Лучший эффект наблюдается при берцово-стопных поражениях. По мнению большинства авторов, лучшие результаты этой операции отмечаются при соблюдении показаний, которые в отечественной литературе чаще устанавливают на основании функциональных проб лазерной флоуметрии. Кротовский и соавт. считают целесообразным выполнение поясничной сим-патэктомии при установленной положительной реакции на пробу с задержкой дыхания в течение 15 с, Ромашов и соавт. проводили тепловую (нагревание конечности до 42 °С) и нитроглицериновую (прием препарата) пробы по данным лазерной флоуметрии, которые считались положительными, если кровоток усиливался в 1,5—2 раза и быстро возвращался к исходному. А.В.Чупин считает целесообразным выполнение операции при усилении кровотока, определяемого при УЗДГ, по бедренной артерии на 50 % после снятия манжеты с бедра. Лучший результат у зарубежных исследователей получен у пациентов с исходным лоды-жечно-плечевым индексом выше 0,3 и болями в покое. Интересен факт, что и в отечественных публикациях лучшие результаты также наблюдались у пациентов с исходно высокими значениями ЛПИ = = 0,48 ± 0,04 и ТсРО2 = 30 ± 0,9 ммрт.ст. Многие авторы считают операцию нецелесообразной у пациентов с критической ишемией.
Рекомендация 51. Различные варианты стимуляции периостального кровотока при критической ишемии применять нецелесообразно.
Стимуляция периостального кровотока (компактотомия болъшеберцовой кости с последующей тракцией отщепленного фрагмента по Илизарову, кортикоэкто-мия, реваскуляризующая остеотрепанация по Зусмановичу, остеопериостальная вас-куляризация) основывается на двух механизмах: ближайший — рефлекторное воздействие на надкостницу и уменьшение спазма артерий, раскрытие уже существующих коллатералей и соответственное снижение периферического сопротивления; отдаленный, который заключается в развитии коллатерального кровотока через 3—4 мес. Основополож-
ник методики реваскуляризирующеи ос-теотрепанации Ф.Н.Зусманович считает ее неэффективной при выраженном болевом синдроме, ортостатических отеках, а противопоказанием к выполнению операции — любые гнойные заболевания пораженной конечности из-за возможности развития остеомиелита. Все это резко ограничивает группу пациентов с критической ишемией, у которых выполнима костная реваскуляризация.
Фармакотерапия. Фармакотерапию необходимо начинать сразу при поступлении пациента в стационар независимо от того, предполагается ли реконструктивная операция или нет. Целесообразно назначение дезагрегантных препаратов (препараты ацетилсалициловой кислоты вместе с тиклопидином или клопидогре-лем), тем более что подавляющее большинство больных страдают ИБС и им прием этих препаратов показан пожизненно. Стандартная схема внутривенной инфузионной терапия включает введение низкомолекулярных декстранов (рео-полиглюкина) — 400 мл и пентоксифил-лина (трентала) 10—15 мл ежедневно. Объем инфузии при наличии тяжелой сопутствующей кардиальной патологии или ХПН можно уменьшить до 200 мл.
Пентоксифиллин, вводимый внутривенно, был изучен в двух мультицентро-вых, двойных слепых, плацебоконтроли-руемых исследованиях, которые показали его эффективность, касающуюся уменьшения болевого синдрома. В первое исследование (The European Study Group, 1995) было включено 314 пациентов с критической ишемией, половина из которых получала пентоксифиллин по 600 мг 2 раза в день внутривенно в течение 21 дня, а другая половина — плацебо. В группе больных, принимавших активный препарат, было достигнуто статистически значимое уменьшение болевого синдрома, количества потребляемых анальгетиков. Во втором исследовании различия в интенсивности болевого синдрома в группах не носили статистически значимого характера (Norwegian Pentoxifylline Multicenter Trial Group, 1996).
He было проведено клинических исследований применения антикоагулянтов в изолированной терапии при лечении пациентов с критической ишемией, хотя в литературе упоминаются случаи успешной консервативной терапии критической ишемии с помощью низкомолекулярных гепаринов. Есть сведения о хорошем эффекте применения сулодек-
сида (Вессел Дуэ Ф) при синдроме диабетической стопы.
Некоторые авторы сообщают об эффективности внутриартериального введения различных реологических растворов и регионарной венозной крови из пораженной конечности; в работе P.Fre-denucci (1985) гипербарическая оксиге-нация позволила купировать ишемичес-кие боли покоя и заживить небольшие по размеру язвы у Уз из 2000 пациентов через 4—6 нед после начала лечения. Это единичные исследования, ориентироваться на которые нецелесообразно. Тем не менее большинство авторов сходятся во мнении, что изолированная традиционная консервативная терапия малоэффективна при лечении больных с критической ишемией нижних конечностей, а отдаленные результаты неудовлетворительны.
Рекомендация 52. Лечение ваза-простаном пациентов с критической ишемией целесообрано в качестве предоперационной подготовки воспринимающего сосудистого русла предполагаемой операции и в случае, когда по каким-либо причинам невозможно выполнение сосудистой реконструкции.
Первоначально предпочтение отдавали внутриартериальному введению про-стагландина Е1, так как был известен факт быстрой инактивации препарата в легких; затем стало известно, что после временной инактивации активного вещества в организме вновь образуется его активный аналог. В дальнейшем в одном из испытаний было доказано преимущество внутривенного введения препарата у пациентов с ишемией III степени. В настоящее время наиболее часто применяемая дозировка — 60 мкг (от 20 до 80 мкг) в сутки в течение 10 дней, возможно продление курса до 30 дней и более. Препарат разводят в 150—200 мл изотонического раствора натрия хлорида и вводят внутривенно в течение не менее 2 ч. Более быстрая инфузия недопустима. В отечественных публикациях нет сведений о проведении рандомизированных исследований простаноидов. В работах российских исследователей [Покровский А.В. и соавт., 1996], посвященных лечению критической ишемии, сообщается о 91,4 % хороших и удовлетворительных результатах у 170 пациентов с различной этиологией, но у половины из этих пациентов вазапростан использовали в качестве предоперационной подготовки. Авторы отмечают, что препарат наиболее эффективен при поражении ар-
терий ниже паховой связки, при транс-кутанном напряжении кислорода больше 5—10 мм рт.ст., хотя существуют и противоположные мнения.
В "Managment of Peripheral Arterial Disease. TASC", опубликованном в 2000 г., приводятся результаты 13 рандомизированных открытых или двойных слепых клинических исследований, где сравнивались результаты лечения критической ишемии аналогами простагландина Е1 (вазапростана) или простагландина 12 (илопроста) с плацебо или пентоксифил-лином. Суточная дозировка вазапростана колебалась от 20 до 80 мкг, илопроста — от 0,5 до 2 нг/кг в 1 мин. Общее количество пациентов, включенных в исследования, составляло 2748 человек. Длительность терапии варьировала от 2 до 4 нед, препараты вводили внутривенно или внутриартериально. Результатами исследования были: уменьшение болей, снижение потребления анальгетиков, ускорение заживления трофических язв. Из них только два испытания не получили статистически значимых различий в группах, т.е. в остальных исследованиях после применения простагландинов уменьшался болевой синдром и ускорялось заживление язв. Пациенты лучше реагировали на длительное лечение (4 нед). Данные об ампутациях через 3—6 мес после лечения опубликованы в трех исследованиях, касающихся лечения илопростом. Оказалось, что уровень ампутаций в этом периоде у пациентов, получавших препарат, меньше, чем в контрольной группе (23 % против 39 %), и различия статистически значимы. Более того, летальность в эти сроки у получавших илопрост была также меньше (35 % против 55 %, р < 0,05). В целом можно констатировать, что вазапростан полезно применять при отсутствии возможностей оперативного лечения, в качестве предоперационной подготовки, а также при рецидивах ишемии на фоне тромбозов трансплантатов. Препарат фактически является альтернативой ампутации, в связи с чем целесообразно его широкое использование в лечении критической ишемии нижних конечностей. Следует учитывать, что эффекты от введения препарата нивелируются через 6 мес после терапии, поэтому при рецидивах ишемии рекомендованы повторные курсы лечения.
Рекомендация 53. При выявлении активности воспалительного процесса у пациентов с облитерирующим тромбанги-итом необходимо проведение курса противовоспалительной пульс-терапии.
Повышение С-реактивного белка, циркулирующих иммунных комплексов (ЦИК), IgG, IgM свидетельствует об активности аутоиммунного воспаления. Для его купирования проводят пульс-терапию, заключающуюся в введении больших доз депо-преднизолона (солю-медрол 1,0 N 3 внутривенно капельно) и цитостатиков (циклофосфан 1,0 внутривенно капельно на первый день лечения). Возможно проведение до трех курсов подобной терапии, интервала между курсами можно не делать. О ее результативности, помимо клинической картины, судят по нормализации перечисленных выше иммунологических показателей. Следует отметить, что изменения СОЭ в данном случае непоказательны.
Рекомендация 54. У пациентов с диабетической полинейропатией целесообразно добавление к лечению препаратов альфа -липоевой кислоты (эспа-липон) и витаминов группы В (миль-гамма).
Эспа-липон назначают в дозе 600— 1200 мг внутримышечно или внутривенно в сутки в течение 2—4 нед с переходом на таблетированную форму препарата в той же дозе в течение 3 мес. Мильгамму применяют по 2 мл раствора в сутки внутримышечно в течение недели.
Дата добавления: 2015-10-21; просмотров: 106 | Нарушение авторских прав
| <== предыдущая страница | | | следующая страница ==> |
| Пути притока бедренно-подколенно-берцовых шунтов | | | Ампутации |