
Читайте также:
|
Во многих случаях равновесную структуру нельзя однозначно отнести к одному типу — кристаллическому или аморфному. Такие типы можно назвать смешанными. К смешанному типу относятся так называемые жидкие кристаллы (ЖК). Особые свойства ЖК обусловлены тем, что они состоят из чрезвычайно анизотропных и, в то же время, жестких молекул. В результате, между молекулами действуют несколько типов ММВ, интенсивность которых значительно отличается. ЖК-структуры образуются тогда, когда условие структурообразования (U > kT) выполняется только для части ММВ, действующих между фрагментами молекул. Это приводит к тому, что структуры в таких системах не имеют трехмерного характера: дальний порядок существует только вдоль некоторых направлений (одномерные ЖК) или плоскостей (двумерные ЖК).
Очевидно, что ЖК-структуры могут существовать только в достаточно узком интервале условий (температура, давление, растворитель), от которых зависит соотношение (U «kT). Обычно выделяют две разновидности ЖК:
· термотропные, образующиеся в некотором характерном температурном интервале,
· лиотропные, образующиеся при использовании определенных растворителей.
Все ЖК-структуры обладают ярко выраженной макроскопической анизотропностью и резкой зависимостью свойств от внешних условий.
Еще один тип смешанных равновесных структур — это т.н. айсберговые структуры (АС). Они отличаются тем, что их полная макроскопическая однородность при уменьшении масштаба нарушается. Можно рассматривать такие структуры как хаотическую смесь кристаллических и аморфных областей микроскопического масштаба. Обычно, аморфные и кристаллические области существенно различаются по свойствам (например, по плотности) и это приводит к пространственному разделению системы на две однородные фазы, разделенные поверхностью раздела. Однако, для некоторых систем такие различия в свойствах недостаточно велики, и разделения на макрофазы не происходит, результатом чего и является образование айсберговой структуры.
Между кристаллическими и аморфными областями АС существует интенсивный обмен веществом. Другими словами, кристаллические области постоянно разрушаются и образуются вновь. Однако, средняя доля вещества, входящего в состав кристаллических областей, постоянна во времени и зависит только от внешних условий, причем можно выделить два вида АС.
а) При высоких температурах основная доля вещества находится в аморфном состоянии и образует сплошную жидкую среду, в которой "плавают" кристаллические айсберги. В результате, система с макроскопической точки зрения ведет себя подобно обычным аморфным жидкостям.
б) При уменьшении температуры айсберги растут в размерах и, начиная с некоторой критической температуры, начинают касаться друг друга. При дальнейшем снижении температуры образуется сплошная кристаллическая среда, в которой случайным образом располагаются микроскопические "озера" аморфной жидкости. С макроскопической точки зрения, свойства системы аналогичны свойствам твердых поликристаллических тел.
АС отличаются наличием критической температуры, где температурные зависимости большинства физических свойств претерпевают излом:
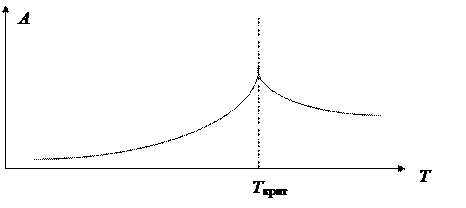 |
Критическая температура очень существенно зависит от наличия примесей. Типичным примером АС является жидкая вода. Для нее критическая температура лежит в интервале 25-35 °С и существенно зависит от наличия таких веществ как амины, спирты, ПАВ и т.д. Сложное поведение, характерное для водных растворов многих веществ, определяется, преимущественно, склонностью воды к образованию айсберговых структур.
Существует множество структурированных макросистем, которые вообще невозможно классифицировать. Типичным примером являются твердые и жидкие полимеры, в которых образуется множество чрезвычайно разнообразных надмолекулярных структур (НМС). Особенным разнообразием НМС отличаются линейные полимеры, построенные из сильнополярных мономерных звеньев различной природы — белки, нуклеиновые кислоты, полисахариды и другие полимеры, образующие химическую основу биологических систем.
Наконец, необходимо отметить, что равновесные макроструктуры обладают временно́й устойчивостью только в макроскопическом масштабе. На короткое время любая структура может разрушаться или изменяться под действием случайных тепловых флуктуаций. Такие кратковременные и микроскопические по размеру нарушения структуры называются дефектами. Несмотря на динамический характер дефектов (они постоянно образуются и исчезают), их среднее число или плотность остается постоянным во времени и зависит только от температуры. Поэтому можно считать дефекты неотъемлемой частью равновесных макроструктур. Многие особенности свойств макроскопических веществ связаны именно с дефектами их структуры (например, пластичность металлов, хрупкость стекол и т.д.).
В качестве особого вида дефектов структуры можно выделить поверхности раздела фаз. В действительности, такие поверхности представляют собой тонкие слои вещества (толщиной от нескольких единиц до нескольких десятков молекулярных размеров). Молекулы, составляющие такой слой, находятся в особых — анизотропных — внешних условиях: свойства двух фаз, разделяемых данным слоем, различны. Поэтому молекулы вынуждены определенным образом ориентироваться относительно этих двух фаз и друг друга. Это, в свою очередь, вызывает появление ряда особенностей в величине и характере ММВ, действующих между молекулами поверхностного слоя. Еще одной особенностью поверхностных слоев является постепенное изменение химического состава и физических свойств вещества вдоль толщины слоя, т.е. в процессе перехода от одной макроскопической фазы к другой.
Существует обширный класс макроскопических систем, в которых заметная доля вещества находится в составе таких межфазных граничных слоев (коллоидные системы). Поэтому отмеченные особенности состояния молекул в граничном слое существенно влияют на свойства и поведение коллоидных систем.
Дата добавления: 2015-10-21; просмотров: 71 | Нарушение авторских прав
| <== предыдущая страница | | | следующая страница ==> |
| Пространственные (геометрические) характеристики | | | Диссипативные КМС |