
Жүйенің математикалық моделін жасау үшін оның құрылымы: жүйені құрайтын элементтер және олардың өзара әсерлерінің сипаты – зерттеледі. Технологиялық процестер үшін ол оның механизмінің – химиялық реакция маршрутын, ағындардың қозғалу сипатын, жылу мен зат тасымалдау процестерін және химизм, гидравлика, жылу – және масса тасымалдаудың өзара әсерлерінің – шифрларын ашу болып табылады. Бұл этапта теңдеулер жалпы түрде алынады – оларға белгісіз коэффициенттер (реакция жылдамдықтарының коэффициенттері, жылу және масса тасымалдау коэффициенттері және т.б.) кіреді. Ол коэффициенттерді модельдің параметрлері деп атайды. Ол параметрлерді анықтау үшін эксперименттік зерттеулер жүргізіледі.
Математикалық модельді жасаудың эмпирикалық әдісі ("қара жәшік" әдісі). Бұл жағдайда жүйенің құрылымы белгісіз, қара жәшікте жасырылған деп есептелінеді. Оны тек жүйенің кіруі мен шығуы жүйеге кіргізілетін әсерлерге оның жауап беруі бойынша ғана білуге болады. Кірудің осындай өзгерісі мен жауап беруді анықтау эксперимент болып табылады. Алынған нәтижелер эмпирикалық теңдеулер жүйесімен сипатталады. Бұл теңдеулер жүйенің математикалық моделі болып табылады. Эмпирикалық әдістің артықшылығы – оның қарапайымдылығы, кемшілігі – зерделеген факторлардың және жүйенің жауап беру шектерінен тыс жерде экстраполяциялаудың сенімсіздігі. X, Y және U –жүйеге берілетін әсерлер, оларды "факторлар" деп атайды. Y –жүйенің қоршаған әлемге әсері, оның функциялануының (жұмыс істеуінің) нәтижесі (жүйенің лебізі шығуы немесе "шығымы, жауап беруі"). Жүйенің "лебізі" өндірілген өнім, оның сапасы, өзіндік құны, мекеменің табысы, түзілетін зиянды шығындылардың мөлшері және т.б. болуы мүмкін. Х және U-олар бақыланатын факторлар, яғни жүйе жұмыс істеу барысында берілетін немесе өлшенетін әсерлер. Х- ол бақыланатын, бірақ реттелмейтін факторлар. Мысалы, шикізат құрамы, өндірістік аппарат өлшемі (размері) және т.б. U- жүйені меңгеру (басқару) үшін белгілі бір бағытын өзгертіп, жүйеге әсер ететін факторлар ("меңгерілетін факторлар"). Бақыланбайтын факторлардың негізгі үш себебі болады:
1. Берілген факторлардың жүйеге айтарлықтай әсері туралы ақпараттардың жетіспеушілігі;
2. "Адам факторы" – ол жеке адам, оны осы жүйемеен жұмыс істегендегі көңіл-күй жағдайы.
3. Әсердің кездейсоқ сипаты-экспериментте ол тәжірибелердің кездейсоқ қателері, өндірісте режимнің кездейсоқ әсерлері ("шулары").

Жүйелік талдау – ол күрделі жүйелерді зерделеудің стратегиясы. Күрделі жүйелерге химиялық технологияның да, химиялық өндірістіің де процестері жатады. Оның зерттеу әдісі ретінде математикалық модельдеу пайдаланылады, ал оның негізгі принципі - күрделі жүйені қарапайым жүйешелерге декомпозициялау (жүйе иерархиясының принципі). Бұл кезде жүйенің математикалық моделі блоктық принциптен құралады: жалпы модель блоктарға бөлінеді, олардың математикалық сипаттамалары айтарлықтай қарапайым болады. Барлық жүйешелер өзара қарым-қатынаста болады да, бір математикалық модель құрайды.
Жүйелік талдау негізіне келесі ережелер жатады:
1. Зерттеу мақсатын нақты тұжырымдау;
2. Қойылған мақсатты жүзеге асыру үшін мәселелер қойып, мәселелерді шешудің тиімділік көрсеткіштерін (критерияларын) анықтау;
3. Негізгі этаптарды және мәселелердің шешу бағыттарын көрсете отырып, зерттеудің жайма жоспарларын әзірлеу;
4. өзара байланысты этаптардың барлық кешені бойынша пропоционалды-тізбектелген түрде алға жылжу;
5. Жеке этаптарда зерттеудің тізбектелген жуықтаулары мен қайталанатын циклдерді ұйымдастыру.
6. Құрамды жеке мәселелерді шешудегі синтездің төмендейтін иерархия принципі.
Реакторда жүретін химиялық процесті жүйелік талдау көмегімен зерттегенде бес блокты бөліп көрсетуге болады:

Алдымен процестің гидродинамикасы мен ағындардың құрылымын, содан соң жылу мен заттың тасымалдануының әсерін, одан кейін химиялық кинетиканы зерделейді де, материалдық және жылулық баланстарды жасайды. Жүйенің функциялануы (жұмыс істеуінің) математикалық сипаттау жалпы түрде теңдеулердің жүйесі түрінде болады:
 (4)
(4)
 функциясының түрін анықтау мүмкін емес, өйткені ол функцияның аргументтері (Z факторы кездейсоқ "шығымдар") белгісіздер. Алайда (4) теңдеуді мынадай түрде жазуға болады:
функциясының түрін анықтау мүмкін емес, өйткені ол функцияның аргументтері (Z факторы кездейсоқ "шығымдар") белгісіздер. Алайда (4) теңдеуді мынадай түрде жазуға болады:
 (5)
(5)
Енді процестің математикалық моделін жасау мәселесі F функциясының түрін анықтау және шумды  бағалаудан тұрады. Математикалық модель деп әдетте теңдеулер жүйесін айтады:
бағалаудан тұрады. Математикалық модель деп әдетте теңдеулер жүйесін айтады:
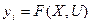 (6)
(6)
мұндағы шуды бағалауды бөліп жеке мәселе етеді. (6)- функцияның түрін құрылымдық тәсіл немесе эмпирикалық әдіспен табады.
Құрылымдық тәсілдегі математикалық сипаттаудың құрылымы. Математикалық модельдер негізделетін заңдар ол сақталу заңы, оның өрнегі баланстың теңдеулері болып табылады. Материалдық баланстың жалпыланған теңдеуі:
Заттың келуі - Заттың шығыны =Заттың жинақталуы (7)
Егер келу шығыннан көп болса, онда оң жинақталу байқалады. Стационарлық режимде (7) материалдық баланстың кәдімгі түріне көшеді.
Заттың келуі = заттың шығыны (8)
(7) және (8) теңдеулерді әрбір затқа және заттардың жиынтығына қолдануға болады. Жылу энергиясы үшін жылулық баланстың жалпыланған теңдеуі былай жазылады:
Жылудың келуі – жылудың шығыны = жылудың жинақталуы (9)
Стационарлық режимде ол жылулық баланстың кәдімгі теңдеуіне айналады.
Жылудың келуі = Жылудың шығыны (10)
(9) және (10)- теңдеулердегі терминдер дұрыс емес, өйткені көбейетін және азаятын жылудың емес, энтальпияның мөлшері.
Химия-технологиялық процестің құрылымының күрделі болатындығы оның құрайтын элементарлық процестердің әртүрлі деңгейде: төменнен (молекула деңгейі) жоғарыға дейін (цех немесе зауыт деңгейі) жүретіндігінен.
Процестің деңгейліктілігін сипаттау әдістері – ол математикалық модельдің иерархиялық құрылымы.
1. Молекулалық деңгей – молекулалар арасындағы қашықтық масштабында жүретін процестерді сипаттау. Бұл деңгейде химиялық кинетиканың (микрокинетика) заңдылықтары орындалады.
2. Кіші көлемдік деңгей – ол катализатордың бір түйірінде, немесе реакциялық көлемге барботирленентін газдың бір көпіршігінде жүретін процестер. Бірінші деңгейдегі заңдылықтар осы масштабтағы болатын жылу және массатасымалдау процестерінің заңдылықтарымен толығады. Бұл жағдайдағы кинетикалық заңдылықтарды талдау – макрокинетиканың мәселесі.
3. Аппараттық жұмыстың аймағының (зонасының) деңгейі (катализатор қабаты, барботаждық қабат және т.б.) – ағындардың қозғалыстарының заңдылықтарымен анықталады.
4. Аппарат деңгейі –жұмыс аймақтарының (зоналарының) саны, конфигурациясы, өзара байланысты және өзара орналасуы еске алынады. Мысалы, аппарат катализатордың бірнеше қабаттарынан тұруы мүмкін, олардың араларында аралық жылу алмастырғыштар орналасады.
5. Агрегат деңгейі – аппараттардың өзара байланыстары еске алынады.
Әрбір жоғары деңгейдің моделі төменгі деңгейлердің модельдерінен және бір деңгейдеен басқа деңгейге көшуді сипаттайтын қарым-қатынастардан тұрады. Бірінші деңгейдегі иерархиялық құрылымда модельдеу стехиометрия, химиялық тепе-теңдік және кинетиканы сипаттаудан құралады [1].
3. СТЕХИОМЕТРЛІК БАЛАНС ТЕҢДЕУІ.
Химиялық реакцияның стехиометрлік теңдеуі реакцияның материалдық балансының қысқаша өрнегі болып табылады:
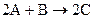 (1)
(1)
мұндағы заттың мөлшері, моль арқылы өрнектеледі. (1)- реакцияның кез-келген уақыт үшін стехиометрлік балансының теңдеулері:

 (2)
(2)
 (3)
(3)
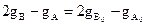 (4)
(4)
мұндағы А0, В0, С0 –А,В,С заттарының бастапқы мөлшері.
Стехиометрлік баланс теңдеуі реакцияланатыын заттардың стехиометрлік эквиваленттілігін көрсетеді. (1)-реакция үшін эквиваленттілік мына қарым-қатынаспен анықталады. А~B~2C (5).
Бір сатылы реакция үшіін эквиваленттілік қарым –қатынастарағы (5) коэффиценттер өзара тең немесе баланс теңдеулеріндегі (2-4) коэффиценттерге пропорционал болады. (2-4) теңдеулерінің сол жақтары реакция барысында өзгермейді, сондықтан оларды реакцияның инварианттары, ал көп сатылы реакциялар үшін реакция жүйесінің инварианттары деп атайды. Стехиометрлік баланс теңдеулері (немесе инварианттар) материалдық баланс теңдеулеріне кіретін белгісіздердің саны азайғандағы есептеу мәселелері шешуге мүмкіндік береді. Мысалы, (2-4) теңдеулерінен мыналар шығады:
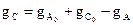 (6)
(6)
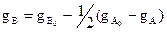 (7)
(7)
(6) және (7) – теңдеулер есептеулерден 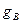 мен
мен  -ны шығарып тастайды да, оларды
-ны шығарып тастайды да, оларды  және бастапқы жағдайлармен өрнектейді. Мәселені шешкенде реакцияның қайтымдылығы еске алынбайды, өйткені стехиометрлік баланстар қайтымдылыққа тәуелсіз болады.
және бастапқы жағдайлармен өрнектейді. Мәселені шешкенде реакцияның қайтымдылығы еске алынбайды, өйткені стехиометрлік баланстар қайтымдылыққа тәуелсіз болады.
Дата добавления: 2015-09-03; просмотров: 673 | Нарушение авторских прав
| <== предыдущая страница | | | следующая страница ==> |
| Модельдеу тәсілдері | | | Реакцияның тәуелсіз сатыларын анықтаудағы стехиометрлік коэффиценттерінің матрицасы |