
|
Читайте также: |
Угол диаграммы состояния двойной системы, в которой примесь (растворенное вещество) понижает температуру плавления растворителя, воспроизводится в виде схемы на фиг. 2.1,а.
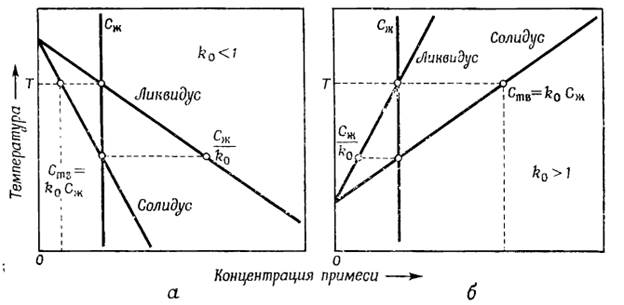
Фиг. 2.1. Углы диаграмм состояния систем, когда примесь понижает (а) и повышает (б) температуру затвердевания растворителя.
Раствор, содержащий примесь в концентрации Сж, существует при температурах выше линии ликвидуса только в жидком состоянии. Если этот раствор медленно охладить до температуры T, лежащей непосредственно ниже линии ликвидуса, то он начнет затвердевать. Первый образующийся кристалл растворителя будет содержать примесь в твердом растворе с концентрацией Ств, которую находят по точке пересечения температурной горизонтали с нижней кривой, называемой линией солидуса. Равновесный коэффициент распределения 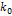 есть отношение
есть отношение 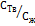 , взятое из диаграммы состояния. На фиг. 2.1, а коэффициент распределения
, взятое из диаграммы состояния. На фиг. 2.1, а коэффициент распределения 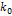 имеет величину меньше единицы, так как кривые ликвидуса и солидуса идут вниз. Соответствующая диаграмма состояния для примеси, повышающей температуру плавления растворителя и, следовательно, дающей коэффициент распределения
имеет величину меньше единицы, так как кривые ликвидуса и солидуса идут вниз. Соответствующая диаграмма состояния для примеси, повышающей температуру плавления растворителя и, следовательно, дающей коэффициент распределения 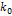 больше единицы, показана на фиг. 2.1, б.
больше единицы, показана на фиг. 2.1, б.
Рассмотрим полное затвердевание такого раствора, о котором речь шла в связи с фиг. 2.1, а. Для большей конкретности представим себе раствор в виде протяженного цилиндра, затвердевающего с одного конца, как это схематически изображено на фиг. 2.2.
Назовем эту операцию нормальной кристаллизацией. Форма твердой фазы не играет никакой роли, а интерес представляет лишь доля вещества, успевшего затвердеть к определенному моменту времени.
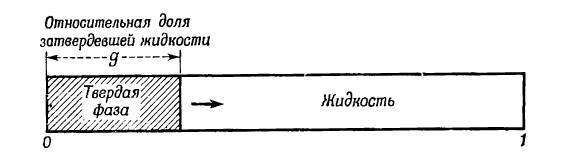
Фиг. 2.2. Схема затвердевания при нормальной кристаллизации.
Распределение примеси между твердой и жидкой фазами при затвердевании и во всей твердой фазе после затвердевания зависит не только от величины коэффициента распределения 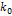 , но и от условий затвердевания. Самым важным таким условием является скорость затвердевания, т.е. скорость перемещения фронта кристаллизации. Почти столь же важное значение имеет степень перемешивания жидкости. В зависимости от этих условий процесс распределения примеси протекает тремя- четырьмя различными путями. Одним из таких предельных случаев является равновесное затвердевание, которое происходит только тогда, когда градиентами концентрации и температуры в системе можно пренебречь. Это предполагает настолько малую скорость затвердевания, что в процессе диффузии в твердой и жидкой фазах все градиенты концентрации успевают выровняться. Поскольку в системе на фиг. 2.1, а происходит равновесное затвердевание, концентрация примеси в твердой фазе всегда равна произведению концентрации примеси в жидкой фазе и коэффициента распределения
, но и от условий затвердевания. Самым важным таким условием является скорость затвердевания, т.е. скорость перемещения фронта кристаллизации. Почти столь же важное значение имеет степень перемешивания жидкости. В зависимости от этих условий процесс распределения примеси протекает тремя- четырьмя различными путями. Одним из таких предельных случаев является равновесное затвердевание, которое происходит только тогда, когда градиентами концентрации и температуры в системе можно пренебречь. Это предполагает настолько малую скорость затвердевания, что в процессе диффузии в твердой и жидкой фазах все градиенты концентрации успевают выровняться. Поскольку в системе на фиг. 2.1, а происходит равновесное затвердевание, концентрация примеси в твердой фазе всегда равна произведению концентрации примеси в жидкой фазе и коэффициента распределения 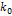 . Поскольку при затвердевании примесь оттесняется в жидкость, ее концентрации в жидкости и в затвердевающей части непрерывно возрастают. Последняя капля жидкости затвердевает тогда, когда концентрация примеси в ней достигает величины
. Поскольку при затвердевании примесь оттесняется в жидкость, ее концентрации в жидкости и в затвердевающей части непрерывно возрастают. Последняя капля жидкости затвердевает тогда, когда концентрация примеси в ней достигает величины 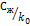 , где Сж — начальная концентрация. Основное различие между равновесным затвердеванием и рассматриваемыми ниже процессами состоит в том, что при равновесном затвердевании благодаря диффузии в твердой фазе все время поддерживается одинаковая концентрация примеси, несмотря на то, что эта концентрация непрерывно возрастает. На практике равновесное затвердевание редко достигается, так как скорость диффузии в твердом состоянии обычно мала.
, где Сж — начальная концентрация. Основное различие между равновесным затвердеванием и рассматриваемыми ниже процессами состоит в том, что при равновесном затвердевании благодаря диффузии в твердой фазе все время поддерживается одинаковая концентрация примеси, несмотря на то, что эта концентрация непрерывно возрастает. На практике равновесное затвердевание редко достигается, так как скорость диффузии в твердом состоянии обычно мала.
Хотя равновесное затвердевание не приводит к сегрегации или разделению в затвердевшем слитке, оно все же делает возможным разделение за счет отделения твердой части в тот или иной момент процесса. В предельном случае степень очистки равна равновесному коэффициенту распределения 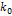 , но это верно лишь для бесконечно малого количества твердой фазы, отделенного в самом начале процесса. В условиях равновесного затвердевания концентрация примеси в твердой фазе после затвердевания доли
, но это верно лишь для бесконечно малого количества твердой фазы, отделенного в самом начале процесса. В условиях равновесного затвердевания концентрация примеси в твердой фазе после затвердевания доли 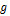 исходного объема жидкости выражается соотношением
исходного объема жидкости выражается соотношением
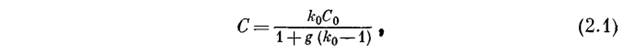
где 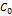 — начальная концентрация примеси в жидкости.
— начальная концентрация примеси в жидкости.
Дата добавления: 2015-08-20; просмотров: 178 | Нарушение авторских прав
| <== предыдущая страница | | | следующая страница ==> |
| НОРМАЛЬНАЯ КРИСТАЛЛИЗАЦИЯ И КОЭФФИЦИЕНТ РАСПРЕДЕЛЕНИЯ | | | Сегрегация при нормальной кристаллизации |