
Читайте также:
|
10.1. Определите составные части комплексных соединений: внешнюю и внутреннюю координационные сферы, комплексообразователь, его к.ч., лиганды:
01. [ Со(NO3)2(NH3)4 ] Cl 16. [ Pt(NH3)4 ] SO4
02. K3 [ Fe(CN)6 ] 17. [ Co(H2O)6 ] Cl3
03. [ Pt(NH3)4SO4 ] Br  18. Ba [ Pt(NO2)4Cl2 ]
18. Ba [ Pt(NO2)4Cl2 ]
04. [ Cu(NH3)4 ] SO4 19. [ Co(NH3)6 ] I3
05. K4 [ Fe(CN)6 ] 20. [ Co(NH3)6 ] Cl3
06. [ Os(NH3)6 ] Br3 21. [ Co(NH3)5I ] I2
07. [ Co(NH3)5Br ] SO4 22. [ Zn(NH3)4 ] Cl2
08. Ba [ Cr(NH3)2(SCN)4 ] 2 23. [ Ag(NH3)2 ] OH
09. [ Pd(NH3) C l ] Cl 24. [ Co(NH3)4I2 ] I
10. [ Co(NH3)5(H2O) ] Cl3 25. [ Al(H2O)6 ] Cl3
11. [ Pt(NH3)4(OH)2 ] SO4 26. [ Co(NH3)  SO4 ] Br
SO4 ] Br
12. [ Cu(NH3)2 ] OH 27. [ Pt(NH3)6 ] Cl4
13. [ Co(NH3)5Cl ] Cl2 28. [ Fe(H2O)6 ] SO4
14. [ Cr(H2O)5Cl ] Cl2 29. [ Ni(NH3)6 ] SO4
15. [ Ti(H2O)6 ] Br3 30. [ Be(NH3)4 ] Cl2
10.2. Назовите комплексные соединения, указанные в разделе 10.1.
10.3. Напишите уравнения диссоциации и выражение константы 
нестойкости комплексных соединений, указанных в разделе 10.1.
10.4. Обоснуйте выбор комплексообразователя, лигандов и составьте формулы комплексных соединений, имеющих состав:
01. Ca2+, Pt+4,  к.ч.=6 16. Ag+, NH3, NO3- к.ч.=2
к.ч.=6 16. Ag+, NH3, NO3- к.ч.=2
02. Co3+, NH3,  к.ч.=6 17. Ni2+, NH3, SO42- к.ч.=6
к.ч.=6 17. Ni2+, NH3, SO42- к.ч.=6
03. Na+, Zn2+, OH - к.ч.=4 18. Cu2+, H2O, NO3- к.ч.=4
04. K+, Be2+, F - к.ч.=4 19. K+, Al3+,  к.ч.=6
к.ч.=6
05. K+, Cr3+, CN - к.ч.=6 20. K+, Al3+,  к.ч.=4
к.ч.=4
06. Cr3+, H2O,  к.ч.=6 21. K+, Pb2+,
к.ч.=6 21. K+, Pb2+,  к.ч.=4
к.ч.=4
07. Co3+, H2O,  к.ч.=4 22. Pt4+, NH3,
к.ч.=4 22. Pt4+, NH3,  к.ч.=6
к.ч.=6
08. Na+, Ag+,  к.ч.=623. Fe3+, H2O,
к.ч.=623. Fe3+, H2O,  к.ч.=6
к.ч.=6
09. Mg2+, Be2+,  к.ч.=4 24. K+, Hg2+,
к.ч.=4 24. K+, Hg2+, 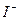 к.ч.=4
к.ч.=4
10. Ni2+, NH3,  к.ч.=6 25. K+, Ni2+,
к.ч.=6 25. K+, Ni2+,  к.ч.=6
к.ч.=6
11. H+, Si+4,  к.ч.=6 26. K+, Pb2+,
к.ч.=6 26. K+, Pb2+, 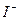 к.ч.=4
к.ч.=4
12. Co3+, NH3, 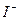 к.ч.=4 27. Na+, Al3+,
к.ч.=4 27. Na+, Al3+,  к.ч.=6
к.ч.=6
13. K+, Fe3+,  к.ч.=6 28. Cd2+, NH3,
к.ч.=6 28. Cd2+, NH3,  к.ч.=4
к.ч.=4
14. K+, Fe2+,  к.ч.=6 29. Pt4+, NH3,
к.ч.=6 29. Pt4+, NH3,  к.ч.=6
к.ч.=6
15. K+, Cr3+,  к.ч.=6 30. Na+, Be2+,
к.ч.=6 30. Na+, Be2+,  к.ч.=4
к.ч.=4
10.5. Напишите химические формулы комплексных соединений:
1. нитрат динитротетрамминкобальта (ІІІ);
2. дицианоаргентат (І) натрия;
3. дихлородиамминплатина;
4. трихлоротриамминкобальт;
5. хлорид гексамминкобальта (ІІІ);
6. гексанитрокобальтат (ІІІ) калия;
7. хлорид гексамминникеля (ІІ);
8. гексацианоферрат (ІІ) калия;
9. гексацианоферрат (ІІІ) калия;
10. трифторогидроксобериллат (ІІ) магния;
11. гексацианохромат (ІІІ) калия;
12. бромид гексамминкобальта (ІІІ);
13. иодид бромопентаммминкобальта (ІІІ);
14. тетрахлородиамминплатина;
15. гексагидроксоалюминат калия;
16. сульфат карбонатотетрамминхрома (ІІІ);
17. нитрат дибромотетраквахрома (ІІІ);
18. нитрат диакватетраамминникеля (ІІ);
19. трифторотриаквакобальт;
20. тринитротриамминкобальт;
21. тетрароданодиамминхромат (ІІІ) натрия;
22. тетрабромоплатинат (ІІ) калия;
23. пентацианоамминферрат (ІІ) натрия;
24. тетраиододиамминплатина;
25. тригидроксотриамминкобальт;
26. хлоридтетраамминцинка;
27. тетрафторобериллат (ІІ) калия;
28. тетрагидроксоцинкат натрия;
29. дицианоаргентат (І) водорода;
30. гексафторосиликат (ІV) водорода.
10.6. Запишите молекулярные и ионно-молекулярные уравнения
реакций ионного обмена:
01. [ Co(NO3)2(NH3)4 ] Cl + AgNO3
02. K3 [ Fe(CN)6 ] + FeSO4
03. [ Pt(NH3)4 SO4 ] Br2 + AgNO3
04. [ Cu(NH3)4 ] SO4 +BaCl2
05. K4 [ Fe(CN)6 ] + FeCl3
06. [ Os(NH3)6 ] Br3 + AgNO3
07. [ Co(NH3)5Br ] SO4 +BaCl2
08. Ba [ Cr(NH3)2(SCN)4 ] 2 + Na2SO4
09. [ Pd(NH3) C l ] Cl + AgNO3
10. [ Co(NH3)5(H2O) ] Cl3+ AgNO3
11. [ Pt(NH3)4(OH)2 ] SO4 +BaCl2
12. [ Cu(NH3)2 ] OH + MnCl2
13. [ Co(NH3)5Cl ] Cl2+ AgNO3
14. [ Cr(H2O)5Cl ] Cl2+ AgNO3
15. [ Ti(H2O)6 ] Br3+ AgNO3
16. [ Pt(NH3)4 ] SO4 +Ba(NO3)2
17. [ Co(H2O)6 ] Cl3+ AgNO3
18. Ba [ Pt(NO3)4Cl2 ] + Na2SO4
19. [ Co(NH3)6 ] I3 +Pb(NO3)2
20. [ Co(NH3)6 ] Cl3+ AgNO3
21. [ Co(NH3)5I ] I2+ AgNO3
22. [ Zn(NH3)4 ] Cl2+ AgNO3
23. [ Ag(NH3)2 ] OH+CuCl2
24. [ Co(NH3)4I2 ] I+ AgNO3
25. [ Al(H2O)6 ] Cl3+ AgNO3
26. [ Co(NH3)4SO4 ] Br+ AgNO3
27. [ Pt(NH3)6 ] Cl4 + AgNO3
28. [ Fe(H2O)6 ] SO4+BaCl2
29. [ Ni(NH3)6 ] SO4+Ba(NO3)2
30. [ Be(NH3)4 ] Cl2+ AgNO3
10.7. При добавлении к раствору комплексного соединения 1 раствора вещества 2 образуется новое комплексное соединение. Объясните протекание данной реакции, сравнив константы нестойкости комплексов. Для ответа на вопрос используйте данные табл.6 «Таблицы основных свойств элементов и их соединений», Тюмень, 2007 г. Напишите молекулярное и ионно-молекулярные уравнения реакций получения нового комплексного соединения.
| Вариант | Раствор комплексного соединения 1 | Раствор вещества 2 |
| K2[HgCl4] | KCNS | |
| K2[HgI4] | KCNS | |
| [Hg(NH3)4](NO3)2 | KI | |
| K2[HgCl4] | KI | |
| K2[HgCl4] | KCN | |
| K2[CdCl4] | KCN | |
| [Cd(NH3)4]Cl2 | KCN | |
| K2[CdI4] | KCN | |
| [Ag(NH3)2]NO3 | KCN | |
| [Ag(NH3)2]Cl | KI | |
| K3[AgCl4] | KCN | |
| K3[AgCl4] | KSCN | |
| [Co(NH3)6](NO3)3 | KCN | |
| K3[Fe(SCN)6] | KCN | |
| K3[AlF6] | KCN |
Дата добавления: 2015-07-25; просмотров: 184 | Нарушение авторских прав
| <== предыдущая страница | | | следующая страница ==> |
| Тюмень 2010 | | | А) простые вещества б) сложные вещества |