
|
Читайте также: |
Средние соли – продукты полного замещения атомов водорода в молекуле кислоты атомами металла:
2NaOH + H2SO4 = Na2SO4 + 2H2O
сульфат натрия или
тетраоксосульфат (Vl) натрия
 С точки зрения теории электролитической диссоциации средние соли это электролиты, которые диссоциируют в водных растворах или расплавах на катионы металла (или катион аммония) и анионы кислотного остатка:
С точки зрения теории электролитической диссоциации средние соли это электролиты, которые диссоциируют в водных растворах или расплавах на катионы металла (или катион аммония) и анионы кислотного остатка:
Na2SO4 = 2Na+ + SO42-
Ca3(PO4)2 = 3Ca 2+ + 2PO43-
Названия солей тесно связаны с номенклатурой соответствующих кислот. Для солей распространенных кислот сохраняются традиционные названия: Na2SO4 – сульфат натрия (тетраоксосульфат(VI) натрия), KNO3 – нитрат калия (триоксонитрат (V) калия), K3PO4 – ортофосфат калия (тетраоксофосфат(V) калия), K2CO3 – карбонат калия триоксокарбонат (IV) калия), KMnO4 – пермaнганат калия (тетраоксоменганат (VII) калия), Li2CrO4 – хромат лития (тетраоксохромат (VI) лития).
Для солей кислородсодержащих кислот хлора, иода и некоторых других кислот, в которых кислотообразуюший элемент имеет несколько степеней окисления, а также для солей полимерных и других сложных кислот, в правилах ИЮПАК рекомендуется применять систематические названия (традиционные русские названия – в скобках): KClO – оксохлорат калия (гипохлорит калия) KClО3 – триоксохлорат калия (хлорат калия), KСlO4 тетраоксохлорат калия (перхлорат калия), Na6TeO6 – гексаоксотеллурат гексанатрия (ортотеллурат натрия).
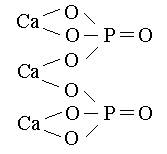
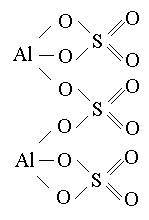
Графические формулы средних солей:
Na2CO3 AlPO4
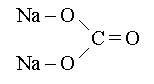
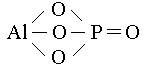
NaNO3 CaCl2
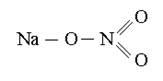
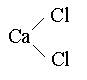
Al2(SO4)3 Ca3(PO4)2
Дата добавления: 2015-07-25; просмотров: 80 | Нарушение авторских прав
| <== предыдущая страница | | | следующая страница ==> |
| Химические свойства. | | | Химические свойства. |