
Читайте также:
|
Основания и кислородсодержащие кислоты содержат связь R–ОН, где R – атом элемента или атом, к которому присоединены другие группы (например, NH4-, CH3COO-).
. Различают основной и кислотный тип диссоциации:
ROH «R++ OH-(основной тип диссоциации);
НОR«H+ + RO- (кислотный тип диссоциации).
При электролитической диссоциации происходит разрыв связей с наибольшей степенью ионности. Чем больше разность относительных электроотрицательностей (ОЭО) элементов, образующих связь, тем сильнее связь поляризована, т.е. тем большую степень ионности она имеет и тем легче диссоциирует на ионы. Например, в соединении NaOH разность ОЭО кислорода и натрия (DОЭОO-Na) равна:
3,5 - 0,9 = 2,6.
Разность ОЭО кислорода и водорода (DОЭОО-Н) равна:
3,5 - 2,1 = 1,4.
Степень ионности связи Na-О больше, чем у связи О-Н. Поэтому едкий натр диссоциирует по основному типу и является типичным основанием: NaOH = Na++ OH-.
В соединении HClO4: DОЭОО-Сl = 3,5 - 3,0 = 0,5;
DОЭОО-Н = 3,5 - 2,1 = 1,4.
Степень ионности связи Cl - O меньше, чем связи О - Н.
Соединение HClO диссоциирует по кислотному типу и является типичной кислотой:
HClO4 = H++ ClO4-.
Если степени ионности связей О-R и О-Н сравнимы по величине, электролиты проявляют свойства и кислоты, и основания, т.е. имеют двойственный характер диссоциации. В нейтральной среде у таких электролитов устанавливается сложное равновесие:
H++ RO- «R - O - H «R++ OH-
кислотный тип основной тип
диссоциации диссоциации
Основаниями (гидроксидами) с точки зрения электролитической диссоциации называются электролиты, которые в качестве анионов образуют только анионы гидроксила (гидроксоанионы) ОН-:
NaOH = Na+ + OH-.
NH4 ОН «NH4++ OH-.
Основания многовалентных металлов диссоциируют ступенчато, а значит, такие гидроксиды будут иметь несколько констант диссоциации – для каждой ступени (стадии) свою.
Например: Ba(OH)2 «BaOH++ OH-(1 ступень),
ВаОН+ «Ва2++ ОН- (2 ступень).
Кислотами, с точки зрения электролитической диссоциации, называются электролиты, которые в качестве катионов образуют только катионы водорода Н+:
HNO3 = H++ NO3-,
CH3COOH «H++ CH3COO-.
Многоосновные слабые кислоты диссоциируют ступенчато, а значит, такие кислоты будут иметь несколько констант диссоциации – для каждой ступени (стадии) свою.
Например: H3РO4 «H++ H2РO4- (1 ступень)
К1 =  = 7,5.10-3,
= 7,5.10-3,
H2РO4- «H++ HРO42- (2 ступень),
К2 =  = 6,2.10-3,
= 6,2.10-3,
HРO42- «H++ РO43- (3 ступень),
К3 = 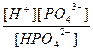 = 2,2.10-3.
= 2,2.10-3.
Всегда К1 > К2 > К3, т.е. многоосновная кислота при диссоциации по первой ступени ведет себя как более сильная кислота, чем по второй и третьей.
Амфотерные электролиты с точки зрения электролитической диссоциации участвуют в сложных ионных равновесиях, в которых образуются и катионы водорода, и анионы гидроксила, т.е. амфотерные электролиты в водных растворах в зависимости от характера среды могут диссоциировать и по типу основания, и по типу кислоты. Например, гидроксид цинка диссоциирует в кислой среде по типу основания:
Zn(OH)2 «ZnOH++ OH- «Zn2+ + 2OH-,
а в щелочной среде - по типу кислоты:
H2ZnO2 «H++ HZnO2- «2H++ ZnO22-.
К амфотерным электролитам относятся: гидроксид цинка Zn(OH)2; гидроксид свинца Pb(OH)2; гидроксид олова Sn(OH)2; гидроксид аллюминия Al(OH)3; гидроксид хрома Cr(OH)3 и др.
Солями с точки зрения электролитической диссоциации, называются электролиты, которые диссоциируют с образованием катионов металла (или аммония NH4+) и анионов кислотного остатка:
NaNO3 = Na+ + NO3-.
CaCl2 = Ca2++ 2Cl-,
K3PO4 = 3К+ + РО43-,
NH4Cl= NH4++ Cl-.
Кислые соли (продукты неполного замещения атомов водорода кислоты на металл) диссоциируют по ступеням. Например:
NaHCO3 = Na++ HCO3- (1 ступень),
HCO3- «H+ + CO32- (2 ступень).
Основные соли (продукты неполного замещения гидроксильной группы основания на кислотный остаток) также диссоциируют по ступеням:
Mg(OH)Cl = Mg(OH)++ Cl- (1 ступень),
Mg(OH)+ «Mg2+ + OH- (2 ступень).
Дата добавления: 2015-07-10; просмотров: 214 | Нарушение авторских прав