
Читайте также:
|
Венозный тромбоз — острое заболевание, характеризующееся образованием тромба в просвете вены с более или менее выраженным воспалительным процессом и нарушением тока крови. Наличие воспалительного компонента в зоне тромбоза определяет другое название этой болезни — тромбофлебит.
Для возникновения тромбоза в вене необходимо три условия, сформу-
лированных еще в XIX в. (триада Вирхова): замедление тока крови, изменение ее состава и повреждение сосудистой стенки, однако значение каждого из этих факторов в патогенезе различных форм флеботромбоза может быть разным.
Данное осложнение достаточно часто встречается в послеоперационном периоде, составляя в среднем 27—30 %. Важность профилактики, ранней диагностики и лечения фле-
ботромбозов обусловлена тем, что у 2—10 % больных на фоне венозного тромбоза развивается такое грозное осложнение, как тромбоэмболия легочной артерии (ТЭЛА), причем в 0,26 % случаев она становится причиной смерти. ТЭЛА и тромбоз глубоких вен как состояния, имеющие общие патогенетические корни, объединяют в понятие венозного тром-боэмболизма (тромбоэмболические осложнения — ТЭО). Число больных с ТЭО основного заболевания растет с каждым годом. В США ежегодно регистрируется около 50 тыс., в Германии — 10 тыс. летальных исходов ТЭЛА. 45—95 % больных, перенесших распространенный тромбоз глубоких вен нижних конечностей, страдают выраженными формами хронической венозной недостаточности, что ограничивает их социальную активность. По данным A.N.Nicolaides и соавт. (1997), венозные трофические язвы возникают примерно у 500 пациентов из 100 000, перенесших тромбоз глубоких вен.
Статистика послеоперационных венозных ТЭО поистине угрожающая. B.Bergqist (1996), обобщивший значительное количество диагностических исследований с меченым фибриногеном, установил, что после различных общехирургических оперативных вмешательств тромбоз глубоких вен (ТГВ) нижних конечностей наблюдается в среднем у 29 % больных. У пациентов травматологического и ортопедического профиля частота венозных тромбозов еще выше. После операций по поводу перелома бедра тромбоз наблюдается в 53 % случаев, причем более чем у половины пациентов он возникает не только в пораженной, но и в здоровой конечности.
В этиологии венозных тромбозов важное значение придают травме, в том числе операционной, воспалению или изменению эндотелия в ответ на инфекционный раздражитель, повышению активности свертыва-
ющей и снижению функции проти-восвертывающей систем крови, нарушению нервной регуляции сосудистого тонуса и лимфатического оттока.
Патофизиология регионарной и общей гемодинамики. Считается, что наиболее часто (до 81 %) местом первичной локализации флеботромбоза являются мышечные ветви вен голеней. Установлено, что в 1/3—1/2 случаев на протяжении 2—3 сут они подвергаются спонтанному лизису и, как правило, клинически не проявляются. Примерно у 40 % больных зона флеботромбоза стабилизируется в размерах или уменьшается. В 7—20 % случаев тромбоз распространяется проксимальнее подколенной ямки, приводя к поражению илеофемо-рального сегмента и тазовых вен с развитием ТЭЛА у 44 % больных.
Второй по частоте локализацией первичного тромботического аффекта являются тазовые вены. Тромбоз чаще всего возникает после родов, абортов и операций на органах малого таза. Далее его распространение идет на общую подвздошную вену и в особо неблагоприятных случаях — на илиокавальный сегмент. Возможен и первичный тромбоз илиофе-морального сегмента и нижней полой вены, который чаще всего обусловлен наличием внутрисосудистых факторов. К ним относятся спайки в подвздошных венах, аномалии нижней полой вены в виде наличия диафрагм, перегородок, атрезий. Наиболее часто внутрисосудистые венозные спайки располагаются в левых подвздошных венах на уровне их перекреста с артериями. Врожденные перегородки находятся между боковыми (медиальной и латеральной) стенками вены, гистологически в них различимы все слои венозной стенки. Приобретенные перегородки локализуются только между передней и задней стенками вены и состоят из соединительной ткани, покрытой эндотелием, имеются признаки воспалительного процесса. Образо-
вание приобретенных перегородок сходно с адгезивным процессом, однако спайки более локализованы и не склонны к распространению.
Классификация острых венозных тромбозов. По клиническому течению флеботромбозов выделяют три стадии: острую, подострую и хроническую. Спорным остается вопрос о сроке, в течение которого флеботромбоз следует считать острым. В настоящее время, по мнению большинства авторов, критериями флеботромбоза как острого процесса считается возможность выполнения во время хирургического вмешательства тромб-эктомии без повреждения внутренней оболочки сосуда и повторного ретромбоза. Продолжительность этой стадии индивидуальна у различных больных и может колебаться от нескольких дней до 1 мес. По мнению А.А.Шалимова, острая стадия продолжается 7—14 дней, затем она переходит в подострую, и через 3 мес начинается хроническая стадия.
Подробной классификацией, учитывающей основные этиологические и клинические стороны флеботромбозов, является классификация Л.И.Клионера (1969).
А. По локализации первичного тром-ботического процесса и путям его распространения.
1. Система нижней полой вены:
а) вены, дренирующие вены мыш
цы голени;
б) илиофеморальный сегмент;
в) подпочечный, почечный, надпо
чечный сегменты или весь ствол
нижней полой вены;
г) сочетанный каваилиофемораль-
ный отдел;
д) сочетанный тотальный тромбоз
всей глубокой венозной системы
нижней конечности.
2. Система верхней полой вены.
Б. По этиологическому признаку. Тромбы в результате:
• инфекций;
• травм;
• операций;
• родов;
• варикозно измененных вен;
• аллергических состояний и обменных нарушений;
• интравазальных врожденных и приобретенных факторов (перегородки, спайки, диафрагмы, ат-резии);
• экстравазальных врожденных и приобретенных факторов (сдавле-ние венозной стенки артериями, опухолями, аневризмами аорты).
В. По клиническому течению:
• острый флеботромбоз;
• подострый флеботромбоз;
• посттромбофлебитический синдром (ПТФС);
• острый тромбофлебит, развившийся на фоне ПТФС.
Г. По степени возникновения трофических нарушений и расстройств гемодинамики:
• легкая форма;
• средняя форма;
• тяжелая форма.
В практической флебологии до сих пор используется классификация, предложенная В.С.Савельевым в 1972 г.
1. По локализации:
• тромбоз магистральных вен нижних конечностей — нижний сегмент;
• тромбоз наружной и общей подвздошной вен — средний сегмент;
• тромбоз нижней полой вены — верхний сегмент.
2. По этиологическому фактору: первичный и врожденный.
3. По клиническому течению: стадия компенсации и стадия декомпенсации.
Клиника флеботромбоза при различной локализации процесса. Острый тромбоз глубоких вен голени. Острый тромбоз магистральных вен нижних конечностей чаще всего начинается в глубоких венах голени и распространяется в проксимальном направлении. Клинические признаки тромбоза данной локализации обычно выражены незначительно вследствие хорошего коллатерального кровотока по остальным венам голени, выраженные нарушения гемодинамики в пораженной конечности при этом отсутствуют. Типичный признак острого тромбоза глубоких вен голени — болезненность икронож-
ных мышц при пальпации. Показателен симптом Хоманса, суть которого заключается в появлении резкой боли в икроножной мышце при тыльном сгибании стопы. Проба Ле-венберга также основана на возникновении боли в икроножных мышцах, но при сдавлении их манжеткой аппарата Рива-Роччи, наложенной на проксимальную часть голени при давлении 140—150 мм рт.ст. Проба Мозеса заключается в сравнительном исследовании характера ощущений больного при пальпации икроножных мышц вначале путем охваты-вания кистью со сдавлением боковых поверхностей, а затем глубокой пальпации II—IV пальцами по ходу сосудистого пучка. При пальпации сосудистого пучка интенсивность боли существенно увеличивается, что свидетельствует в пользу флеботромбо-за. Второй клинический признак заболевания — отечность дистальных отделов голени — достаточно постоянный симптом. Выраженность его зависит от распространенности тромбофлебита в глубоких венах голени. Так, при вовлечении в тромботичес-кий процесс vv.tibialis anterior и posterior, а также vv.peronea или подколенной вены на первый план выступает нарушение венозного оттока из пораженной конечности. Голень становится отечной, больные жалуются на чувство распирания, напряжения вен. При тромбозе подколенной вены отмечаются сглаженность контуров коленного сустава, болезненность при движении, обусловленная реакцией синовиальной оболочки и асептическим воспалением сустава. При распространении тром-ботического процесса на поверхностную бедренную вену с окклюзией ее просвета тромбом обычно выраженного отека бедра не бывает, но имеется ноющая боль по внутренней поверхности бедра. В целом клиническая диагностика острого тромбоза магистральных вен дистальных отделов нижних конечностей достаточно трудна из-за частой невыраженности
и неспецифичности клинических симптомов, схожести клинической картины с другими заболеваниями.
Острый тромбоз общей бедренной вены. При распространении тромбоза в проксимальном направлении клиническая картина заболевания становится ярче, появляются признаки выраженных нарушений гемодинамики (отечность, боль распирающего характера, цианоз кожных покровов) в венах пораженной конечности и таза. Выраженность этих симптомов зависит от степени компенсации коллатерального кровотока. Острый тромбоз общей бедренной вены может быть следствием как распространения тромбоза с поверхностной бедренной вены, так и первичной локализации в ней. В первом случае отмечают внезапный диффузный отек голени и бедра, цианоз, более выраженные на периферии. Через 2—4 дня отек начинает постепенно уменьшаться, но в верхней трети бедра возможно появление расширенных поверхностных вен, что свидетельствует о включении в кровоток новых путей коллатерального оттока. При локализации тромбоза выше устья большой подкожной вены с ее блокадой в коллатеральный кровоток включаются vv.pudendae ext, анастомозирующие с одноименными венами противоположной стороны.
Для первичного тромбоза общей бедренной вены характерна внезапная острая боль в верхней трети передней поверхности бедра и паховой области, после чего появляются отек нижней конечности вплоть до паховой складки, цианоз кожи. Впоследствии, при формировании новых коллатералей, отток венозной крови частично восстанавливается и появляется расширенная венозная сеть на лобке и в паховой области.
Острый тромбоз вен таза. На долю острого тромбоза вен таза приходится 10—15 % общего числа тромбозов в системе нижней полой вены. В настоящее время широко используется собирательный термин "под-
вздошно-бедренный илиофемораль-ный венозный тромбоз", который включает в себя все тромботические окклюзии бедренной, наружной и общей подвздошных вен. Практически всегда заболевание возникает на каком-либо неблагоприятном фоне: состояние после хирургических вмешательств, при сердечной недостаточности, после травм при наличии акушерско-гинекологической патологии. Острый илиофемораль-ный тромбоз у женщин встречается в 3 раза чаще, чем у мужчин. Преимущественно левосторонняя локализация поражения обусловлена тем, что v.iliaca communis sin. перекрещивается одноименной артерией и испытывает постоянную компрессию с ее стороны. Это особенно выражено во время беременности и родов. Кроме того, v.iliaca communis sin. впадает в нижнюю полую вену под углом 130— 140°, что создает предпосылки к затруднению венозного оттока и тромбозу.
В продромальном периоде имеется относительная компенсация венозного кровообращения, обусловленная ограниченным тромбозом v.fern-poralis communis или же пристеночным тромбозом vv.iliacae ext. et communis. Важно, что в этой стадии заболевания создаются наиболее благоприятные условия для возникновения ТЭЛА, так как в просвете сосуда сохранен кровоток и отсутствует прочная связь тромба со стенкой вены. Наиболее типичные симптомы продромальной стадии — это повышение температуры и болевой синдром (боль тупого, ноющего характера в пояснично-крестцовой области, нижних отделах живота и нижних конечностей).
Развернутая клиническая картина заболевания характеризуется типичной триадой симптомов: болью, отеком и изменением окраски кожных покровов от молочно-белой до синюшной. Боль усиливается постепенно и локализуется в паховой области, по переднемедиальной поверхности
бедра и в икроножных мышцах. Характерно вынужденное положение пораженной конечности: она приподнята, отведена и согнута в коленном и тазобедренном суставах. О степени выраженности отека судят по разнице окружности на уровне бедра и голени. Для легкой степени заболевания эта разница составляет до 5 см, для средней — от 6 до 9 см и для тяжелой — 10 см и более. Происхождение отеков при илиофеморальном тромбозе объясняется венозным стазом и нарушением лимфотока. После стабилизации отека появляется достаточно постоянный признак острого илиофеморального тромбоза — усиление рисунка подкожных вен бедра и особенно паховой области. Эти расширенные поверхностные вены компенсируют венозный отток только в горизонтальном положении больного. При вставании пациента появляются распирающая боль и цианоз кожных покровов пораженной конечности.
Большинство зарубежных авторов разделяют острые илиофеморальные тромбозы на phlegmasia alba dolens и phlegmasia cerulea dolens. Первая форма характеризуется отеком конечности, молочной окраской кожных покровов и умеренной болью по ходу сосудов. Процесс в большинстве случаев протекает доброкачественно, смертельные исходы редки. Phlegmasia cerulea dolens (синяя флегмазия, венозная гангрена), которую также называют массивным тромбозом, или болезнью Грегуара, являясь довольно редким заболеванием, отличается тяжелым течением и неблагоприятным прогнозом. Для этой формы характерно 4 основных признака: внезапная боль в конечности, цианоз кожных покровов, массивный отек конечности, отсутствие артериальной пульсации.
Эмбологенные тромбозы. Клини-ко-анатомическими исследованиями установлено, что развитие ТЭЛА наиболее вероятно при проксимальном флеботромбозе (илиофеморальный и
илиокавальный сегменты системы нижней полой вены). Такие потенциально опасные в отношении эмболии тромбозы получили название "эмбо-логенных". Характерной морфологической чертой таких тромбозов является расположение большей части флотирующего тромба в интенсивном потоке крови, что препятствует его прочной фиксации к стенке вены. В результате образуется массивный, флотирующий в токе крови цилиндрический тромб, занимающий значительную часть просвета вены, но имеющий минимальную площадь фиксации в дистальном своем отделе. Такое строение тромба объясняется его происхождением — распространением тромбоза из вен дисталь-ных отделов (заднебольшеберцовых) в вены крупного диаметра (подколенная, илиофеморальный сегмент).
Диагностика. Для ранней и точной диагностики тромбоза глубоких вен данные клинического осмотра необходимо дополнять результатами инструментальных методов исследования. Основными из них в настоящее время являются импедансная плетизмография, радиоиндикационный метод, УЗ-исследования (в В-режи-ме, дуплексное сканирование), контрастная флебография, термография, фибриногеновый тест, ЯМР-томо-графия.
Неинвазивные методы диагностики используются значительно чаще, чем более дорогостоящая и инвазив-ная флебография. Применение им-пендансной окклюзионной плетизмографии при венозных тромбозах основано на том, что изменение объема депонированной венозной крови в нижней конечности приводит к изменению электрического сопротивления, что регистрируется графически.
Специфичность метода при диагностике тромбоза у больных с симптомами предполагаемого тромбоза глубоких вен илиофеморального сегмента составляет 95 %, чувствительность — 90—95 %. У асимптомных
больных с высоким риском возникновения тромбоза чувствительность импедансной плетизмографии низка (12—70 %, по данным различных авторов). Чувствительность метода при диагностике ТГВ голени также низка (около 20 %). Ошибки в виде ложно-положительных или ложноотрица-тельных результатов наблюдаются при наличии у больного хорошо развитых коллатералей, сердечной недостаточности с замедлением скорости венозного возврата и повышением ЦВД, при сдавлении вен паравазаль-ными образованиями.
Радиоиндикационный метод основан на выявлении радиоиндикатором введенного в вену фибриногена, меченного 1311, избирательно концентрирующегося в тромбах. Этот метод точен, безвреден и очень важен для диагностики начальных стадий заболевания. Чувствительность и специфичность метода в диагностике дистального тромбоза составляют 58 и 94 % соответственно, при проксимальных поражениях эти показатели значительно ниже. Тем не менее именно фибриногеновый тест способен установить следующее:
• частота асимптоматических тромбозов в послеоперационном периоде значительно выше, чем принято считать, исходя из клинических данных;
• большинство тромбов первично образуется в глубоких венах голени;
• 50 % эмболии происходит от тромбов, которые распространяются в подколенную вену и илиофеморальный сегмент.
Данный метод непригоден для диагностики двустороннего флеботром-боза и установления границы тромба, что необходимо для выбора плана операции. Возможности теста ограничены при операциях на бедре (когда кровь попадает во внесосудистое пространство), при наличии гематомы, воспаления, разрывов мышц, артритов, так как результаты часто могут быть ложноположительными.
УЗ-исследование. С 1967 г. в диагностике острого венозного тромбоза
используют ультразвуковые методы. Простейшим и наиболее распространенным из них является ультразвуковая допплерография (УЗДГ). При анализе отраженного УЗ-сигнала можно определить характер венозного кровотока, который при тромботичес-ких процессах резко изменяется. Наибольшей информативностью при тромбозах обладает дуплексное сканирование, сочетающее прямую визуализацию сосуда и анализ доппле-ровского сигнала. Это неинвазивное исследование может выполняться в динамике и дает возможность выявить характер и протяженность тромбоза, определить структуру тромба и характер кровотока.
В настоящее время именно дуплексное сканирование по праву считается золотым стандартом в диагностике тромботических поражений венозного русла и отвечает следующим основным требованиям идеального теста:
• точность (высокая чувствительность, специфичность);
• безопасность и неинвазивность исследования;
• быстрое выполнение и относительно несложная интерпретация результатов;
• возможность широкого применения методики и повторения исследования, относительная доступность, отсутствие громоздкой аппаратуры.
В исследовании больных с ТГВ бед-ренно-подколенного ДС является достаточной для постановки правильного диагноза и принятия тактических действий. У пациентов с наличием симптомов точность ДС в выявлении илиофеморальных тромбозов сравнима с возможностями флебографии (чувствительность и специфичность достигают 90—95 %). При вовлечении в процесс супраингвинальных вен точность диагностики снижается до 70 %.
Следует отметить, что даже при отрицательных первоначальных результатах методов неинвазивной диагнос-
тики необходимо проводить повторные исследования.
Использование термографии основано на том, что при ТГВ температура кожи конечностей становится выше, чем в норме. Это отражается цветовым кодом с использованием камеры инфракрасного излучения.
Среди лабораторных тестов необходимо отметить значение определения в крови уровня продуктов деградации фибриногена (например, уровень D-димера — фрагмент продукта деградации перекрестно-связанной молекулы фибрина), содержание которых повышается при тромбоэм-болических осложнениях. Комбинированное использование подобных быстрых и качественных тестов в сочетании с другими неинвазивны-ми методами (преимущественно с ДС) является основой диагностики и принятия решений в лечебной тактике у больных ТГВ. Изменение показателей коагулограммы подтверждает повышение активности свертывающей системы (повышение уровня фибриногена, снижение фибрино-литической активности крови и т.д.).
Флебографическое исследование. На протяжении длительного периода времени рентгеноконтрастная флебография считалась наиболее информативным методом исследования при ТГВ, и лишь с появлением и развитием техники ультразвуковых методов показания к выполнению инвазивной флебографии возникают значительно реже. Лишь в некоторых случаях, например при оценке состояния "немых" для ультразвука зон (приводящий, или гунтеров, канал, икроножные мышцы), рентгенокон-трастные исследования остаются наиболее информативными. В зависимости от задач исследования и места введения контрастных веществ флебографию разделяют на дистальную и проксимальную. При дистальной флебографии контрастное вещество вводят чрескожной пункцией средней или медиальной краевой вены стопы с наложением жгута на ниж-
нюю треть голени и наклоном рентгеновского стола под углом 45°. Другим видом дистальной флебографии является внутрикостная, которую используют лишь в случаях резкого отека голени и стопы, при наличии обширных трофических изменений кожи и подкожной клетчатки в нижней трети голени.
Проксимальную флебографию применяют для уточнения данных дистальной флебограммы, когда имеются признаки внутритазового тромбоза и необходимо установить его проксимальный уровень. С этой целью выполняют чрескожную пункцию бедренной вены по Сельдингеру или острым путем выделяют устье большой подкожной вены бедра и через нее проводят катетер в поверхностную бедренную вену.
На окклюзию магистральных вен указывают следующие рентгенологические признаки:
• отсутствие контрастирования магистральных вен на месте их обычного расположения;
• дефект наполнения в просвете вены при пристеночном расположении тромба;
• "ампутация" магистральной вены — обрыв тени контрастного вещества, расширение вены дисталь-нее окклюзии и контрастирование мелких коллатеральных сосудов.
Несмотря на достаточную информативность, флебография является инвазивным исследованием, требующим использования контрастных йодсодержащих препаратов и ионизирующего излучения. Среди возможных осложнений контрастной флебографии — ятрогенный ТГВ (до 4 %) и аллергические реакции (3 %). Применение данного метода ограничено для систематического ежедневного обследования больных.
ЯМР-томография. Наряду с дуплексным сканированием и флебографией в последние годы широко используют с хорошими диагностическими результатами новые технологии, например ядерно-магнитно-резонанс-
ную (ЯМР) томографию. Эта методика не требует применения йодсодержащих контрастных агентов или ионизирующего излучения. Дополнительная информация об окружающих тканях, полученная при ЯМР-исследовании, помогает объяснить причину возникновения вторичных тромбозов.
Дифференциальный диагноз. Ряд сосудистых заболеваний имеет клиническую картину, сходную с острым тромбозом магистральных вен. Для тромбангиита Бюргера в его начальной стадии и флеботромбоза общими признаками являются боль в икроножных мышцах, быстрая утомляемость конечности, ослабление пульсации на периферических артериях. Однако при тромбангиите отмечаются постепенное развитие заболевания, перемежающаяся хромота, похолодание и онемение конечности, в то время как острый флебо-тромбоз начинается с острой боли по ходу пораженной конечности. Пульсация бедренной артерии при наличии отека ослаблена или отсутствует, поэтому дифференциальный диагноз необходимо проводить и с острой эмболией подвздошно-бедренного артериального сегмента. Для эмболии характерны внезапное появление сильной боли в дистальных отделах конечностей, чувство похолодания и онемения, бледная окраска конечности с пятнистым цианозом, нарушение движений в пальцах стопы и голеностопном суставе, гипестезия.
Боль при невритах седалищного нерва носит постоянный характер. В острой стадии воспаления нервный ствол, как и иннервируемые им мышцы, при пальпации болезне-ны, резко положительны симптомы натяжения. Отмечаются расстройства чувствительности — от кратковременной гиперестезии до гипестезии. Для невритов характерны выраженные нарушения в виде сосудодвига-тельных, секреторных и трофических нарушений.
Острый лимфостаз нижних конеч-
ностеи возникает после рожистого воспаления, лимфангиита, пахового лимфаденита. При лимфостазе не выражен болевой синдром, не характерны цианоз кожных покровов и усиление венозного рисунка конечности. Отеки нижних конечностей при сердечной недостаточности развиваются медленно и имеют двусторонний характер без болевого синдрома.
Дифференциальный диагноз проводят также с миалгиями, миозитом, артритом, травматическим повреждением мышц, компрессией магистральных вен различными образованиями.
Заболевания, требующие дифференциальной диагностики с тромбозом глубоких вен:
• растяжение и тупая травма мышц;
• разрыв мышц с субфасциальной гематомой;
• спонтанная гематома мягких тканей;
• разрыв синовиальной кисты (киста Бейкера);
• артрит, синовит, миозит;
• целлюлит, лимфангиит, рожистое воспаление;
• тромбофлебит поверхностных вен;
• артериальная недостаточность;
• беременность или использование оральных контрацептивов;
• лимфедема;
• липедема;
• хроническая венозная недостаточность;
• наружная компрессия венозных магистралей: лимфаденопатия, опухоль, гематома, абсцесс, сдавление подвздошной артерией;
• системные отеки: врожденные пороки сердца, хроническая почечная недостаточность, метаболические нарушения, отеки после артериальных реконструкций;
• артериовенозная фистула.
Консервативная терапия. Основ
ные задачи лечения при ТГВ:
▲ восстановление адекватного венозного оттока;
▲снижение риска эмболии легочной артерии;
▲предупреждение дальнейшего роста тромба;
▲предупреждение повреждения венозных клапанов и возникновения посттромбофлебитического синдрома;
▲ предотвращение повторного венозного тромбоза.
Лечебная тактика при тромбозе глубоких вен нижних конечностей определяется на основании данных клинических и инструментальных методов исследования, позволяющих установить характер и протяженность тромботического процесса, прогноз для жизни больного и сохранения конечности в случае консервативного лечения.
Консервативный метод является основным при лечении больных острым венозным тромбозом, однако положительный результат отмечается лишь у 36—39,7 % из них. После консервативной терапии процент развития посттромбофлебитического синдрома остается достаточно высоким (до 70-75 %).
Основным средством, применяемым для профилактики и лечения данной патологии, является нефрак -ционированный гепарин. Его использование даже в фиксированной дозе (15 000 ЕД/сут в течение 7—10 дней) у больных, перенесших операции на органах брюшной полости по поводу острой хирургической патологии, снижает частоту тромбоза глубоких вен нижних конечностей в 4,1 раза, а послеоперационную летальность от эмболии легочной артерии — в 7 раз. У лиц с более высоким риском тромботических осложнений более эффективно применение гепарина в индивидуально подобранной дозе (20 000-45 000 ЕД) под контролем показателей коагулограммы. Оптимальный способ введения в такой ситуации — медленная внутривенная инфузия при помощи инфузомата. С 4-го дня дозу препарата постепенно
уменьшают до 15 000 ЕД/сут и продолжают профилактику подкожными инъекциями в режиме мини-доз.
Применение гепаринов низкой молекулярной массы (НМГ) позволяет уменьшить число побочных эффектов, вызываемых гепарином, в частности выраженной кровоточивости. НМГ оказывают значительно меньшее влияние на функцию тромбоцитов, отличаются более продолжительным действием, большей предсказуемостью поведения, отсутствием необходимости частого лабораторного контроля. НМГ в отличие от нефрак-ционированного гепарина обладают большей активностью по отношению к фактору свертывания Ха, следовательно, оказывают более выраженный противотромботический и менее выраженный антикоагулянт-ный эффект (определяется по воздействию на антитромбин- III, клинически проявляется кровоточивостью).
Среди наиболее распространенных на сегодняшний день 7 препаратов наибольшей Ха-активностью обладают клексан (эноксапарин), фрагмин, фраксипарин. При лечении острых венозных тромбозов клексан назначают в дозе 1 мг/кг 2 раза в сутки подкожно. Дозировка фраксипарина — 7500 ЕД, фрагмина - 5000-7500 ME 2 раза в день.
Фибринолитические препараты и активаторы фибринолиза при применении в первые дни заболевания способны вызвать растворение свежих тромбов, но малоэффективны в более поздних стадиях. Фибринолити-ки вводят капельно внутривенно, лучше целенаправленно в вены пораженной конечности в течение 3—6 дней. Внедрение в клиническую практику катетерного направленного тромбо-лизиса улучшило результаты и безопасность тромболитической терапии.
При лечении илиофеморального тромбоза урокиназой после пункции бедренной вены контралатеральной конечности или правой яремной вены и установки катетера болюсно вводят 250 000-500 000 ЕД с после-
дующей инфузией в дозировке 250 000 ЕД/ч. Возможно сочетанное применение урокиназы с тканевыми активаторами плазминогена (t-PA) в дозе 10 мг. Повторные флебогра-фические исследования выполняют с интервалами 8—12 ч, окончание терапии определяют по достижении максимального лизиса. После завершения тромболизиса необходимо продолжение антикоагулянтной терапии (гепарин, НМГ) с переводом в дальнейшем на длительный прием (иногда до 6—8 мес) таблетирован-ных антикоагулянтов.
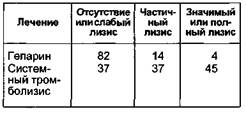
Сравнительные результаты тромболитической терапии (флебографи-ческий контроль) на основании данных 13 крупных исследований приведены в табл. 13.3.
Применение низкомолекулярных декстранов (реополиглюкин, реомак-родекс и др.) направлено на снижение вязкости крови и агрегации тромбоцитов, улучшение микроциркуляции и коллатерального кровообращения. Кроме того, эти препараты оказывают слабое антикоагулянтное действие, усиливают диурез, способствуют удалению жидкости из тканей и уменьшению отеков. Дополнительно назначают противовоспалительные и спазмолитические средства (бутади-он, реопирин, аспирин), венотоники.
Хирургическое лечение. Цель оперативного вмешательства при остром тромбозе магистральных вен нижних конечностей и таза — профилактика ТЭЛА и восстановление кровотока в венозных магистралях.
Таблица 13.3. Лизис тромбов при использовании гепарина и тромболитиков (в процентах)
Хирургическое лечение при остром тромбозе считается абсолютно показанным при флотирующем тромбе в просвете вены и распространенном характере тромботического процесса (вовлечение нижней полой вены, угроза развития венозной гангрены и предшествующие ТЭЛА).
Тромбэктомия и восстановление венозного кровотока необходимы при сегментарных поражениях и локализации тромба в местах слияния крупных магистральных вен. Данное вмешательство возможно и эффективно в сроки заболевания до 5 сут. В более поздние сроки даже при наличии технической возможности тромбэктомия при окклюзивных тромбозах клапансодержащих сосудов нецелесообразна, так как в отдаленном периоде вследствие необратимых изменений клапанов развивается хроническая венозная недостаточность.
Изучение проходимости оперированных вен показало, что в 85—89 % наблюдений, несмотря на технически правильно выполненную тромб-эктомию и адекватно восстановленный кровоток, повторно развивается окклюзивный тромбоз. Это связано с изменениями во внутренней оболочке сосуда, проявляющимися частичной или полной десквамацией эндотелия, обнажением субэндотелиаль-ного и мышечного слоев стенки вены, обладающих повышенной тромбо-генностью.
Развитию тромботической окклюзии способствуют низкая скорость кровотока в вене, уменьшение поперечного сечения сосуда, вызванное тромбозом ваза-вазорум, травма сосудистой стенки.
Для тромбэктомии в илиокаваль-ном венозном сегменте используют три основных доступа (бедренный, лапаротомный и забрюшинный) или их комбинацию. Выбор доступа определяется локализацией тромбоза. При тромбозе общей бедренной и наружной подвздошной вен используют изолированный бедренный доступ. При левосторонней локализации

Рис. 13.1. Этап выполнения тромбэктомии катетером Фогарти из подвздошно-бедренного сегмента.
илиофеморального тромбоза с обструкцией общей подвздошной вены наиболее предпочтителен забрюшинный доступ, обеспечивающий прямой доступ к сосудам таза. Это дает возможность провести тромбэк-томию открытым способом с контролем радикальности восстановления проходимости магистрали визуально, а главное — позволяет установить причину обструкции (спайки, мембраны) и устранить ее (рис. 13.1).
Дистальный тромб выдавливают тугим бинтованием конечности эластичным бинтом или ручным массажем. Усиленные сгибания и разгибания конечности облегчают удаление тромба. Если указанные мероприятия неэффективны, то через клапаны проводят баллонный катетер и выполняют тромбэктомию. Удаление

Рис. 13.2. Компрессия по Эсмарху для удаления тромбов из дистальных отделов венозного русла.
тромбов возможно и через обнажение заднебольшеберцовых вен в нижней трети голени (рис. 13.2).
Тромбэктомию из нижней полой вены осуществляют через венотомию в бедренной вене. До введения баллонного катетера устанавливают режим искусственной вентиляции с положительным давлением в конце выдоха (PEEP) 10 см вод.ст. Эта процедура снижает риск развития эмболии легочной артерии и делает ненужным размещение баллона для проксимальной окклюзии. В случаях флотирующего, нестабильного тромба в НПВ или при неполной тромб-эктомии в результате первой попытки необходим баллон для проксимальной окклюзии с целью предотвращения эмболических осложнений.
Основные условия для успешного выполнения тромбэктомии:
• полная визуализация тромботи-ческих масс (обязательно контрастирование при флебографии контрала-терального илиофеморального сегмента и нижней полой вены;
• предпочтительно использование во время операции интубационного наркоза с положительным давлением в конце фазы выдоха;
• использование достаточных доз гепарина;
• использование интраоперацион-ной инфузии активаторов плазмино-гена после выполнения тромбэктомии при наличии установленного баллона в подвздошном сегменте (с целью его окклюзии);
• использование экструзионной техники (баллон Фогарти) для удаления дистальных тромбов;
• для подтверждения адекватности тромбэктомии обязательно выполнение флебографии;
• при удачно выполненной тромбэктомии рекомендуется наложение артериовенозной фистулы между подкожной веной или одним из крупных проксимальных притоков с поверхностной бедренной артерией;
• в случае неполного устранения окклюзии подвздошного сегмента, при наличии наружной компрессии вены выполняют перекрестное обходное венозное шунтирование с использованием 8- или 10-миллиметрового ПТФЭ-протеза с обязательным формированием временной артериовенозной фистулы;
• использование наружной пнев-мокомпрессии в послеоперационном периоде;
• продолжение гепаринотерапии (нефракционированный гепарин или низкомолекулярные его фракции) в послеоперационном периоде с переходом в дальнейшем на прием перо-ральных антикоагулянтов.
Для увеличения скорости кровотока в дезобтурированной вене используют временную артериовенозную фистулу. Ускорение венозного кровотока и уменьшение стаза крови в вене после тромбэктомии снижают риск немедленного ретромбоза и создают условия для восстановления венозного эндотелия, что происходит в сроки от 4 нед до 4 мес. По мнению B.Ekloff (1992), одного из веду-
щих специалистов в области лечения острых венозных тромбозов, тромб -эктомия с наложением временной артериовенозной фистулы является методом выбора при лечении острого илиофеморального тромбоза.
Кровоток через временные фистулы постепенно возрастает, поэтому некоторые авторы считают необходимым активное закрытие артериовенозной фистулы в сроки от 4 нед до 6 мес. С другой точки зрения, ликвидация такой фистулы не обязательна, так как до 30 % артериове-нозных фистул самостоятельно закрывается в течение первого месяца. В целом эта методика безопасна и служит необходимым дополнением к венозной тромбэктомии, уменьшая частоту повторных тромбозов и осложнений, вызванных ТГВ.
Тромбэктомия из глубоких вен системы нижней полой вены с помощью катетера Фогарти дает 58—90 % хороших и удовлетворительных результатов. Основной причиной неудач (у 30—32 % больных) являются поздние сроки оперативного вмешательства. Успех операции обратно пропорционален времени, прошедшему от начала тромбоза. Наилучших результатов достигают при тромбэктомии, выполненной в 1—4-е сутки от начала болезни.
Тромболизис также дает хорошие результаты, но за более длительный срок, и сопровождается большим числом осложнений.
Частичную (паллиативную) тромб-эктомию выполняют при угрозе отрыва флотирующей части тромба и возникновения ТЭЛА. Операция заключается в резекции части тромба, не связанного со стенкой вены. С целью профилактики ТЭЛА иногда используют пликацию нижней полой вены или устанавливают кава-фильтр.
Противопоказания к операции тромбэктомии. Абсолютным противопоказанием к оперативному вмешательству служит терминальное состояние больного. Относительными противопоказаниями являются огра-
ниченный тромбоз вен голени, фле-ботромбозы в прошлом, наличие противопоказаний к лечению антикоагулянтами, престарелый возраст.
У больных с активным целлюлитом или принимающих иммуносупрессо-ры проблема заживления ран может препятствовать выполнению тромбэктомии. Наложение артериовенозной фистулы относительно противопоказано больным с хронической сердечной недостаточностью, поскольку усиление венозного возврата крови может усилить застойные явления. Изолированные ТГВ ниже коленного сустава сопровождаются меньшими осложнениями, но проведение тромбэктомии в этих случаях затруднительно, поэтому при данной локализации тромбэктомия, как правило, не показана. У больных с ХВН или венозными тромбозами, возникшими вследствие сдавления магистральных вен извне (новообразования, рубцовые процессы), удаление свежего тромба лишь в небольшой степени предупреждает повторный тромбоз и другие осложнения ТГВ. Не показана тромбэктомия больным с массивной легочной эмболией, так как это не разрешает всех проблем. Гиперкоагуляционные состояния сопровождаются высокой частотой повторных тромбозов и первично лечатся консервативно антикоагулянтами в течение длительного времени (схема 13.2).
Сравнительная оценка результатов оперативного и консервативного лечения. Хорошие непосредственные и отдаленные результаты хирургического лечения венозных тромбозов наблюдаются у 67—85 % больных, а плохие (посттромбофлебитический синдром легкой или средней степени тяжести) — только у 13—33 % оперированных. Эти результаты значительно лучше, чем при консервативном лечении. Скандинавское рандомизированное исследование [Plate G. et al, 1990] с учетом отдаленных результатов (6 мес) тромбэктомии при острых венозных тромбозах в срав-
49 - 4886

|
нении с консервативным лечением антикоагулянтами подтверждает эти данные (табл. 13.4).
Профилактика. Большинство исследователей признают, что веноз-
Таблица 13.4. Отдаленные результаты консервативного и оперативного методов лечения острого венозного тромбоза

ные тромбозы и эмболии способны значительно осложнять выздоровление хирургических пациентов в стационаре и являются потенциально опасным фактором, однако существует много противоречивых мнений, касающихся эффективности и выбора средств профилактики.
Опасность развития подобных осложнений существует в течение даже спустя 5 нед после хирургического вмешательства. По данным G.L.Jon-son и соавт., у больных, перенесших травматологические вмешательства (общая частота встречаемости осложнения 1,04 %), 9,7 % эпизодов ТЭЛА возникло в течение первой недели, 54,2 % — второй, 22,9 % — третьей, 8,4 % — четвертой, 4,8 % — в течение пятой недели послеоперационного периода. С учетом этого актуальность проведения антикоагу-лянтной терапии сохраняется и после выписки больного из стационара. В зарубежной литературе наиболее употребима модифицированная классификация групп риска Salzman и Hirsh, определяющая частоту разви-

|
| Таблица 13.5. Частота развития тромботических осложнений (в процентах) у стационарных больных в зависимости от группы риска |
тия тех или иных тромботических осложнений (табл. 13.5).
Применение гепарина в клинике доказало его высокую эффективность в профилактике и лечении тромбо-эмболических осложнений. Появление в конце 80-х годов низкомолекулярных гепаринов (НМГ) и их внедрение в клиническую практику были обусловлены желанием свести к минимуму недостатки стандартной ге-паринотерапии, улучшить результаты профилактики тромбозов и лечения больных с тромбоэмболическими осложнениями.
M.Samama и соавт. (1998) в своем исследовании сравнивали различные дозы эноксапарина (20 и 60 мг), вводимого однократно, со стандартным гепарином в дозе 5000 ЕД 3 раза в сутки. Клиническая эффективность НМГ отмечена при введении всех исследуемых доз, поэтому общехирургическим больным рекомендовано применять наименьшую из них — 20 мг. Частота тромбоза среди пациентов, получавших 20 мг эноксапарина, составила 3,8 %, среди получавших стандартный гепарин — 7,2 %.
Рекомендуемый способ применения НМГ в общей хирургии с умеренным риском развития ТЭО: 20 мг клексана (2500 ЕД фрагмина или 2850 ЕД фраксипарина) подкожно один раз в день; первую дозу вводят за 2 ч до операции; профилактическое лечение следует продолжать до
тех пор, пока существует риск тромбоэмболии. У больных с более высокой степенью риска рекомендуемая доза составляет 40 мг клексана (5000 ЕД фрагмина или 5700 ЕД фраксапа-рина) подкожно один раз в день.
По данным многочисленных исследований, частота венозных тромбозов в группе НМГ существенно ниже, чем у больных, получавших стандартный гепарин: у травматологических больных с большим риском ТЭО — 3—5 % среди получавших НМГ (клексан 30 мг 2 раза в день); в группе больных, получавших стандартный гепарин в дозе 5000 ЕД каждые 8 ч,- 10-12 %.
Среди немедикаментозных средств профилактики важное значение имеет применение компрессионных средств (эластичные бинты, градуированные компрессионные чулки), а также использование прерывистой пневматической компрессии.
Необходимость продолжения профилактики НМГ существует как минимум в течение месяца после обширных травматологических вмешательств (при этом частота послеоперационного тромбоза снижается вдвое).
Литература
Балуда В.П., Балуда М.В., Голъдберг А.П. и др. Претромботическое состояние//Тром-боз и его профилактика.—Москва—Амстердам, 1999.-297 с.
Сапелкин СВ., Покровский А.В. Роль Эноксапарина (Клексана) в профилактике и лечении тромбоэмболических осложнений (обзор литературы)//Ангиол. и сосуд. хир.-1998.-Т. 3-4.
Becker D.M., PhilbrickJ.T., Humphries J. E. D-dimer testing and acute venous thromboembolism. A shortcut to accurate diagnosis?//Arch. Intern. Med.-1996.-Vol. 156.-P. 939-946.
Carpenter J.P., Holland G.A., Baum R.A. et al. Magnetic resonance venography for the detection of deep venous thrombosis: comparison with contrast venography and duplex Doppler ultra-sonography//Vasc. Surg.—1993.—Vol. 18. — P. 7134-7141.
Dunn C.J., Goa K.L. Enoxaparin. A pharmaco-economic appraisal of the use in thromboembolic prophylaxis after total hip arthroplasty//Pharma-coeconomics.—1996.—Vol. 10.—P. 179-190.
49*
Evans A.J., Sostman H.D., Knelson M.H. et al. 1992 ARRS Executive Council Award. Detection of deep venous thrombosis: prospective comparison of MR imaging with contrast venography//A.J.R.-1994.-Vol. 161(1).-P. 131-139.
Kniemeyer H. W., Sandmann W., Schwindt С et al. Thrombectomy with arteriovenous fistula for embolizing deep venous thrombosis: an alternative therapy for prevention of recurrent pulmonary embolism//Clin. Investig.—1993.— Vol. 72.-P. 40-45.
Krievins D.K., Beygui R.E., Katlaps G.J., Fog-arty T.J. Какова роль тромбэктомии при тромбозах полой вены и илеофеморального сегмента?//Ангиол. и сосуд, хир.—1997.— Vol.1.—Р. 83-95.
Meissner М., Caps М., Bergelin R. et al. Propagation, rethrombosis and new thrombus formation after acute deep venous thrombosis//.!. Vase. Surg.-1995.-Vol. 22.-P. 558-567.
Planes A. et al. Risk of deep-venous thrombosis after hospital discharge in patients having undergone total hip replacement: double-blind randomized comparison of enoxaparin versus pla-cebo//Lancet.-1996.—Vol. 348.-P. 224-228.
Plate G., Akesson Н., Einarsson E. et al. Long-term results of venous thrombectomy combined with a temporary arterio-venous fistula//Europ. J. Vase. Surg.-1990.-Vol. 4.-P. 483-489.
Prandoni P., Villata S., Bagatella P., Rossi L. et al. The clinical course of the deep vein thrombosis. Prospective long-term follow-up of 528 symptomatic patients//Haematol.—1998.— Vol. 82.-P. 423-428.
Risk of an prophylaxis for venous thromboembolism in hospital patients. Thromboembolic Risk Factor (THRIFT) Consensus Group// Brit. Med. J.-1992.-Vol. 305.-P. 567-574.
Samama M. et al. Low molecular weight heparin compared with unfractionated heparin in prevention of postoperative throm-bosis//Brit. J. Surg.-1998.-Vol. 75.-P. 128-132.
Semba СР., Dake M.D. Iliofemoral deep venous thrombosis: aggressive therapy with catheter-directed thrombolysis//Radiology.— 1994.-Vol. 191.—P. 487-494.
Solis MM., Ranval T.J., Thompson B. W. et al. Results of venous thrombectomy in the treatment of deep vein thrombosis//Surg. Gynec. Obstet.-1993.-Vol. 177.-P. 633-639.
Дата добавления: 2015-10-21; просмотров: 146 | Нарушение авторских прав
| <== предыдущая страница | | | следующая страница ==> |
| Классификация заболеваний венозной системы | | | Ишемические венозные тромбозы |