
|
Читайте также: |
Þ угловая структура (Ð920)
ЭО(Н) = 2,1 и ЭО(S) = 2,5 Þ связь полярная.
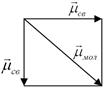
m м = S m св¹ 0 Þ молекула в целом полярная.
Молекула SbН3
 Sb…5 s 25 p 3
Sb…5 s 25 p 3
|


Гибридизация:
|
Если у атома в образовании химических связей участвуют разные по типу АО (s-, p-, d- или f-АО), то химические связи формируются электронами не «чистых», а «смешанных», или гибридных орбиталей.
Перекрывание гибридных АО происходит в большей степени, чем негибридных орбиталей Þ
► химические связи прочнее
► молекула более устойчива.
Гибридная орбиталь:
 |
Дата добавления: 2015-10-21; просмотров: 134 | Нарушение авторских прав
| <== предыдущая страница | | | следующая страница ==> |
| H2S (92o), Н2Se (91o) и Н2Те (89о) изменяется? | | | Типы гибридизации АО и структура молекул |