
Читайте также:
|
A. Простые липиды: сложные эфиры жирных кислот с различными спиртами. 1. Глицериды представляют собой
сложные эфиры трехатомного спирта глицерина и высших жирных кислот. 2. Воска: сложные эфиры высших жирных кислот и одноатомных или двухатомных спиртов.
Б. Сложные липиды: сложнее эфиры жирных кислот со спир-тами, дополнительно содержащие и другие группы. 1. Фосфолипиды: липиды, содержащие, помимо жирных ки-слот и спирта, оста-ток фосфорной ки-слоты. В их состав часто входят азоти-стые основания и другие компоненты: а)глицерофосфолипиды (в роли спирта выступает глице-рол); б) сфинголипиды (в роли спирта - сфингозин). 2. Гли-колипиды (гликос-финголипиды). 3. Стероиды (Не гидролизуются с освобождением жир-ных кислот. К стерои-дам относятся гор-моны коркового ве-щества надпочечников, желчные кисло-ты, витамины группы Д). 4. Другие сложные липиды: сульфолипиды, аминолипиды. К этому классу можно отнести и липопротеины.
Предшественники и производные липидов: жирные кислоты, глицерол, стеролы, спирты, жирорастворимые витамины, гормоны.
Жирные кислоты, входящие в состав триглицеридов, практически определяют их физико-химические свойства. Так, температура плавления тригли-церидов повышается с увеличением числа и длины остатков насыщенных жир-ных кислот. Фосфолипиды В зависимости от того, какой многоатомный спирт участвует в образо-вании фосфолипида (глицерин или сфингозин), последние делят на 2 группы: глицерофосфолипи-ды и сфингофосфо-липиды. Глицерофосфолипиды являются производными фосфатидной кисло-ты. В их состав вхо-дят глицерин, жир-ные кислоты, фосфорная кислота и обычно азотсодер-жащие соединения. Для всех глицеро-фосфолипидов характерно, что одна часть молекул обна-руживает резко вы-раженную гидрофоб-ность, тогда как дру-гая часть гидро-фильна благодаря отрицательному за-ряду фосфорной ки-слоты и положительному заряду ра-дикала.
19.Липидный бислой. Липосомы. Мембрана представляет двойной липидный бислой икрустированный интегральными белками, опирающийся на каркас из периферических белков. Толщина липидного бислоя 6-10нм. Сна-ружи л.б. окружен слоем гликокаликса, образованного углеводными фрагментами гликолипидов и гликобелков. Основу л.б. составляют молекулы фосфолипидов, представляющие ацелглицерол, у котор. одна гидро-ксильная группировка этерифицирована остатком фосфорной к-ты. В свою очередь остаток фосфорной к-ты этерифицирован каким-либо спиртом (этанолом, холин, серин). Осн. св-во фосфолипидов это их амфифильность. В моле-куле фосфолипида часть молекул обладает гидрофобными св-ми (неполярный хвост), часть обл. гидрофильными св-ми (полярная голова). Помимо фосфолипидов в липидный бислой входят молекулы холестерина, имеющие размеры близкие к размерам фосфолипидов. Холестерин заполняет пустоты в мембране придовая ей необход. жесткость. Самый важный структур-ный переход в мембране - это переход между твердым кристаллическим состоянием и жидко-кристалическим. Этот переход назы-вается фазовым переходом в мембране. Зависит от состава мембраны и лежит в физиологическом диапазоне температур.
Липосомы, или фосфолипидные везикулы (пузырьки), получают обычно при набухании сухих фосфолипидов в воде или при впрыскивании раствора липидов в воду. При этом происходит само-сборка бимолекулярной липидной мембраны. Минимуму энергии Гиббса отвечает замкнутая сферическая одноламеллярная форма мембраны. При этом все неполярные гидрофобные хвосты находятся внутри мембраны и ни один из них не соприкасается с по-лярными молекула-ми воды. Однако чаще получаются несферические мно-голамеллярные ли-посомы, состоящие из нескольких бимолекулярных слоев, — многослойные липосомы.
20. Природные мембраны. Биол. мемб. (БМ) обесп: транспорт веществ в организме, проведение нервных импульсов, восприятие внешних сигналов. Общая площадь БМ – несколько сот тысяч га. Впервые мембрану выделил Левенгук. Мембрана – тонкая (толщиной 7-10 нм) плоская структура, образованная липидным бислоем, инкрустированная молекулами белка, которые отделяют клетку от окружающей среды и клеточные органеллы друг от друга. Основные функции клеточных М.: 1. Барьерная – выполняет роль перегородки или барьера, обеспечиая специфический перенос вещества внутрь клетки и наружу; 2. Защитная; 3. Матриксная – роль основы или матрицы для протекания большинства биохимических процессов; 4. Регуляторная (сигнальная) – может обеспечивать перенос сигнала (трансдукции) внутрь клетки. Классификация: 1. Биологические, те что в кл-ке; 2. Искусственые. БМ: плазматические (окружают всю клетку) - поверностные, митохон., ядерн., микросомальные (окружают эндоплазматический ретикулум), специализированные мебраны. В состав мембран входят 2 типа липидов (фосфолипиды, холестеролы). В М. животн. кл. более 50% всех липидов сост-т фосфолипиды — глицерофосфолипиды и сфингофосфолипиды. Молекулы фосфолипида обладают гидрофобным хвостом, нерастворимым в воде, и гидрофил-ой головкой, растворимой в воде (рисунок). Гликолипиды несут разнообр. ф-ции: отвеч. за рецепцию нек. биологически активных веществ, участв-т в дифф-ке ткани, опред-т видовую специфичность. Входят многочисенные белки. Белки могут взаимод-ть с липидн. бислоем за сч. электростатич. и (или) межмолекул. Сил. По степени ассоциации с мембраной белки разделяются на: интегральные и периферические. Белки мембран вып-т три основные функции: каталитическую (ферменты), рецепторную и структурную . Углеводы в биол. М. нах-ся в соединении с белками (гликопротеины) и липидами (гликолипиды). Углеводные цепи белков предст. соб. олиго- или полисахаридные стр-ры, в состав кот. вход. глюкоза, галактоза, фукоза и манноза.
Также входит вода, кот образует мономолекулярный слой, окружающий мембрану. Основная функция мембран – избирательная проницаемость.
21.Надмолекулярн. организация мембран. Жидкостно-мозаичная модель строения биол. м. (Сингер и Никольсон, 1972 год): структурн. основу биол. м. сост-т двойной слой фосфолипидов, инкрустир. белками. Липиды нах-ся при физиол. усл. в жидк. агрегатн. состоянии. Одним из подтвержд. жидк.-моз. модели явл. и тот факт, что в разных м. соотнош. м/ду содерж. белков и фосфолипидов сильно колеблется, в то время как, согласно "бутербродной" модели, соотнош. кол-ва белков и липидов во всех М. д. б. одинак. В М. животн. кл. много холестерина. В частности, обнаружено, что белк. не всегда свободно плавают в липидном море, а м. б. "заякорены" на внутр. (цитоплазматич.) стр-ры кл. К таким стр-рам отн. микрофиламенты и микротрубочки.
Твердокаракасная модель (С.В. Конев): липидн. бислой фиксирован жестк. белк. каркасом, в то вр. как часть мембр. белков может достат. свободно перемещ-ся в плоск-ти липидн. бислоя. Основу липидн. бислоя сост-т молек. Фосфолипидов, представл. ацилглицерол.
СН2 - СН - СН2 R1,R2- «хвост», все остальное – «головка»
| | |
С=О С=О НО-Р=О
| | |
R1 R2 OH сюда прикр-ся эфирн. гр-ка.Осн. св-во фосфолипидов амфифильность. В молек. фосфолипидов ч. молек. облад. гидрофобн. св-ми (неполярн. «хвост»), ч. – гидрофильн. (полярн. «головка»). Холестерин заполн-т пустоты в мембр., придавая ей необх. жесткость. Амфифильн. соед. спос. обр-ть замкнутые или плоские бислойн. (или моносл.) стр-ры, в кот. полярн. «гол.» экспонированы в воду. Обр-ие таких стр-р происх. самопроизв. в рез. действ. термодин. сил. Предполагается, что интегральные белки окружены пограничным слоем липидных молекул (т. наз. аннулярные липиды), подвижность к-рых ограничена или, по крайней мере, нарушена в результате контакта с неровной пов-стью белковой глобулы. Электростатич. (кулоновские; солевые мостики (в белках)) - взаимод. м/ду заряж. хим. группировками. Гидрофобн. - взаимод. м/ду ат. или молек., для кот. термодинамически более выгодно нах-ся в контакте др. с др., нежели в контакте с молекулами воды
22. Периферические и интегральные белки. Белки, наз. периферич. или поверхностными, сравнит. слабо связаны с М. и отдел-ся от нее в мягких условиях, напр. в р-рах, имеющих высокую ионную силу или содержащих комплексоны. Намного прочнее связаны с М. т. наз. интегр., или внутримембр., белки. Чтобы их выделить, требуется, как пр., предварит. разрушить М. с пом. ПАВ или орг. р-рителей. Периферич. белки по своим св-вам мало отл-ся от обычных водорастворим. белков. Характерн. ос-ть интегр. белков - плохая р-римость в воде. Особенность интегр. белков - наличие в их полипептидной цепи довольно протяженных уч-ков с преобладающим содерж. неполярн. АК. Как прав., эти уч-ки им. конформацию a-спирали, на наружной стороне кот. располож. бок. углеводородн. фрагменты аминокислотных остатков, в рез. чего вся спираль, в целом, приобретает гидрофобн. хар-р. Участков с b-структурой, как прав., мало. В белках, кот. пронизывают биол. М. насквозь, такие гидрофобные тяжи соед-ют м/ду соб. полярные области белковой молекулы, находящиеся на противоположных сторонах М. У белков, располож. только на одной стороне биол. М. и погруженных в нее лишь частично, a-спирали служат своеобразным гидрофобным "якорем", прочно удерживающим белок в М. В нек-рых случ. "заякоривание" белков в биол. М. происх. при пом. ковалентно связ. с ними липидов. Мембранные белки наряду с липидами игр. важн. структурн. роль. Ферментативная активность присуща мн. мембраносвя-занным белкам, причем мембраны разл. клеток и отдельных органоидов имеют свой характерный набор ферментов. Как правило, ферментные белки располагаются в биол. М. в опред. порядке, кот. делает возм. последовательное протекание р-ций метаболии, цикла.
М. предст. динамич. стр-ру. Выд. неск. типов подвижн-ти мембр. компонентов: 1) вращат. движ. молекул фосфолипидов. Время вращат. корреляции молек. ф-дов 10-9 с; 2) латеральн. подв-ть (движ. м-лы ф-дов в плоск-ти М. За 1 с м-ла ф-да перемещ-ся на 5 тыс нм); 3) флип-флоп переходы – перескоки ф-дов м/ду монослоями (минуты и часы). Время вращат. корреляции молекулы молек. белков 10-5 с. Функционир. мембр. стр-р осущ-ся в рез. их конформац. подв-ти. Многие биохим. проц. перенесены внутрь М., т.к. в М. низк. диэлектрич. прониц-ть (3). Сам. важн. структ. переход в М. – переход м/ду тв. кристаллич. (квазитвердокристаллич.) состоян. и жидкокрист. Этот переход наз. фазовым переходом в М. Он завис. от состава М. и лежит в физиол. диапазоне температур
23. Проницаемость мембран и транспорт в-в. Перенос включает как перенос метаболитов через м-ну, так и направленную секрецию БАВ. Основной параметр, хар-щий перенос в-ва ч/з мембрану- поток в-ва (J). Поток- кол-во мол-л или молей в-ва, переносимых ч/з единицу площади мембраны в единицу времени.
Механизмы транс-та малых молекул через м-ну:
1. Диффузия 2. Облегченная диффузия; 3. Активный транспорт; 4. эндоцитоз; 5. экзоцитоз
Диффузия – перенос в-ва через м-ну проницаемую для этого в-ва, по градиенту концентрации (разность концентраций в-ва по обе стороны м-ны). Это движение от большей конц-ции к меньшей. Движ силой явл-ся разность электрохим потенциалов в-ва по обе стороны мембраны. Процесс диффузии описывается ур-м Фика: J= –D Δc/Δx, где J– поток в-ва ч/з мембрану, D- коэф-т диффузии, Δс/Δx - градиент концентрации
ГРАФИК ДИФФУЗИИ: чем больше градиент, тем больше поток в-ва.
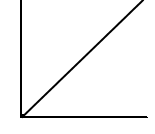
Когда исчезнет поток, градиент превращается в ноль.
Облегченная диффузия – отличается от диффузии:
1. Наличием специфичных белков-переносчиков (аквапорины, анионпереносящий белок полосы3)
2. Избирательностью
3. Насыщение (заполняют все белком-переносчиком)
4. Происходит быстрее, чем диффузия.
ГРАФИК:
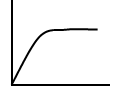
По механизму облегченной диффузии транспортир-ся в клетку АК, глюкоза, др. сахара.
Активный транспорт – перенос в-ва через м-ну против градиента концентрации и осуществляет с расходованием энергии АТФ специфическими насосами.
Насосы: H+-АТФаза (протонная);
Na+,K+-АТФаза; Ca2+-АТФаза; Mg2+-АТФаза.
24.Потенциал покоя. Потенциал действия. ПП – это разность потенциалов м-ду внутренней и наружной поверхностью м-ны у кл-ки, которая находится в состоянии физиологического покоя. При этом наружная сторона заряжена «+», внутренняя – «-». Величина ПП может быть в пределах 30-90мВ. Для обозначения величины отрицательного заряда мембраны применяют символ Е0. В механизме возникновения ПП ведущая роль принадлежит следующим факторам:
1. Наличие разности концентраций (градиентов) ионов K+ и Na+ м-ду внутриклеточной и внеклеточной средой. Градиент по содержанию Na+ в разных кл-ках – от 10 до 15. Еще большая величина градиента K+ – от 30 до 40. Содержание ионов хлора и кальция снаружи клеток больше, чем внутри. Градиент по хлору у разных кл-ток может значительно различаться, составляя от 12 до 30. Градиент по кальцию может достигать 10000.
2. Различная проницаемость клеточных м-н для минеральных ионов.
Из-за большой концентрации K+ в кл-ке и относительно высокой проницаемости для него клеточной м-ны калий выходит и выносит с собой положительный электрический заряд. Отрицательно заряженные ионы не могут пройти через м-ну и остаются в кл-ке. Таким образом, на кл-ой м-не формируется разность потенциалов с отрицательным зарядом внутри кл-ки и положительным снаружи.
3. Работа натрий-калиевого насоса, которая вносит вклад в создание ПП. Этот встроенный в м-ну белок называют Na+, K+ АТФазой. Расщепляя 1 молекулу АТФ, этот насос переносит 3 иона натрия из кл-ки наружу и 2 иона калия снаружи внутрь. На 2 положительных заряда, поступающих в кл-ку, выносится 3 положительных заряда из кл-ки. Этот насос косвенно способствует поляризации м-ны, создавая высокую концентрацию калия в кл-ке.
ПД – это быстрое, высокоамплитудное изменение заряда м-ны, вызываемое действием достаточно сильных (сверхпороговых) раздражителей, это волнадеполяризации, распрост-ся от тела клетки по аксону к нервным окончаниям.Характерным признаком наличия ПД служит появление кратковременной инверсии (перемены) знака заряда на м-не. Снаружи он на короткое время (0,5-2мс) становится «». Величина инверсии может составлять до 30мВ, а величина всего ПД – 60-130мВ. Потенциал действия запускается образованием Nа+-каналов, связанных с рецепторами нейромедиаторов (канал обеспечивает облегчённая диффузия). Эти каналы создают пороговый потенциал, равный приблизительно 10 мВ. Преодоление порогового потенциала открывает потенциалчуствительные Nа+- каналы, через которые внутрь аксона устремляется Nа+. Потенциал принимаем имеющим отрицательное значение (-75 мВ), потому что внутриклеточное содержимое заряжено отрицательно. Чем сильнее изменяется потенциал – тем сильнее и больше открываются Nа+- каналы. Потенциал +20 мВ – это максимальный положительный потенциал, возникающий на аксоне – он называется потенциал действия. Однако натриевые каналы остаются открытыми не более 1-2мс. Через такое время от момента начала ПД закрываются инактивационные ворота и натриевые каналы становятся непроходимыми для Na+. Поэтому поток Na+ внутрь кл-ки резко ограничивается, а поток ионов калия из кл-ки наружу возрастает из-за открытия калиевых каналов. Поток K+ удаляет из кл-ки избыток «+» зарядов и м-на быстро реполяризуется – на ее внутренней стороне восстанавливается «-» заряд.
Если на кл-ку действует сверхпороговый раздражитель, то величина локального потенциала достигает уровня Ек и возникает ПД. В этот момент возбудимость кл-ки мгновенно падает до нулевого уровня. Начинается фаза абсолютной рефрактерности (невозбудимости). Эта фаза длится до начала реполяризации. После начала реполяризации возбудимость кл-ки начинает возрастать, но остается пониженной относительно уровня нормы – фаза относительной рефрактерности. Во время следовой отрицательной возбудимость кл-ки повышена – фаза супернормальной возбудимости (экзальтации), а во время следовой положительности – понижена (фаза субнормальной возбудимости).
Возбудимость кл-ки имеет прямую зависимость от разности уровней потенциала покоя (Е0) и потенциала критической деполяризации (Ек). Эту разность называют пороговым потенциалом (ΔЕ):
ΔЕ= Е0 - Ек.
Чем меньше ΔЕ, тем больше возбудимость.
ПД подразделяют на участки: деполяризацию, реполяризацию и гиперполяризацию.
Деполяризацией называют всю восходящую часть ПД, в ней выделяют участок, соответствующий локальному потенциалу (от уровня Е0 до Ек), быструю деполяризацию (от уровня Ек до уровня 0мВ), инверсию знака заряда (от 0мВ до начала реполяризации). Далее идет реполяризация. Приближаясь к уровню Е0, ее скорость может замедляться, и этот участок называют следовой отрицательностью (или следовым отрицательным потенциалом). У некоторых клеток вслед за реполяризацией идет гиперполяризация (возрастание поляризации м-ны). Ее называют следовым положительным потенциалом.
Начальную высокоамплитудную быстропротекающую часть ПД называют также пик или спайк. Он включает фазы деполяризации (до следового
Равновесн. процессы – бесконечно медленные процесс., они предст-т идеализир-ное описание реальных процессов. Е.
25. Биофизические механизмы возбудимости.Потенциал действия – волна деполяризации, распространяющаяся вдоль тела аксона. Нервный импульс это и есть волна деполяризации. Проведение нервного импульса это и есть потенциал действия. Потенциал (из физики) – напряжение. Проведение импульсов возможно тогда, когда ПД достигнет перехвата Ранвье и приводит к открытию потенциалчувствительных натриевых каналов.
Потенциал покоя обеспечивается неравномерным распределением ионов Nа+ и К+ и избирательной проницаемостью к ионам плазматической мембраны аксона. Электрический потенциал мембраны – 10 мВ. Внутри к-к – избыток «-«заряда, снаружи «+». Циклическое изменение потенциала аксона и называется потенциалом действия. Запускается нервный импульс (потенциал действия) взаимодействием нейромедиаторов соответствующими рецепторами на постсинаптической мембране.
Покоящийся аксон характеризуется потенциалом покоя, под которым понимаем трансмембранный потенциал, который равен -70 мВ, существующий в каждой точке возбуждённого волокна. Первые эксперименты по измерению трансмембранного потенциала были проведены учёными Ходжкин и Катц на гигантском аксоне кальмара.
График ПД – это график зависимости электрического потенциала мембраны от времени.
ПД подразделяют на участки: деполяризацию, реполяризацию и гиперполяризацию.
Деполяризацией называют всю восходящую часть ПД, в ней выделяют участок, соответствующий локальному потенциалу (от уровня Е0 до Ек), быструю деполяризацию (от уровня Ек до уровня 0мВ), инверсию знака заряда (от 0мВ до начала реполяризации). Далее идет реполяризация. Приближаясь к уровню Е0, ее скорость может замедляться, и этот участок называют следовой отрицательностью (или следовым отрицательным потенциалом). У некоторых клеток вслед за реполяризацией идет гиперполяризация (возрастание поляризации м-ны). Ее называют следовым положительным потенциалом.
Начальную высокоамплитудную быстропротекающую часть ПД называют также пик или спайк.
В механизме развития ПД важнейшая роль принадлежит увеличению проницаемости клеточной м-ны для ионов Na+. При действии на кл-ку электрического тока он вызывает ее деполяризацию, и когда заряд м-ны уменьшается до критического уровня (Ек) – открываются электроуправляемые натриевые каналы. Чтобы канал мог пропустить Na+, необходимо, чтобы все его ворота были открыты. Это и происходит, когда деполяризация достигает уровня Ек. Открытие натриевых каналов приводит к лавинообразному вхождению натрия внутрь кл-ки. Поскольку ионы натрия несут «+» заряд, они нейтрализуют избыток «-» зарядов в кл-ке, затем на внутренней стороне м-ны происходит инверсия (перемена) знака заряда с «-» на «+».
Однако натриевые каналы остаются открытыми не более 1-2мс. Через такое время от момента начала ПД закрываются инактивационные ворота и натриевые каналы становятся непроходимыми для Na+. Поэтому поток Na+ внутрь кл-ки резко ограничивается, а поток ионов калия из кл-ки наружу возрастает из-за открытия калиевых каналов. Поток K+ удаляет из кл-ки избыток «+» зарядов и м-на быстро реполяризуется – на ее внутренней стороне восстанавливается «-» заряд.
Если на кл-ку действует сверхпороговый раздражитель, то величина локального потенциала достигает уровня Ек и возникает ПД. В этот момент возбудимость кл-ки мгновенно падает до нулевого уровня. Начинается фаза абсолютной рефрактерности (невозбудимости). Эта фаза длится до начала реполяризации. После начала реполяризации возбудимость кл-ки начинает возрастать, но остается пониженной относительно уровня нормы – фаза относительной рефрактерности. Во время следовой отрицательной возбудимость кл-ки повышена – фаза супернормальной возбудимости, а во время следовой положительности – понижена (фаза субнормальной возбудимости).
Возбудимость кл-ки имеет прямую зависимость от разности уровней потенциала покоя (Е0) и потенциала критической деполяризации (Ек). Эту разность называют пороговым потенциалом (ΔЕ):
ΔЕ= Е0 - Ек.
Чем меньше ΔЕ, тем больше возбудимость.
Ионные каналы действуют не по всей длине аксона, а только в перехватах Ранвье. Перемещение ионов поперек волокна обеспечивается чрезвычайно высокую скорость распространения импульсов вдоль волокна.
26.Синапсы Синапс – специализированная ст-ра, обеспечивающая передачу возбуждающих или тормозных влияний с одной возбудимой кл-ки на другую(контакт 2-х нервных клеток). Это может быть передача возбуждения или торможения с одной нервной кл-ки на другую, с нервной кл-ки на волокно скелетной или гладкой мышцы, а также с рецепторной кл-ки на нервное волокно.
Синапс состоит из 1) пресинаптической мембраны (внутри имеются везикулы, содержащие нейромедиаторы – норадреналин, ГАМК, ацетилхолин и т. д.) 2) синаптическая щель и 3) постсинаптическая мемб. (содержит специфические рецепторы, реагирующие с нейромедиаторами).
По механизму передачи возбуждения синапсы подразделяют на электрические, химические, смешанные. В электрических синапсах возбуждение передается электротонически, за счет локальных круговых токов м-ду пре- и постсинаптическими м-ми. Эти м-ны находятся очень близко друг к другу (на расстоянии 1-2нм), м-ду ними существуют целевые контакты, обладающие хорошей электропроводностью. Большинство синапсов в организме человека – химические.
По признаку медиатора (в-ва-посредника), выделяемого в синапсах, их подразделяют на: холинэргические – ацетилхолин, адренергические – адреналин и норадреналин и др. Медиаторами могут быть дофамин, аминокислоты глутамин и аспарагин, выполняющие возбуждающую функцию в нервных центрах. Тормозные влияния передаются чаще всего нейромедиаторами глицином и гамма-аминомасляной кислотой (ГАМК).
В передаче возбуждения в синапсах могут участвовать пептиды: в-во П, ВИП (вазоинтестинальный пептид), соматостатин, эндорфины, энкефалины. Эти в-ва выделяются вместе с основным медиатором (ацетилхолином, норадреналином, серотонином) и оказывают модулирующее действие на передачу возбуждения в синапсе
28.Основные понятия и законы фотофизики и фотохимии. Спектральные методы широко применяются для изучения разнообразных свойств и реакций биологических систем и макромолекул. Среди спектральных методов наибольшее распространение получили оптические методы. Основные параметры светового излучения:
-длина волны λ (нм) и частота излучения ν (Гц), связанные соотношением ν = с/λ (с - скорость света),
-энергия кванта света Е = ħ∙ν (ħ – постоянная Планка),
- интенсивность излучения I = n∙E (n- число квантов в световом потоке).
Оптический диапазон длин волн включает ультрафиолетовое (200-400 нм), видимое (400- 800 нм), инфракрасное (800-10000 нм) излучение.
Поглощение света веществом – внутримолекулярный одноэлектронный физический процесс. Свет поглощается молекулами, при этом электрон переходит из основного в энергетически более высокое возбужденное состояние. Вся энергия кванта света поглощается сразу за время 10-15- 10-14с, поглощение света – процесс дискретный.
Свет представляет электромагнитную волну, при взаимодействии с веществом свет ведет себя подобно потоку частиц(квантов света или фотонов). Энергия фотонов определяется длиной волны излучения. Из квантов света с различными энергиями могут поглощаться только те, энергия которых соответствует энергии переходов между какой-либо парой уровней в молекуле вещества.
Каждый электрон в молекуле находится на определенной орбитали и обладает определенной энергией. Таким образом, в молекуле существует система электронных энергетических уровней.
Способность молекул поглощать свет лежит в основе спектрофотометрии. Поглощение света проявляется в ослаблении светового потока после прохождения через исследуемый объект, и оно тем больше, чем выше концентрация вещества (с, моль∙л–1), толщина раствора (1, см), способность вещества к поглощению. Для монохроматического света эти закономерности выражаются законом Бугера — Ламберта — Бера: Д=lg∙I0/I = εcl, где D — так называемая оптическая плотность образца, I0 и I — интенсивности падающего и прошедшего через раствор вещества света. Величину ε (моль-1 л см-1) называют молярным коэффициентом экстинкции. Иногдаиспользуют параметр поперечное сечение поглощения s. Физический смысл s — эффективное сечение молекулы, при попадании в которое происходит поглощение фотона данной длины волны.
Графики, выражающие зависимости оптической плотности D, коэффициента молярной экстинкции ε или s от длины волны, называются спектрами поглощения. Электронные спектры поглощения возникают в результате переходов электронов в возбужденные состояния
29 Биофизика регуляторных процесссов Нервная регуляция - координирующее влияние нервной системы (НС) на клетки, ткани и органы, приводящее их деятельность в соответствие с потребностями организма и изменениями окружающей среды; один из основных механизмов саморегуляции функций. Вследствие Н. р. деятельность клеток и органов может инициироваться, прекращаться, усиливаться, ослабляться; могут меняться функциональное и биохимическое состояние клеток и органов, особенности их строения. Возникшее в какой-либо из клеток возбуждённое состояние поверхностной мембраны может иногда распространяться, охватывая клетку за клеткой (так называемое нейроидное проведение — процесс, по ионному механизму схожий с проведением импульса нервного). Н. р. может быть быстрой и локальной. Это обеспечивается тем, что при Н. р. медиатор выделяется из нервных окончаний прямо на иннервированные клетки, а также тем, что выделение медиатора вызывается быстро распространяющимся сигналом — нервным импульсом. Между Н. р. и гормональной регуляцией нет резкой границы, некоторые нервные окончания выделяют активные вещества в кровь. Быстрота и адресованность Н. р. особенно важны при регуляции движений, поэтому НС хорошо развита у организмов с совершенной локомоцией. Под нервным контролем находятся как исполнительные (эффекторные), так и чувствительные (рецепторные) органы и клетки, а также все вегетативные функции. Н. р. распространяется и на ткани, обеспечивающие метаболические потребности организма (например, жировая ткань). Чтобы медиатор мог подействовать на клетку, она должна быть чувствительной к нему, т. е. иметь соответствующие рецепторы. Так, в скелетной мышце позвоночных на поверхности каждого мышечного волокна расположены так называемые холинорецепторы, которые вступают во взаимодействие с медиатором двигательных нервных окончаний — ацетилхолином. В результате реакции между медиатором и рецептором меняется ионная проницаемость поверхностной мембраны иннервированной клетки. При этом изменяются ионный состав цитоплазмы и мембранный потенциал, вследствие чего специфическая деятельность клетки усиливается или угнетается. По-видимому, в некоторых случаях медиатор может оказывать прямое, не опосредованное ионами, влияние на процессы обмена веществ клетки.
Гуморальная регуляция - координация физиологических и биохимических процессов, осуществляемая через жидкие среды организма (кровь, лимфу, тканевую жидкость) с помощью биологически активных веществ (метаболиты, гормоны, гормоноиды ионы), выделяемых клетками, органами и тканями в процессе их жизнедеятельности. У высокоразвитых животных и человека Г. р. подчинена нервной регуляции и составляет совместно с ней единую систему нейрогуморальной регуляции. Продукты обмена веществ действуют не только непосредственно на эффекторные органы, но и на окончания чувствительных нервов (хеморецепторы) и нервные центры, вызывая гуморальным или рефлекторным путём те или иные реакции. Так, если в результате усиленной физической работы в крови увеличивается содержание CO2, то это вызывает возбуждение дыхательного центра, что ведёт к усилению дыхания и выведению из организма излишков CO2. Гуморальная передача нервных импульсов химическими веществами, т. н. медиаторами, осуществляется в центральной и периферической нервной системе. Наряду с гормонами важную роль в Г. р. играют продукты межуточного обмена.
Мембранная регуляция.
Плазматическая мембрана обеспечивает сохранение разности концентраций метаболитов и неорганических ионов между внутриклеточной и внешней средой. Контролируемый транспорт метаболитов и ионов определяет внутреннюю среду, что существенно для гомеостаза, т.е. поддержания постоянной концентрации метаболитов и неорганических ионов, и других физиологических параметров. Регулируемый и избирательный транспорт метаболитов и неорганических ионов через поры и посредством переносчиков становится возможным благодаря обособлению клеток и органелл с помощью мембранных систем.
В мембранах на границе между липидной и водной фазами локализованы ферменты. Именно здесь происходят реакции с неполярными субстратами. Примерами служат биосинтез липидов и метаболизм неполярных ксенобиотиков. В мембранах локализованы наиболее важные реакции энергетического обмена, такие, как окислительное фосфорилирование (дыхательная цепь) и фотосинтез.
30 Мембранный механизм сигнализации В основе теории гормональной регуляции, разработанной Эрлом Сазерлендом в 1951, лежит теория вторичных мессенджеров (посредники, переносчики).

Рецептор сод-т высокоспецифический центр связывания гормона. Взаим-е гормона с рецептором приводит к активации рецептора. Активированный рец-р взаим-ет с G-белком (GTP, ГТФ-связывающий белок). G-белок с ГТФ нах-ся в активном состоянии, а с ГДФ- в неактивном.
G-белок наз-т трансдуктором, т.к. переносит сигнал от рецептора к белку-эффектору (аденилатциклаза - А). А катализир-т цАМФ виз АТФ. цАМФ принадлежит ко вторичным мессенджерам. Помимо цАМФ в роли вторичных мессенджеров могут выступать: диацилглицерол (ДАГ), иназитолтрифосфат (IP3), Са2+, NO.
Каскад переноса сигнала обеспечивает:
1. специализацию сигнала,
2. его многократное усиление
цАМФ взаим-т с протеинкеназами, кот.в свою очередь катализ-т р-wb. Фосфорилирования ферментов, переводя их в активное состояние.
В итоге любой внеклеточный сигнал приводит к:
1) измен-ю активности соответствующих ферментов,
2) измен-ю ур-ня экспрессии ферментов,
3) измен-ю ионной проницаемости мембраны.
Дата добавления: 2015-10-29; просмотров: 128 | Нарушение авторских прав
| <== предыдущая страница | | | следующая страница ==> |
| Movements and ideologies | | | GRAMMAR IN THE SYSTEMIC CONCEPTION OF LANGUAGE |