
|
Читайте также: |
Нанесение надписи на ампулы производят на полуавтомате (рис. 13.24). В бункер (7) загружают ампулы и барабаном подачи (8) направляют к офсетному цилиндру, на котором нанесены буквы и цифры надписи, вдавленные в виде углубления в 40-50 мкм. Формный цилиндр (5), вращаясь в ванне с быстро-высыхающей краской для глубокой печати, подает ее на офсетный цилиндр. Избыток краски с помощью ракеля (4) и регулирующего устройства снимается с поверхности офсетного цилиндра и остается в углублениях надписи. При контакте надпись наносится на ампулу, быстро высыхает и ампулы передаются на упаковку.
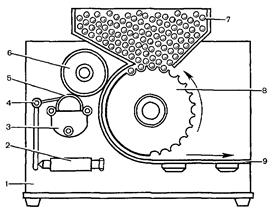
Рис. 13.24. Устройство полуавтомата для маркировки ампул.
1 - корпус; 2 - регулирующее устройство; 3 - ванна; 4 - ракель; 5 - формный цилиндр; 6 - офсетный цилиндр;
7- бункер; 8 - барабан подачи ампул; 9 - направляющие.
На автомате для упаковки ампул вместимостью 5 мл (модель 529) на полимерной пленке при нагревании формируются ячейки пуансонами и сжатым воздухом. Из питателя в ячейки попадают ампулы, а сверху накладывается фольга, термосклеивающаяся под действием пресса. Из общей ленты вырезаются готовые упаковки, они поступают в накопитель.
На автомате для упаковки ампул вместимостью 1 мл (модель 570) происходит одновременно упаковка и маркировка. Пленка полихлорвинила размягчается нагревателем, ячейка формируется вакуумом при одновременной маркировке ампул. Они загружаются в ячейки, происходит термосклеивание с верхним покровным материалом. На упаковку горячим теснением наносится серия, срок годности препарата, готовая упаковка вырезается и попадает в накопители. Имеются автоматы для упаковки ампул в картонные коробки по 10 штук.
В качестве примера приводим технологию нескольких растворов.
Раствор желатина медицинского 10% для инъекций (Solutio Gelatinae medici-nalis 10% pro injectionibus) получают из желатина медицинского, проверяют силу н крепость 10% геля, относительную вязкость 14,82% раствора, проводят бактериологические исследования. Желатин для инъекции в растворе 1:10 не должен быть мутнее эталона № 3 и выдержать испытание на пирогенность при введении 10 мл его на 1 кг массы животного.
Желатин в виде мелких пластинок ставят на 20 мин для набухания в воде, переносят в реактор и заливают кипящей водой. После полного растворения значение рН раствора доводят щелочью до 9,0-0,7, а концентрацию вещества - до 10%, устанавливают температуру 80°С и выдерживают 40 мин для частичного разрушения примесей белкового характера и пирогенных веществ. Раствор охлаждают до 60°С, значение рН доводят до 6,8-7,0, добавляют 3 белка куриных яиц на 1 л, уголь активированный, натрия хлорид (для стабилизации желатина) и с помощью миксера интенсивно перемешивают. Температуру повышают до 105°С и выдерживают 15-20 мин. Белковые примеси коагулируют и адсорбируют углем. Раствор охлаждают до 90°С, фильтруют на друк-фильтре через 4 слоя бязи и слой фильтровальной бумаги, затем через фильтр ХНИХФИ с толщиной ровницы 3-4 см, ампулируют по 10 и 25 мл. Стерилизуют при температуре 105°С 30 мин, медленно повышают ее до 120°С и выдерживают 15 мин. После стерилизации ампулы помещают в термостат на 7 сут при 38-40°С. Раствор не должен мутнеть. Проводится анализ раствора по следующим показателям: подлинность, относительная вязкость, температура плавления, значение рН, прозрачность и цветность. Препарат испытыва-ется на пирогенность и стерильность. Технология раствора преследует цель - максимально удалить пирогенные вещества \\/ белки с антигенными свойствами и одновременно сохранить способность желатинирования (гелеобразования). Перед введением раствор подогревается до 37°С.
Раствор кальция глюконата 10% для инъекций (Solutio Calcii gluconatis 10% pro injectionibus). Кальция глюконат медленно растворим в 50 частях воды и растворим в 5 частях кипящей воды, таким образом, 10% раствор пересыщен. В отличие от многих солей кальция глюконат при нагревании улучшает растворимость. Поэтому растворение проводят при нагревании в течение 3 ч.
В кальция глюконате содержится примесь кальция оксалата как побочный продукт при получении вещества, который во время растворения образует комплекс с кальция глюконатом, а при стерилизации и хранении выпадает в осадок. Его удаляют добавлением кристалликов кальция оксалата в качестве затравки и для повышения концентрации одноименных ионов. При охлаждении образуется осадок, поэтому раствор фильтруют в горячем состоянии. Его анализируют, проверяют значение рН, расфасовывают и стерилизуют паром под давлением при температуре 110°С в течение 1 ч. При более высоких температурах происходит карамелизация. Перед введением раствора больному необходимо убедиться, что шприц и игла не содержат этанол, так как в этом случае в момент введения препарата выпадает осадок. Выпускают в ампулах по 10 мл.
Раствор глюкозы 5, 10, 25 и 40% для инъекций (Solutio Glucosi 5, 10, 25, 40% pro injectionibus). Исходная глюкоза подвергается анализу на прозрачность и цветность ее растворов, кислотность, наличие хлоридов, сульфатов, кальция, бария. Тяжелых металлов допускается не более 0,0005% при отсутствии мышьяка. Раствор получают с учетом содержания кристаллизационной воды в глюкозе двойной очисткой активированным осветляющим углем марки «А». Гидратную глюкозу растворяют при температуре 50-60°С и добавляют уголь активированный, обработанный кислотой хлороводородной. *Для удаления примесей и активирования перемешивают 10 мин и еще добавляют уголь активированный, перемешивают, фильтруют через бельтинг и бязь. Затем раствор доводят до кипения, охлаждают до температуры 60°С, добавляют уголь активированный, перемешивают 10 мин и фильтруют. К раствору добавляют стабилизатор Вейбеля (натрия хлорид и 0,1 н. раствор кислоты хлороводородной), перемешивают, анализируют и фильтруют через фильтр ХНИХФИ, ампулируют и стерилизуют в паровом стерилизаторе при температуре 100-102°С в течение 1 ч. В растворе проверяется подлинность, цветность, значение рН среды (должно быть 3,0-4,0). 5% раствор при введении 10 мл на 1 кг массы животного должен быть апирогенным. Проверяется его стерильность.
Номенклатур* растворов для инъекций включает около 250 наименований. Имеются особенности приготовления других растворов в промышленном производстве. Например, раствор гексаметилентетрамина при повышенной температуре гидролизуется, поэтому он изготовляется в асептических условиях без стерилизации. Для приготовления раствора эуфиллина (2,4%) используют специальный сорт «для инъекций» с повышенным содержанием этилендиамина - 18-22% вместо 14-18%. Раствор цианкобаламина получают на 0,9% растворе натрия хлорида для изо-тоннрования, раствор диколина - с 0,25% натрия цитрата для поддержания значения рН в интервале 4,2-4,9. Проверена и доказана необходимость газовой защиты для растворов папаверина гидрохлорнда, алкалоидов спорыньи, тиамина хлорида. Раствор кон-валлотоксина 0,03% консервируют 0,1% нипагином и этанолом. Раствор коргликона 0,06%-0,4% хлор-бута нол гидратом.
Кроме лекарственных форм для инъекций в промышленном производстве готовят глазные лекарственные формы.
13.11. ГЛАЗНЫЕ ЛЕКАРСТВЕННЫЕ ФОРМЫ
(FORMAE MEDICAMENTORUM OPHTALMICAE)
В промышленном производстве готовят глазные лекарственные формы: капли, мази, пленки. Они выделяются в отдельную группу в связи с особенностями, вытекающими из строения и функций органа зрения^ такими как специфические механизмы всасывания, распределение и взаимодействие лекарственных веществ с тканями и жидкостями глаза, легкая ранимость глаза и т. д. При многих заболеваниях глаз резко изменяется проницаемость мембран и часто в слезной жидкости уменьшается содержание лизоцима (фермент муромидаза), что снижает защищенность от воздействия микроорганизмов. 'Поэтому наряду с общими требованиями для многих готовых лекарственных форм к ним предъявляются повышенные требования: стерильность, стабильность, изотонич-ность, отсутствие механических включений и раздражающего действия, точность дозирования. Для выполнения перечисленных требований производство глазных лекарственных форм осуществляется так же, как и лекарственных форм для инъекций^Наиболее ответственные операции - приготовление раствора, наполнение флаконов и их укупорка проводятся в помещениях или зонах 1-го класса чистоты в ламинарном потоке стерильного воздуха на автоматических или полуавтоматических линиях при минимальном контакте с окружающим воздухом. Особенно это относится к асептически изготовляемым препаратам, не подвергающимся термической стерилизации.^Аналогичные требования предъявляются к качеству исходных лекарственных веществ и растворителей.
Дата добавления: 2015-10-28; просмотров: 228 | Нарушение авторских прав
| <== предыдущая страница | | | следующая страница ==> |
| БРАКЕРАЖ АМПУЛИРОВАННЫХ РАСТВОРОВ | | | ТЕОРЕТИЧЕСКИЕ ОСНОВЫ ЭКСТРАГИРОВАНИЯ |