
Читайте также:
|
Рассмотрим особенности охлаждения или нагревания реального газа в процессе Джоуля – Томсона на примере газа Ван-дер-Ваальса. Для простоты примем, что масса газа составляет один моль. Прежде всего найдем выражение для производной  , которая входит в формулу (28) для коэффициента Джоуля – Томсона. Для этого продифференцируем обе части уравнения (3) по T при P = const, полагая
, которая входит в формулу (28) для коэффициента Джоуля – Томсона. Для этого продифференцируем обе части уравнения (3) по T при P = const, полагая 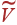 функцией T. В результате получаем уравнение
функцией T. В результате получаем уравнение
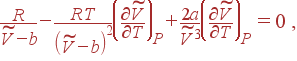
|
откуда

| (31) |
Подставим теперь (31) в (28). Имеем

|

|
или

| (32) |
Таким образом, коэффициент Джоуля – Томсона обращается в нуль при условии
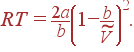
| (33) |
При использовании приведенных переменных (8) это условие принимает вид

| (34) |
Если разрешить (34) относительно переменной v и подставить в (10), то получается уравнение инверсии

| (35) |
решение которого имеет вид

| (36) |
Наконец, возвращаясь к переменным T и P, приходим к следующей формуле для температуры инверсии

| (37) |
Эта формула определяет кривую инверсии на (T, P) диаграмме, которая имеет куполообразную форму (рис. 11). Область положительного эффекта Джоуля – Томсона находится под кривой.

|
Из формулы (37) видно, что при P < 9 Pk имеется две точки инверсии, различие между которыми уменьшается с ростом P. При P = 9 Pk верхняя и нижняя точки инверсии сливаются в одну точку
| Ti 0 = 3 Tk. | (38) |
Для большинства газов нижняя точка инверсии лежит в области жидкого состояния, и ее рассмотрение не представляет интереса.
Максимальная температура инверсии, соответствующая  , согласно (37) равна
, согласно (37) равна

| (39) |
Это соотношение приближенно выполняется для большинства газов. Так, для кислорода Ti max составляет 893 K а Tk – 154 K. Для водорода Ti max = 205 K, а Tk = 33 K. Для гелия Ti max = 40 K, а Tk = 4,2 K. Из этих данных следует, что при нормальных температурах водород и гелий нагреваются в процессе Джоуля – Томсона. Поэтому для сжижения их нужно предварительно охладить до температуры ниже температуры инверсии.
Вопросы
Дата добавления: 2015-09-02; просмотров: 545 | Нарушение авторских прав
| <== предыдущая страница | | | следующая страница ==> |
| Эффект Джоуля – Томсона | | | Магия чуда |