
Читайте также:
|
Перед выполнением работ студенты обязаны ознакомиться с их теоретическими основами. Отчет по лабораторной работе должен быть выполнен в соответствии с СТО ИрГТУ.005-2007 и содержать теоретические основы работы, описание установки, экспериментальную и расчетную части, выводы. Все графики в отчете представляются на миллиметровой бумаге.
Работа 1. Определение константы скорости восстановления йода пероксидом водорода
Цель работы: ознакомление с закономерностями протекания гомогенных реакций первого порядка и определение константы скорости реакции.
Примером реакции первого порядка является реакция восстановления йода при окислении его ионов пероксидом водорода.
При этом протекают следующие реакции:
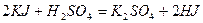 , (а)
, (а)
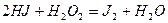 , (б)
, (б)
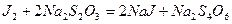 . (в)
. (в)
Реакции (а) и (в) практически мгновенны, так как являются ионными, поэтому скорость процесса определяется скоростью реакции (б). Концентрация ионов йода поддерживается постоянной за счет прибавления одинаковых количеств гипосульфита натрия (по 0,5 см3), что сдвигает равновесие справа налево, возвращая пропорциональное количество ионов йода 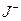 в реакцию. Скорость реакции определяется изменением концентрации пероксида водорода
в реакцию. Скорость реакции определяется изменением концентрации пероксида водорода 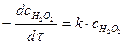 . Поэтому интегральная форма для расчета константы скорости будет иметь вид:
. Поэтому интегральная форма для расчета константы скорости будет иметь вид: 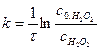 . При использовании этой формулы вместо концентраций пероксида водорода можно использовать его объемы.
. При использовании этой формулы вместо концентраций пероксида водорода можно использовать его объемы.
В ходе опыта в реакционную колбу приливается 10 см3 пероксида водорода. Однако к началу опыта некоторое его количество, пропорциональное объему в 0,5 см3, считаем вступившим в реакцию (б), так как в реакционной колбе находилось именно такое количество раствора гипосульфита натрия. Поэтому в начальный момент времени  . Каждая новая порция гипосульфита натрия в 0,5 см3 снижает количество пероксида водорода от начального в 9,5 см3 до
. Каждая новая порция гипосульфита натрия в 0,5 см3 снижает количество пероксида водорода от начального в 9,5 см3 до 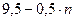 , где
, где 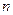 - порядковый номер добавления гипосульфита натрия в реакционный сосуд (
- порядковый номер добавления гипосульфита натрия в реакционный сосуд (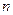 = 1 - это первое добавление,
= 1 - это первое добавление, 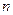 = 2 - второе добавление и т.д.), т.е.
= 2 - второе добавление и т.д.), т.е. 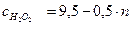 . Отсюда
. Отсюда
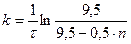 . (28)
. (28)
Приборы и материалы: технические весы, цилиндр на 500 см3, колба на 1 дм3, бюретка, пипетки на 10 и 20 см3 по 1 шт., секундомер, порошкообразный 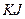 . Растворы: 0,1М
. Растворы: 0,1М 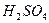 , 0,05М
, 0,05М  , 0,05М
, 0,05М 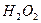 , крахмал.
, крахмал.
Дата добавления: 2015-08-10; просмотров: 48 | Нарушение авторских прав
| <== предыдущая страница | | | следующая страница ==> |
| Основные признаки протекания гетерогенного процесса | | | Порядок выполнения работы |