
Читайте также:
|
Соли вступают в реакции обмена с кислотами, щелочами, другими солями, если при этом образуются газ, осадок или малодиссоциирующее вещество:
K2СО3 + Н2SО4  K2SО4 + Н2О + СО2
K2SО4 + Н2О + СО2 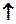
К2СО3 + Ва(ОН)2  2KОH + BaCO3
2KОH + BaCO3 
K2СО3 + СаС12  2КС1+CaCO3
2КС1+CaCO3 
Соли слабых кислородсодержащих кислот могут взаимодействовать с оксидами, соответствующими более сильным или менее летучим кислотам:
Nа2СО3 + SО3  Nа2SО4 + СО2
Nа2SО4 + СО2 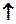
Na2CO3 + SiO3  Na2SiO3 + CO2
Na2SiO3 + CO2 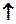
(крист.)
Кислые соли взаимодействуют со щелочами:
NаНСОз + NаОН  Nа2СО3 + Н2О
Nа2СО3 + Н2О
Основные соли реагируют с кислотами:
СuОНСI + НС1  СuС12 + Н2О
СuС12 + Н2О
Многие соли разлагаются (нерастворимые карбонаты, силикаты, сульфиты; сульфаты тяжелых металлов, все нитраты, все соли аммония; кислые соли разлагаются на кислоту и среднюю соль, основные соли - на оксид металла и кислоту):
СаСОз  СаО + СО2
СаО + СО2 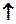
2СuSО4  2СuО + 2SО2
2СuО + 2SО2 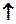 + О2
+ О2 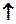
2Сu(NO3)2  2СuО + 4NO2 + О2
2СuО + 4NO2 + О2
NH4CI  NH3
NH3 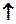 + HCI
+ HCI
NaHCO3  Na2CO3 + H2O + CO2
Na2CO3 + H2O + CO2 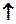
(CuOH)CO3  2CuO + H2O + CO2
2CuO + H2O + CO2 
Соли вступают в реакции замещения с металлами, если металл в составе соли менее активен, чем простое вещество:
СuSО4 + Zn  ZnS04 + Сu, но Сu + ZnSО4 -/>
ZnS04 + Сu, но Сu + ZnSО4 -/>
Дата добавления: 2015-07-25; просмотров: 57 | Нарушение авторских прав
| <== предыдущая страница | | | следующая страница ==> |
| Химические свойства кислот. | | | Способы получения оксидов, оснований, кислот, солей. |