
Читайте также:
|
Масса тигля  , г
, г
Масса меди  г
г
Масса тигля с сульфидом меди 
1-е взвешивание, г
2-е взвешивание, г
Расчет
1. Рассчитайте массу сульфида меди:
 .
.
2. Вычислите массу прореагировавшей серы:
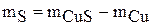 .
.
3. Предположив, что в состав молекулы сульфида меди входит xатомов Cu и yатомов S и приняв во внимание, что относительные атомные массы равны  ,
,  , можно составить следующее равенство 64x: 32y= = mCu: mS. Разделив первые члены этой пропорции на 64, а вторые – на 32, получим:
, можно составить следующее равенство 64x: 32y= = mCu: mS. Разделив первые члены этой пропорции на 64, а вторые – на 32, получим:
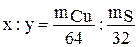 ,
,
где xи y– атомные факторы. Чтобы выразить атомные факторы в виде целых чисел, разделим их на наименьший из атомных факторов. Тогда формула сульфида меди будет СuaSв.
4. Рассчитайте массовые доли (в %) меди и серы в сульфиде меди:
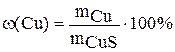 ,
,  .
.
Контрольные вопросы
1. Какую информацию о веществе дает его химическая формула?
2. В чем отличие простейшей формулы вещества от молекулярной (истинной)? Всегда ли простейшая формула вещества совпадает с молекулярной?
3. Что необходимо знать для установления простейшей формулы вещества, а также для нахождения молекулярной формулы химического соединения?
4. Почему перед началом опыта фарфоровый тигель прокаливают?
5. С какой целью в опыте выдерживают фарфоровый тигель с сульфидом меди в эксикаторе? Какие осушающие вещества применяют в эксикаторе?
Задачи
1. Определите простейшую формулу вещества, в котором массовая доля натрия составляет 43,4%, углерода – 11,3% и кислорода – 45,3%.
2. Определите простейшую формулу оксида ванадия, зная, что 2,73 г оксида содержит 1,53 г металла.
3. После прокаливания 14,26 г основного карбоната магния образовалось 8,06 г MgO, 1,8 г Н2О и 4,4 г СО2. Выведите формулу соли.
4. При полном сжигании 2,66 г некоторого вещества получилось 1,54 г СО2 и 4,48 г SO2. Определите простейшую формулу вещества.
5. Определите молекулярную формулу соединения, в котором массовая доля углерода составляет 54,5%, кислорода – 36,4% и водорода – 9,1%. Плотность соединения по водороду равна 44.
РАБОТА №4. УСТАНОВЛЕНИЕ ФОРМУЛЫ КРИСТАЛЛОГИДРАТА
Цель работы: на основании экспериментальных данных вывести формулу кристаллогидрата.
Приборы и химическая посуда: электронные весы, кварцевая чашка для взвешивания, шпатель, штатив с кольцом, фарфоровый тигель, фарфоровый треугольник, сухое горючее, тигельные щипцы, эксикатор.
Реактивы: кристаллогидраты солей хлорида кобальта (II), сульфата меди (II), сульфата никеля (II), карбоната натрия.
Дата добавления: 2015-07-25; просмотров: 274 | Нарушение авторских прав
| <== предыдущая страница | | | следующая страница ==> |
| Опыт проводится в вытяжном шкафу. | | | Результаты опыта |